|
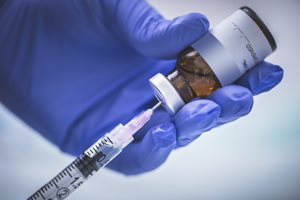
欧盟已对两款候选新冠疫苗展开滚动审评
2020.10.07
欧洲药品管理局(EMA)于 10 月 6 日宣布已开始对第二个 COVID-19 候选疫苗进行滚动审评,该疫苗为 BioNTech 与辉瑞公司合作开发的 BNT162b2 疫苗。此前,EMA 于 10 月 1 日宣布了针对 阿斯利康与牛津大学合作开发的 AZD1222 疫苗的首个滚动审评。
EMA 表示人用药委员...
|

|
七名前 FDA 局长联名呼吁美国政府停止对 FDA 信誉...
2020.10.02
继半个月前八名 FDA 现职专业负责人联名发表声明承诺基于科学的决策之后【FDA 专业负责人联名承诺:科学至上】,七名前任 FDA 局长于 9 月 29 日在《华盛顿邮报》的观点文章1中联名呼吁停止政府对 FDA 信誉的破坏。科学家应根据数据做出决策,不受政治压力或意识形态或既得利益...
|
|
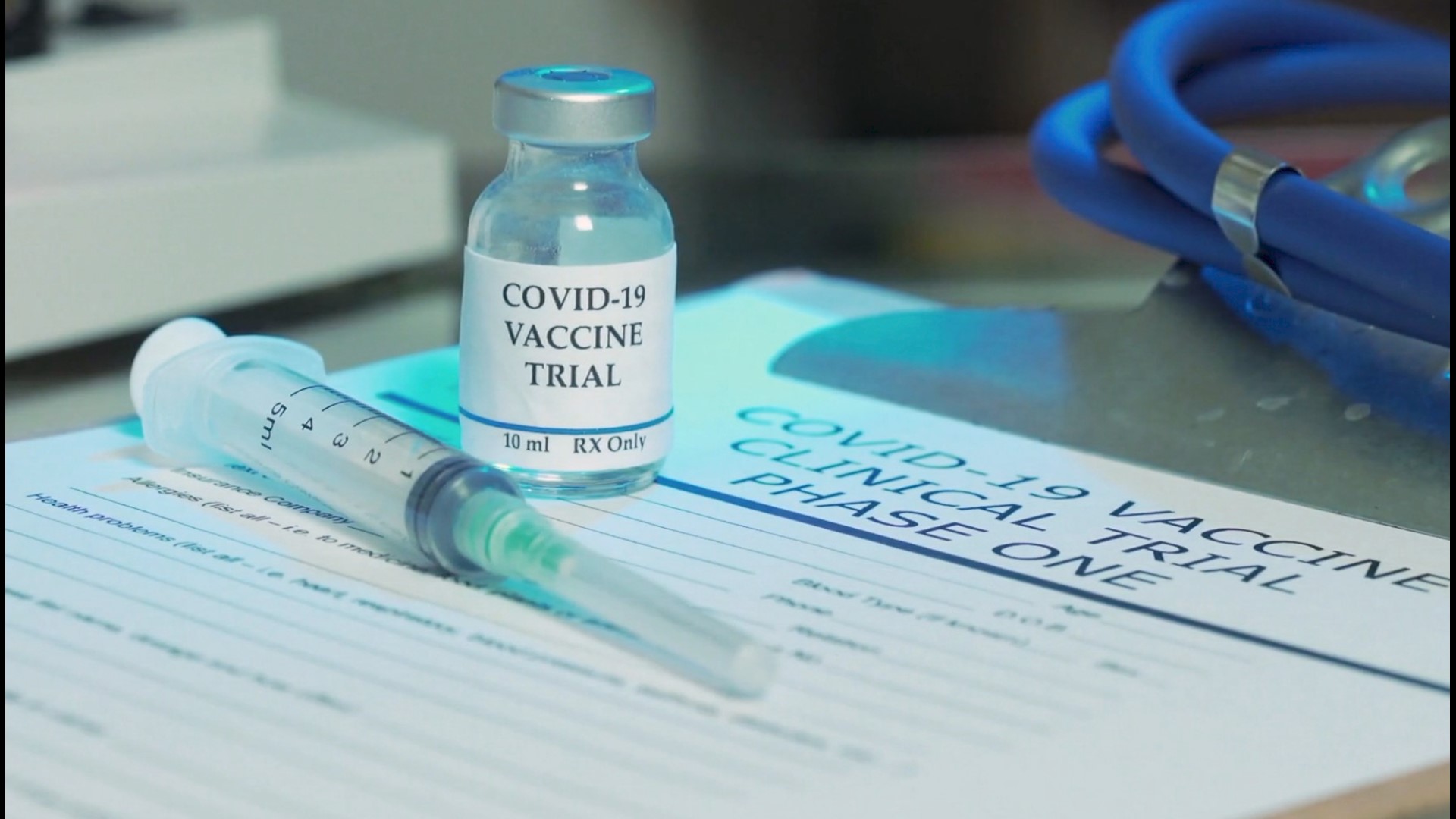
首个新冠疫苗获批后,其它试验如何维持安慰剂对照?
2020.09.22
美国 FDA 官员正在考虑如何确保即使在一款新冠疫苗成功获得监管许可后,仍然可以继续进行针对新冠疫苗候选者的随机、安慰剂对照 III 期临床试验。一旦 FDA 批准或紧急使用授权了新冠疫苗,试验受试者的招募可能会变得更加困难,已经入组的受试者可能希望退出试验转而接受已被证明有...
|

|
FDA 远程索要超五百份记录,将更新远程监管评价流程
2020.09.19
美国 FDA 监管事务办公室(ORA)在疫情期间已经在未现场检查的情况下对数百家药品生产场地的质量做出判断,FDA 助理局长 Elizabeth Miller 在 9 月 16 日 PDA/FDA 联合监管会议上的报告如是表示。
她指出,这为制药企业提供了一定程度的保证,即,在病毒广泛传播时,许多...
|

|
重新思考药品监管:加速快跑还是谨慎持重?
2020.09.17
最近在美印商会(USAIC)年度生物制品和医疗保健峰会上,业界讨论了一些有趣且存在争议的内容,关于新冠疫情是否为重新考虑药品监管流程提供了机会。
简化试验,加快监管进程
百康(Biocon)公司董事长 Kiran Mazumdar-Shaw 表示,大流行期间美国的曲速行动(Operation Warp Spe...
|
|
FDA 发布疫情期间制药企业复工复产指南
2020.09.14
美国 FDA 于 9 月 10 日发布《COVID-19 公共卫生紧急事件期间恢复正常的药品和生物制品生产运行》指南,关注疫情下恢复生产,缓解药品短缺并完成隔离批次的质量保证活动。
FDA 在指南中建议,随着 COVID-19 疫情的消退,制药企业在恢复全面 GMP 药品生产运营之时,应优先...
|
|
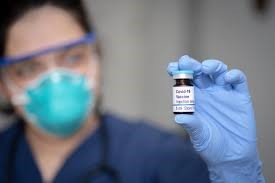
FDA 拟发布新冠疫苗紧急使用授权指南,或将要求更多...
2020.09.12
美国 FDA 生物制品审评与研究中心主任 Peter Marks 表示,FDA 可能会采用紧急使用授权(EUA)途径许可新冠疫苗,但全面许可通常会有更严格的安全性和有效性标准。
在 9 月 10 日 Duke-Margolis 卫生政策中心关于 COVID-19 疫苗接种的安全和有效性网络会议上,Marks 将这...
|

|
FDA 专业负责人联名承诺:科学至上
2020.09.12
在《今日美国》 9 月 10 日发表的一篇观点文章中,八名 FDA 职业领导联合表达了对于 FDA 基于科学的决策过程以及如何实现这一过程的承诺。他们在文中做出了这样的保证:科学将决定他们的决策。承诺文章的最后,作者们说承诺只代表他们个人,不代表FDA、卫生部和政府。也就是说,...
|
|
阿斯利康新冠疫苗试验暂停原因披露,且并非第一次试验...
2020.09.10
昨日医药领域最为引发热议的新闻之一恐怕就是阿斯利康/牛津大学 COVID-19 疫苗的 3 期试验因一名参与者出现与疫苗接种相关的疑似严重不良反应而暂停。现在事件又有了最新进展,我们一起来看看。
根据 STAT NEWS 的消息,阿斯利康首席执行官 Pascal Soriot 在美国时间周三上...
|
|
欧盟开始审评用于新冠治疗的地塞米松药品申请
2020.09.03
欧盟药品管理局(EMA)于 9 月 2 日表示,正在评估 Taw Pharma 的类固醇药物地塞米松 Taw(Dexamethasone Taw),作为 COVID-19 成年住院患者的潜在治疗方式。EMA 人用药委员会(CHMP)已经从 8 月 31 日开始审评 Taw Pharma 的上市申请。
该药的申请由英国咨询公司 Taw...
|
|
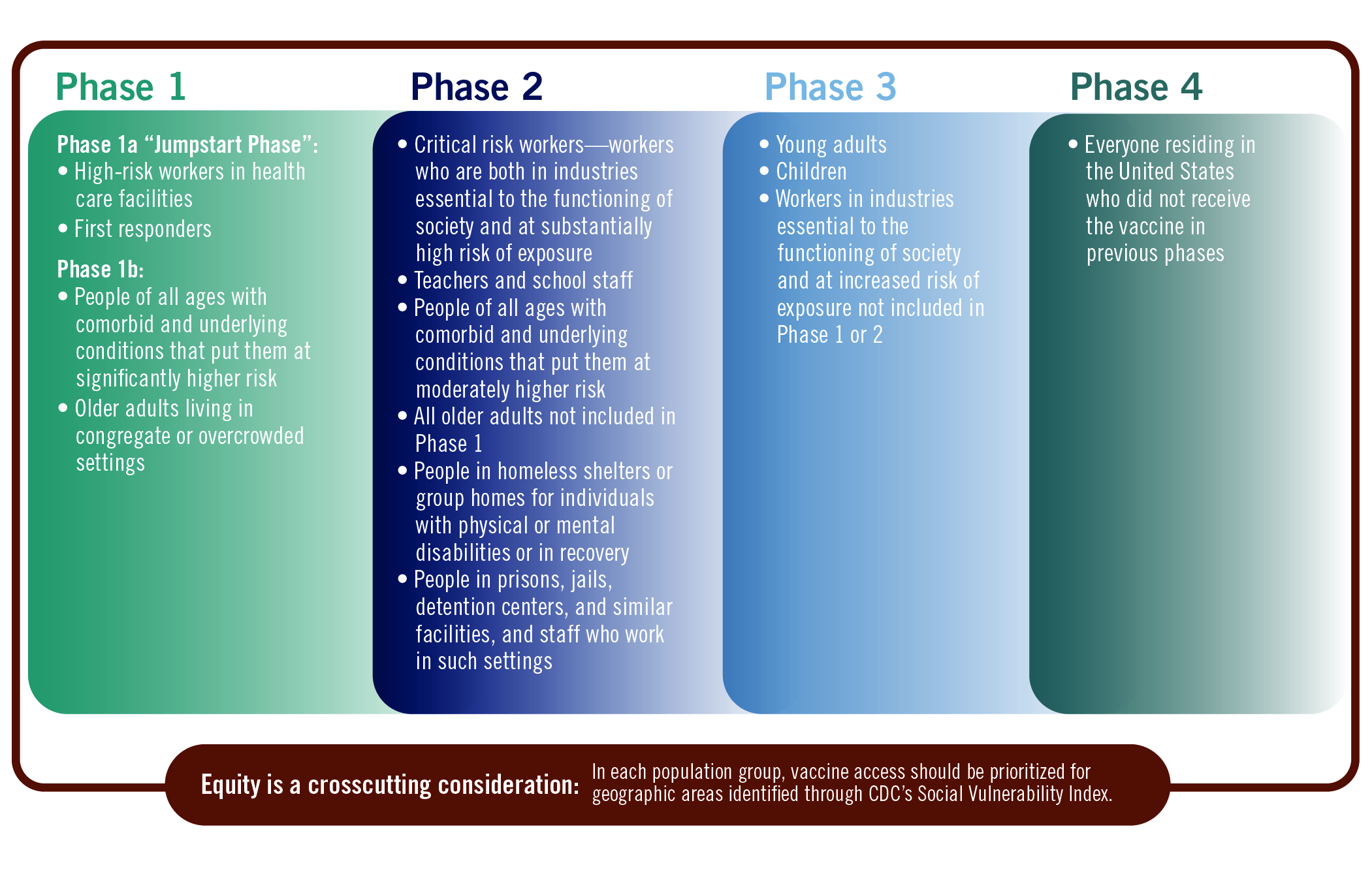
美国科学院发布 COVID-19 疫苗优先接种建议草案
2020.09.02
9 月 1 日,美国国家科学、工程和医学研究院发布了一份讨论哪些群体应优先接种 COVID-19 疫苗的报告草案,对于接种人群的优先级给出了详细建议。
报告题目为“公平分配 COVID-19 疫苗的初步框架讨论草案”,长达 114 页,由国家卫生研究院院长 Francis Collins 和美国疾控中心(C...
|

|
法律专家对 FDA 疫情期间检查指南的解读与预测
2020.09.01
法律专家认为美国 FDA 新发布的疫情期间药品检查问答指南为行业留下了一些余地,可以提出新的方法来评估 GMP 合规符合性而无需进行现场检查。法律专家认为,可灵活发挥的程度将取决于 FDA 如何执行该指南,以及是否会发布更多指南。
FDA 于 8 月 19 日发布《COVID-19 公共...
|

|
FDA 新冠康复期血浆紧急使用授权的证据是否支持结论...
2020.08.26
美国 FDA 于 8 月 23 日许可了新冠(COVID-19)康复期血浆的紧急使用授权(EUA),引发了业内的广泛批评。尤其是 EUA 的发布时间非常敏感,就在特朗普总统公开指责 FDA 为阻止他竞选连任而在 COVID-19 疫苗和治疗产品方面行动缓慢。人们担心 FDA 的决策可能受到政治压力和...
|

|
USP 使用标准品销售数据构建供应链风险模型预测药品...
2020.08.25
美国药典会(USP)正在建立一种风险模型,以帮助利益相关者评估药品供应链中如果不加以防治可能会导致药品短缺的漏洞。该模型基于对 USP 参照标准品的需求程度和地域分布,于今年早些时候启动,以应对 COVID-19 大流行期间的药品短缺问题。
USP 供应链分析高级总监 Vimala Raghaven...
|

|
美国总统公开指责 FDA 并限制其对新冠检测的监管
2020.08.24
【编者按】FDA 一直自视为独立的科学监管机构,尽管卫生部是其名义上司。史上只有一次 FDA 的决定被卫生部推翻,那就是 9 年前的避孕药事件。这次总统公开指责 FDA 为阻止他竞选连任,而拖延审批新冠病毒检测产品,卫生部又明令限制FDA对检测的监管。事态的发展,值得注意。
...
|

|
FDA 发布指南详述疫情期间现场检查策略
2020.08.21
美国 FDA 于 8 月 19 日发布《COVID-19 公共卫生紧急事件期间生产、供应链、药品和生物制品检查问答》即时生效指南,提供了与检查、待决药品申请和已批准药品生产设施变更相关的法规和政策常见问题解答。
FDA 在指南中确认,在 FDA 对申办人在其产品上市申请中列出的生产设...
|

|
美国国家研究所牵头研究 COVID-19 疫苗制造问题
2020.08.13
美国国家生物制药制造创新研究所(NIIMBL)于 7 月 28 日举办网络研讨会,会上目前新冠(COVID-19)疫苗研发的几大主要参与者探讨了疫苗制造技术问题以及 NIIMBL 可以帮助解决的方面。
为保护人们免受 COVID-19 感染,疫苗制造商将重点放在尽快生产疫苗上,但是针对速度的优...
|
|
FDA 局长和主任联合发文增强公众对新冠疫苗的信心
2020.08.12
为打消公众对于新冠(COVID-19)疫苗的担忧,增强疫苗的信心,美国 FDA 局长、副局长和生物制品中心主任联合撰文,向公众解释和保证对 COVID-19 疫苗的严格监管。
FDA 局长 Stephen Hahn 医学博士、生物制品审评与研究中心(CBER)主任 Peter Marks 医学博士和 FDA 副局长 Ana...
|

|
瑞德西韦:向 FDA 提交新药申请,与辉瑞合作扩大生...
2020.08.11
吉利德(Gilead)公司的瑞德西韦(remdesivir)是至今为止唯一一个获得监管部门批准用于治疗 COVID-19 患者的药品。瑞德西韦已在欧盟、日本、澳大利亚和英国获得有效条件上市许可,在美国获得紧急使用授权(EUA)。吉利德于https//www.gilead.com/news-and-press/press-room/press-re...
|

|
美国政府开始招标储备关键原料药
2020.08.05
美国政府正在储备可用于在未来大流行或国家紧急情况下用于生产基本药品的原料药(API),以期为美国药物供应链增加一层保护。
美国储备库之前仅限于医疗机构需要用来应对诸如飓风、大流行或炭疽爆发的药品和医疗用品。现在生物医学高级研究与发展局(BARDA)正在征求在政府战略国家储备...
|