
|
ICH雅典会议召开:指南进展,新指南计划,以及MedDRA
2022.06.14
ICH于5月21日至25日首次以混合形式(线下与线上)在希腊雅典举行了会议。在会议中,审查了ICH所有31个工作组的活动状况,听取了MedDRA(Medical Dictionary for Regulatory Activities,ICH标准化医学术语词典)管理委员会的报告,并更新了近期与培训和交流有关的几项重要活动。
...
|
|
【识林工具】ICH M7(R2)拆解思维导图:“基毒”杂...
2022.05.28
药品中的所谓“基因毒性”杂质,蕴含着相当高的安全性风险,也就意味着相当高的审评和质控风险,本就令企业分析人员乃至工艺开发人员头痛不已,近年来,“亚硝胺”导致的召回层出不穷,更令业界谈“基毒”色变。
这类杂质研究的纲领性指南文件,非ICH《M7(R2):评估和控制药物中的DNA...
|

|
ICH Q3D(R2)正式版发布:部分 PDE,各论,皮肤与...
2022.05.16
5月9日,国际人用药品注册技术协调会(ICH)颁布了元素杂质指导原则修订版 Q3D(R2),是之前于2020年9月25日发布的 Q3D(R2)草案(Draft)的最终版本(Final),相比于草案,该版本的主要变化包括:
修正了附录2中金(Au)、银(Ag)和镍(Ni)的每日允许暴露量(Permitted/Permissibl...
|
|
EMA 发布制药业对 ICH Q9 (R1) 质量风险管理的...
2022.05.13
近日,欧洲药品管理局 (EMA) 发布了 ICH Q9 (R1) 质量风险管理评论概述。这份 pdf 文件长达41页,内容是来自制药行业各相关方对于 ICH Q9 (R1) 提出的反馈意见。这些意见多达数百条,部分来自 PDA、ISPE、ECA 等大型行业协会,当然也有阿斯利康、吉利德、武田等跨国药企...
|

|
【识林社区】优质问答集锦3
2022.04.30
以下是识林社区中的部分优质问答:
1.【研发】ICH M7一类杂质可摄入量计算:用动物实验的TD50推导出人类致癌剂量的背后逻辑是什么?
ICH M7中原文:根据致癌性数据库(CPDB数据库官方名称),环氧乙烷的TD50为21.3 mg/kg体重/天(大鼠)和63.7 mg/kg体重/天(小鼠)。在...
|

|
ICH发布《Q14分析方法开发》和《Q2分析方法验证》(R2...
2022.04.02
ICH刚刚发布Q14 Analytical Procedure Development 分析方法的开发,以及Q2修订版Q2(R2) Validation of Analytical Procedures 分析方法的验证,两份征求意见稿。尽管姗姗来迟,也是制药行业CMC领域翘首以盼。
Q2(R1) 现行版发布于2005年11月,十余年来一直是药品分...
|

|
ICH 考虑开辟途径吸收临床医生和患者代表意见
2022.02.23
ICH 正在寻求增加医务人员和患者群体参与其指南制定过程的方法,尤其是在涉及临床试验时。
ICH 去年 11 月在一次关于 E8(R1)《临床研究的一般考虑因素》指南的公开会议上讨论了一些不同寻常的内容,建议临床医生和患者代表应与监管机构和行业团体一样在 ICH 中占有一席之地。
自 ...
|

|
制药商对 ICH Q13 连续制造指南草案反馈意见,要求...
2021.12.23
一些行业协会要求 ICH Q13《原料药与制剂的连续制造》指南给出更多澄清,包括构成连续制造过程受控状态的内容、指南范围和批量大小的定义。其中一个制药商表示,指南过分强调不合格物料,这在连续制造中并不是一个重要问题。
ICH Q13 指南于 2021 年 7 月 27 日发布,描述了连...
|

|
ICH Q9 质量风险管理指南修订版发布
2021.12.20
ICH 于 2021 年 12 月 16 日发布了 Q9《质量风险管理》指南修订草案以公开征求反馈意见。ICH 预计将于 2022 年 9 月定稿,比之前宣布的 2022 年 6 月的定稿目标有所延迟。
指南草案重点关注五个主要领域的变化:质量风险管理(QRM)的主观性;供应链风险管理;正式程...
|

|
欧盟官员表示 ICH Q6B 生物制品检测方法和可接受标...
2021.12.07
瑞典医疗产品管理局疫苗和单克隆抗体(MAb)高级专家 Mats Welin 在 2021 年 11 月 30 日由国际制药工程协会(ISPE)主办的关于以患者为中心的质量标准网络研讨会上表示,ICH Q6B《质量标准:生物技术产品及生物制品的检验方法和接受标准》设定了新生物制品的可接受标准,需要修...
|

|
ICH 2021 年 11 月大会公布最新指南进展和下一步...
2021.11.27
ICH 大会于 11 月 17 日至 18 日通过网络召开,会议之前是 ICH 管理委员会和 MedDRA 管理委员会网络会议。
大会上 ICH 进一步扩大了会员和观察员。墨西哥 COFEPRIS 成为新的 ICH 成员,此外还有三个新的 ICH 观察员:埃及 EDA,印度尼西亚 FDA 以及乌克兰 SECMOH。目前...
|

|
ICH 正修订 E2D 上市后安全数据管理指南,协调处理...
2021.11.26
ICH 正在准备更新 E2D《上市后安全数据管理》指南,帮助公司处理来自越来越多来源的批准后安全数据。
ICH E2D(R1) 专家工作组报告员、AbbVie 卓越药物警戒副总裁 Vicki Edwards 在 10 月初 DIA 药物警戒受权人(QPPV)论坛上表示,正在考虑采取多种方法更新关于批准后安全数...
|

|
行业组织就 ICH Q12 实施细节向 FDA 提交反馈意...
2021.10.30
国际制药工程协会(ISPE)正在呼吁美国 FDA 对 ICH Q12 批准后变更指南进行多处修订。FDA 于今年 5 月发布 Q12 实施考量指南草案并公开征求意见。
ISPE 在其 10 月 8 日的反馈意见中提出,拟议报告类别应放在通用技术文件(CTD)的区域性信息部分,而不是模块 3 中。ISP...
|

|
ICH Q9 质量风险管理指南修订将推迟三个月,解决风...
2021.10.15
ICH Q9《质量风险管理》指南的修订由于新冠疫情已推迟了大约三个月,但修订过程仍在继续推进。
爱尔兰卫生产品监管局高级 GMP 检查员 Kevin O'Donnell 在 9 月 30 日的 PDA/FDA 联合监管会议上表示,这将是“非常有针对性的修订。我们不会修改指南的许多方面,这绝不是完...
|

|
ICH 发布 E8(R1) 临床研究的一般考虑指南
2021.10.12
ICH 于 10 月 6 日宣布,E8(R1)《临床研究的一般考虑因素》指南已达到第 4 阶段,正在等待各监管机构批准采纳。这份广受期待的指南通过采用质量源于设计的原则,使临床试验的设计、实施和报告现代化。指南结合了“实现符合预期目的的数据质量的当前概念。”
ICH 表示,“ICH E...
|

|
ICH 调研显示指南实施和采纳水平普遍较高
2021.09.22
根据 9 月 9 日公布的一项最新调研结果显示,ICH 的 55 份与质量、安全性和有效性相关的指南以及多学科指南中的大部分已被其 10 个非创始成员和观察员以及 30 家制药企业采纳。
该调研旨在监测监管机构和行业对 ICH 指南实施的充分性和水平,并补充 2019 年发布的关于 I...
|

|
业界要求 FDA 进一步澄清 ICH Q12 的既定条件、...
2021.08.10
美国 FDA 于今年 5 月发布《ICH Q12:FDA 监管产品的实施考量》指南草案向利益相关者征求反馈意见【FDA 发布 ICH Q12 实施考量指南,详述如何实施既定条件并提供示例 2021/05/16】,反馈截止日期为 7 月 19日,FDA 收到了包括来自制药行业贸易协会以及单独企业的https//www.regulat...
|
|
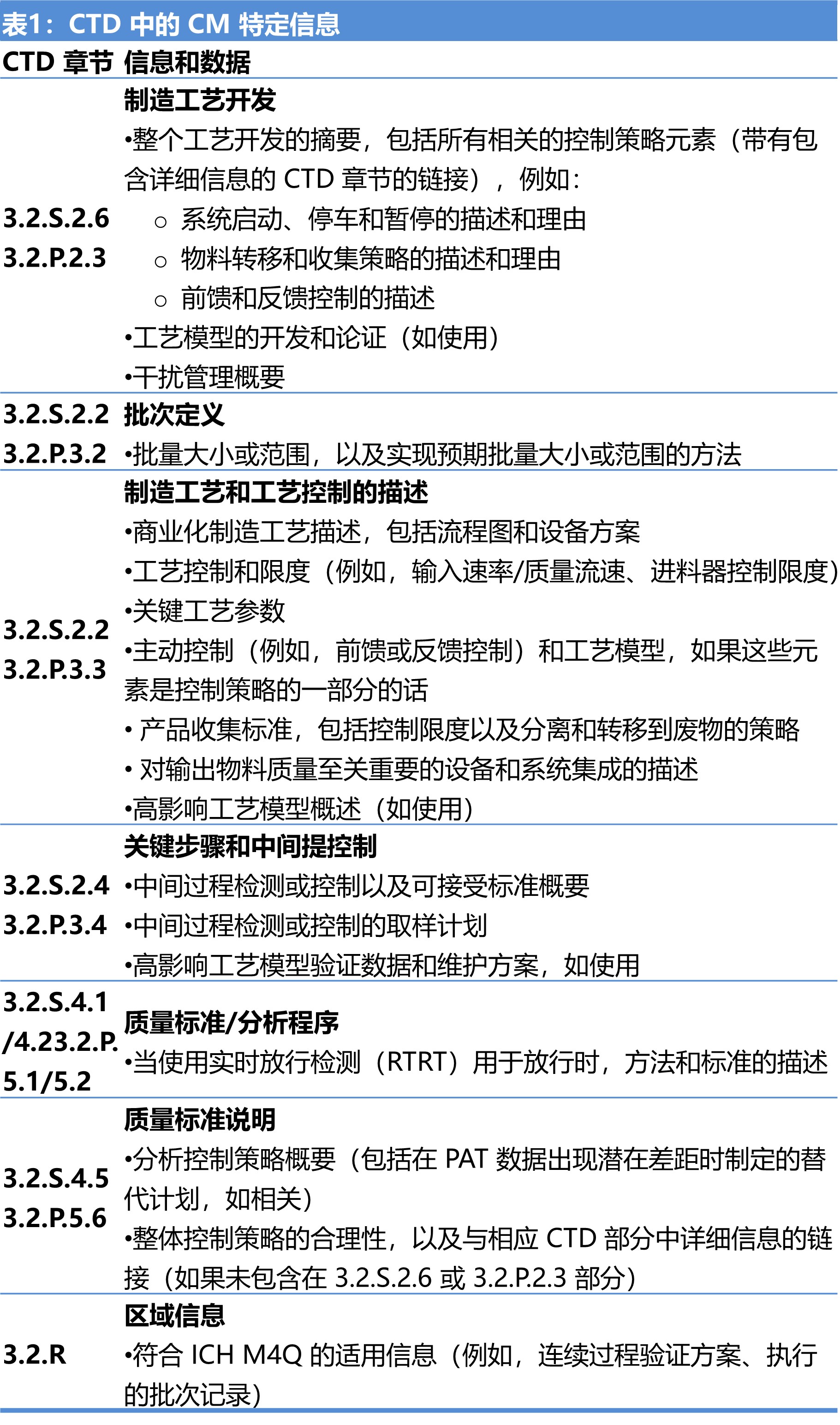
ICH Q13 连续制造指南正式发布
2021.07.29
ICH 于 7 月 27 日正式发布了广受期待的 Q13 《原料药与制剂的连续制造》指南,公开征询意见。指南“描述了连续制造(CM)的开发、实施、操作和生命周期管理的科学和监管考虑因素。”指南还“澄清了 CM 的概念,描述了科学方法,并提出了针对原料药和制剂连续制造的监管考量。”...
|

|
ICH Q13 连续制造指南即将发布
2021.07.17
ICH Q13 关于连续制造的指南预计将很快发布征询反馈意见。7 月 14 日,由加州分离科学学会(CASSS)主办的 CMC 战略论坛上,美国 FDA 药品质量办公室生物技术产品办公室审评员 Cyrus Agarabi 概述了 ICH Q13 指南的最新进展。Agarabi 是 FDA 连续制造团队的成员之一。
IC...
|
|
ICH 公布以患者为中心的药物开发思考性文件意见征询...
2021.06.28
ICH 以患者为中心的药物开发(PFDD)思考性文件于 2020 年 11 月获得 ICH 大会批准【ICH 将着手制定以患者为中心的药物开发指南 2020/12/12】,确定了纳入患者观点可提高药物开发的质量、相关性、安全性和有效性,并为监管决策提供信息的关键领域。思考性文件还提出了制定新 IC...
|