
|
【周末杂谈】疫情之后国际药品供应链面临的困境
2020.04.12
3月19日,识林报道美国国会议员提出“保护我们的药品供应链免受中国影响法案”【美国国会议员提出法案限制中国原料药进口 2020/03/21】。当然,不是所有提案最终都能成为法律,但值得注意的是,就在19日当天,总统签署完成立法的价值两万亿美元的“冠状病毒资助、救援和经济保障法”(CAR...
|
|
REMAP-CAP:应对大流行的全球临床试验
2020.04.11
前两天我们介绍了横跨整个英国的最大新冠临床试验 RECOVERY 【英国启动最大新冠临床试验,两周入组近千人】,文中提到 RECOVERY 是英国同时开展的三项“国家优先临床试验之一”,今天我们来看看这三个优先临床试验的另外一个:REMAP-CAP。
对于新型冠状病毒疾病(COVID-19)患者...
|

|
FDA 检查冻结合规判定或加速,疫情下企业纠正措施难...
2020.04.10
新型冠状病毒疾病(COVID-19)大流行,可能会导致美国 FDA 加快对之前已检查设施的合规行动,因为检查员不再出现场,他们或有更多时间来完成对以前检查的设施评估。但,检查冻结可能会使制药商在拿到不利检查结果后试图使工厂重新达到合规状态更加困难,并且可能会延迟 FDA 对检查设...
|
|
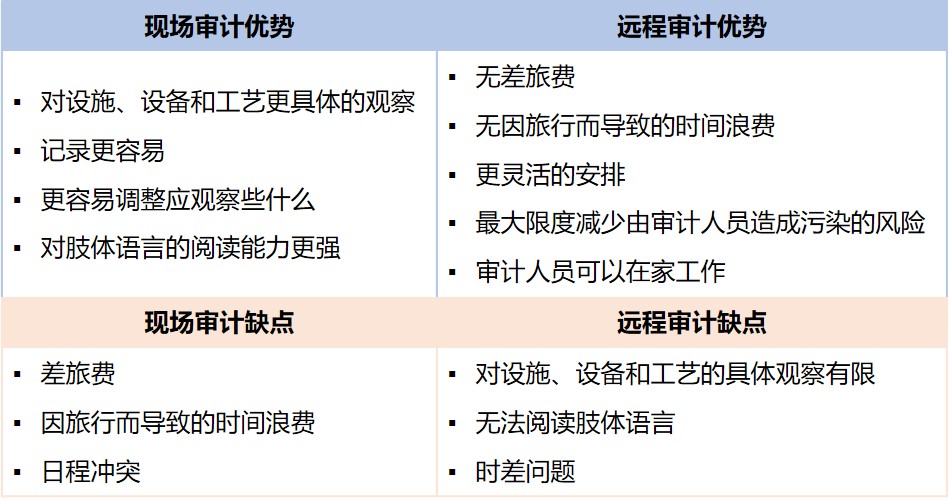
疫情下如何开展远程 GMP 合规审计
2020.04.10
新型冠状病毒疫情(COVID-19)大流行的笼罩下,每个受监管的制药企业也都不可避免地受到影响,同时也暴露了全球供应链的脆弱性以及对应急计划缺乏重视。本文重点介绍 GMP 合规的远程审计,主要关注执行远程内部和外部审计所面临的挑战、优势和最佳实践。
审计通常用于多方面的原因,...
|

|
医院和药房检测药品质量是可持续的方法吗?
2020.04.09
前段时间我们曾介绍过美国医疗机构对于公开质量评级持普遍支持态度,远比药业积极得多。但医院对于当前市场上药品的质量状态非常担心,虽然 FDA 一再保证仿制药的质量与品牌药一样。【公开质量评级,医院比药业更支持 2020/02/29】。医疗机构对处方的仿制药无效、仿制药被召回或售罄...
|

|
英国启动最大新冠临床试验,两周入组近千人
2020.04.09
一项横跨整个英国的针对新型冠状病毒疾病(COVID-19)治疗药的随机临床研究可以帮助巩固英国作为未来临床试验场地的声誉。这项研究被视为英国监管机构对潜在 COVID-19 治疗药物的“果断行动”的一部分,试验已创下许多记录,任何 18 岁以上因 COVID-19 住院的患者均获邀参加。
该...
|

|
FDA 放宽有关罕见病基因治疗药物安慰剂对照试验的限...
2020.04.08
今年1月底,FDA公布了《罕见病基因治疗》(Human Gene Therapy for Rare Diseases)的定稿指南。在指南中,FDA拒绝了利益相关者关于取消安慰剂对照试验的要求,但是通过增加 “当可行时”的前置描述,使这一建议在实际操作中的灵活性有所提高。同时,考虑到业界对2018年指南草案中关...
|

|
新冠疫情下的药品专利:自愿知识产权池还是强制许可?
2020.04.08
随着新型冠状病毒疫情(COVID-19)大流行,各个国家都在竞相研制应对疫情的治疗药物和疫苗,但是对于贫穷国家或药物研发能力较弱的国家来说,如何才能让自己的国民尽快用上能负担得起的药物?WHO 总干事于 4 月 6 日发表讲话,表示支持建立关于 COVID-19 产品的自愿知识产权池,...
|

|
个体化基因治疗的开发与监管挑战,NIH 公共平台载体...
2020.04.07
个体化疗法(Individualized Therapeutics)是指通过设计产品解决潜在病症的特定作用机制而专门开发的针对一个或极少数患者的治疗方式。波士顿儿童医院的研究人员已经将这种定制疗法工作推动到了最前沿,他们为一名患有罕见 Batten 遗传病的儿童患者,使用针对患者定制的反义寡核苷酸方法...
|
|
专家提醒对 COVID-19 疫苗的紧急使用授权应格外谨...
2020.04.07
当前针对新型冠状病毒疫情(COVID-19)疫苗的研发各机构都在紧锣密鼓的进行中,至少三例已经进入了 1 期临床,包括康希诺生物的 Ad5-nCoV,Moderna 公司的 mRNA-1273,以及牛津大学的 ChAdOx1。随着疫情日益严重,人们都希望有效的疫苗能够尽快上市,但三名前 FDA 部门负责人和...
|

|
药企应警惕实验室因临床时间压力而放行不可靠数据
2020.04.06
当前,为应对全球新型冠状病毒疫情(COVID-19)大流行,很多制药公司和研发机构都在紧锣密鼓的开展旨在证明药物对 COVID-19 有效性的临床试验,但此时对临床过程中的实验室数据更不能掉以轻心,数据的可靠性将直接影响临床试验进展和决策,进而影响患者治疗和疫情控制。英国监管机构 M...
|

|
【更新提示】识林一周回顾(20200330-0405)
2020.04.06
上周国内的重磅政策当属新修订《药品注册管理办法》和《药品生产监督管理办法》的颁布,另随办法配套发布了相关解读。ICH 发布残留溶剂指南,拟限定3种残留溶剂的指南。各药监机构继续出台大量政策指南应对新型冠状病毒疫情。FDA 上周要求所有雷尼替丁产品撤市,欧盟表示正在讨论,将...
|

|
周末杂谈开启《质量对话》专栏
2020.04.05
【编者按】从这周起,在周末杂谈项下,将开启不定期的《质量对话》专栏,由刺槐主持,从专业和理性的角度,探讨医药产品质量问题,促进公众对质量问题的认知和交流。欢迎大家关注,并参与讨论。
编辑:最近有媒体报道,有些国家抱怨我国支援的新冠病毒检测试剂盒有质量问题,你怎么看...
|

|
如何说服公司投资过程分析技术(PAT)
2020.04.04
多年来,制药业高管普遍拒绝在过程分析技术(PAT)上花钱,尽管这些技术可以减少运行时间、控制成本并确保更稳健的制造过程。最近在 IFPAC(国际过程分析与控制论坛)年会“为 PAT 打造商业案例”会议环节,辉瑞、Vertex 制药和 Biogen 公司介绍了他们在说服管理层投资过程分析技术...
|

|
药房可自行配制羟氯喹?风险太大
2020.04.03
美国 FDA 于 3 月 25 日宣布将羟氯喹列入类别 1 配药物质供配药房使用,其原因是由于该药预期可能用于新型冠状病毒疫情(COVID-19)治疗而导致的潜在药物短缺。而专业人士则对此举表示质疑和担忧。
FDA 对于用于配药的待包装原料药规定了三个类别,其中类别 1 是指这些原料药符...
|
|
FDA 关于雷尼替丁中 NDMA 杂质情况的问答更新
2020.04.03
昨日的资讯中介绍了美国 FDA 要求所有雷尼替丁制药商将产品撤市,今天我们来看看 FDA 在更新的问答文件中对于这一决定的说明。
关于雷尼替丁产品中 NDMA 杂质的重要信息
美国 FDA 已经要求制药商从市场上撤回所有雷尼替丁。这意味着雷尼替丁产品在美国将无法通过新的或现有处...
|

|
FDA 药品中心主任谈疫情下审批和检查工作,新冠治疗...
2020.04.02
美国 FDA 药品审评与研究中心主任 Janet Woodcock 医学博士最近在家远程接受采访,讨论了在新型冠状病毒疫情(COVID-19)影响下的审评截止日期、批准前检查以及社交疏离时代如何召开咨询委员会会议等问题。
Woodcock 表示,尽管包括抗病毒、重症监护和肺部疾病在内的应对应对疫...
|

|
FDA 要求所有雷尼替丁产品撤市,亚硝胺杂质可在正常...
2020.04.02
内容提要:
- 在正常贮存条件下,雷尼替丁中 NDMA 含量也会增加
- 较高温度(包括产品在分销和由消费者处置的过程中产品可能暴露的温度)下贮存的样品 NDMA 显著增加
- 雷尼替丁产品越老,或者自生产出厂以来的时间越长,NDMA 的含量就越高
- FDA 向所有雷尼...
|

|
美国研究所发布路线图,提供疫情应对详解
2020.04.01
美国企业公共政策研究所(American Enterprise Institute for Public Policy Research,简称 AEI)于 3 月 29 日发布https//www.aei.org/research-products/report/national-coronavirus-response-a-road-map-to-reopening/ 《国家新冠疫情应对:重新开放路线...
|

|
诺华基因治疗药数据操纵问题悄然平息
2020.04.01
诺华子公司 AveXis 因操纵用于 Zolgensma 基因治疗药物批准的数据而引发的数据完整性危机似乎已经悄然结束,美国 FDA 指示 AveXis 公司纠正问题,未施加任何惩罚。
问题的根源是诺华在向 FDA 披露 Zolgensma 的数据操纵方面存在延迟,诺华在 2019 年 3 月 Zolgensma ...
|