|
FDA 阿尔茨海默药 Aduhelm 风险获益综合评价重点内...
2021.06.24
美国 FDA 于北京时间 6 月 23 日早在其网站上公布了三份详细的阿尔茨海默新药 Aduhelm(aducanumab)的审评备忘录,其中神经科学办公室解释批准决定的 69 页的摘要备忘录详述了 FDA 对于争议最大的几点问题的讨论和结论,包括:提前终止且不一致的两个三期研究;淀粉样斑块蛋...
|

|
阿尔茨海默新药批准影响持续升温,参议员要求 FDA ...
2021.06.21
美国 FDA 加速批准渤健(Biogen)阿尔茨海默病新药 Aduhelm(aducanumab)带来的影响仍在发酵,一位关键民主党议员在 6 月 18 日给拜登总统的信中呼吁罢免 FDA 最高决策者。
西弗吉尼亚州民主党参议员 Joe Manchin 要求拜登总统罢免 FDA 代理局长 Janet Woodcock,并迅...
|
|
阿尔茨海默药批准后续:倡导者不满 FDA 审批肌萎缩...
2021.06.19
美国 FDA 加速批准渤健(Biogen)阿尔茨海默病新药 Aduhelm 引发的争议已波及到该疾病领域之外,肌萎缩侧索硬化症(ALS)倡导者对 FDA 在 ALS 领域的缓慢行动感到不满。
FDA 在加速审批路径下批准了 Aduhelm,加速审批允许根据替代终点批准药物。在 Aduhelm 之前,这一路径...
|

|
公益组织敦促对阿尔茨海默批准问责,要求FDA代理局长...
2021.06.18
在美国 FDA 加速批准备受争议的渤健(Biogen)阿尔茨海默新药之后,消费者倡导组织 — 公共公民(Public Citizen)于 6 月 16 日致信美国卫生部(HHS)部长 Xavier Becerra,呼吁其立即要求对 Aduhelm 的决定负有最大责任的 FDA 的三名高级官员辞职或撤职,包括 FDA 代理局长 Jan...
|

|
【周末杂谈】FDA 批准阿尔茨海默药后的感想
2021.06.13
不明有效性的药未必无疗效,听上去邪乎,但合法合理
FDA药品中心主任就批准阿尔茨海默症新药发表的说明中有这样一句话“归根结底,我们遵循了在数据不明确的情况下做出监管决策的一贯行动方针”。用白话说,就是认为不明有效性的药有疗效。
听上去邪乎,但合法合理。
有效性(effic...
|

|
阿尔茨海默新药批准:三名专家组成员辞任,FDA代理局...
2021.06.12
美国 FDA 于 6 月 7 日宣布加速批准备受争议的渤健(Biogen)阿尔茨海默新药 Aduhelm 之后【FDA 加速批准渤健阿尔茨海默症新药,赞扬批评声缠结】,到目前为止已有三名专家顾问委员会成员辞去委员会职务。
美国布莱根妇女医院监管项目主任、哈佛生物伦理学家,自 2015 年以来一...
|
|
FDA 专家组成员之一因阿尔茨海默新药获批而辞任
2021.06.10
美国 FDA 在 6 月 7 日宣布了对备受争议的渤健(Biogen)阿尔茨海默病新药 Aduhelm 的批准之后,曾投票反对该药批准的 FDA 专家顾问委员会的一名成员已经辞去委员会职务。
FDA 外周和中枢神经系统药物专家小组成员,华盛顿大学神经学家 Joel Perlmutter 表示,他已于周一退...
|
|
FDA 加速批准渤健阿尔茨海默症新药,赞扬批评声缠结
2021.06.08
美国 FDA 于北京时间 6 月 7 日晚上 11 点多批准了备受争议的渤健(Biogen)的阿尔茨海默治疗药 Aduhelm(aducanumab),这是近二十年来 FDA 批准的首个治疗阿尔茨海默症的新药,具有里程碑意义。但对于 FDA 的此项批准决定公众、业界、患者群体和科学界也呈现出两极分化的反...
|
|
FDA 关于阿尔茨海默症新药批准决定的说明
2021.06.08
美国 FDA 于 6 月 7 日加速批准了渤健(Biogen)的阿尔茨海默症新药 Aduhelm(aducanumab),在宣布加速批准的同时,FDA 药品审评与研究中心(CDER)主任 Patrizia Cavazzoni 发布了一份对批准决定的说明。
说明首先承认了 Aduhelm 所受到的广泛关注和引发的争议,以及争议...
|

|
【周末杂谈】写在FDA阿尔茨海默药决定前夜的话
2021.06.06
无论FDA如何决定都会招致不满,但长远看却是营造了满盘皆赢的局面
明天,6月7日,是美国FDA决定是否批准渤健(Biogen)公司阿尔茨海默药Aducanumab的截止日期。这应是FDA史上最难产的决定之一了。有关此事的跟踪报道,请参见识林资讯:
三名专家小组成员公开发文呼吁 FDA 拒绝渤健阿...
|

|
渤健阿尔茨海默药 FDA 判决日期临近,资本市场发出...
2021.06.03
美国 FDA 将于 6 月 7 日就渤健(Biogen)的 aducanumab 做出决定。如果获得批准,将成为二十多年来第一个上市的阿尔茨海默症治疗方法。【FDA 推迟对渤健阿尔茨海默药的审批决定 2021/01/30】
而如果被拒,可能会对这家总部位于马萨诸塞州的公司产生深远影响。根据 Insightia 发布的...
|
|
ICER 公布渤健阿尔茨海默治疗药成本效益定价,远低于...
2021.05.11
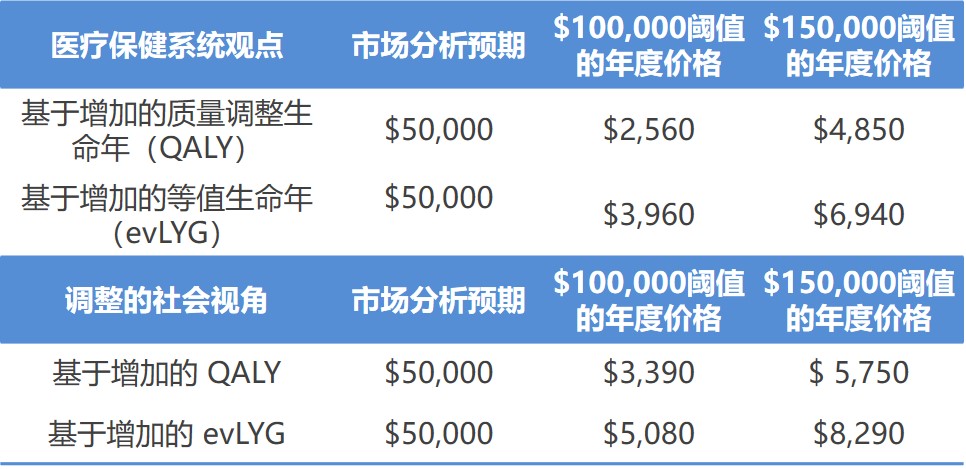
美国临床与经济评价研究所(ICER)在 5 月 5 日发布的一份草案报告中表示,渤健(Biogen)备受瞩目的阿尔茨海默症治疗药 aducanumab,由于获益证据“不足”,该药的成本应低至每年 2500 美元才被认为具有成本效益。
即使采用较高的成本效益阈值,ICER 的估计价格为 8,290 美...
|

|
FDA 新药审批收紧?Nuplazid 扩大痴呆及阿尔茨海默...
2021.04.06
Acadia 制药公司于 4 月 5 日表示,美国 FDA 拒绝了其对抗精神病药 Nuplazid(酒石酸哌马色林)寻求治疗广泛痴呆症相关的精神病(DRP)患者(包括阿尔茨海默症和其它疾病)的幻觉和妄想的补充新药申请(sNDA)。FDA 的拒绝理由是“在某些痴呆亚组中缺乏统计学意义”并且“对某些...
|

|
三名专家小组成员公开发文呼吁 FDA 拒绝渤健阿尔茨...
2021.04.02
美国 FDA 的专家会制度通常是 FDA 召集药品或疫苗咨询委员会,10 余位外部专家提出他们的看法并就 FDA 设定的投票问题投票,然后 FDA 可以选择听取或不听取专家会的意见。【周末杂谈:从FDA专家会,想我国药业发展】但渤健(Biogen)阿尔茨海默药 aducanumab 的专家会和审评过...
|
|
新型阿尔茨海默症恒河猴模型或可加快治疗药研究
2021.03.19
根据 3 月 18 日发表在《阿尔茨海默症和痴呆症》杂志上的一篇最新论文,研究人员创建了一种新的模型用于研究恒河猴中阿尔茨海默症的治疗方法,可能会加快可产生显著效果的人用治疗药的开发速度。论文题为“阿尔茨海默症发病机理的基于 tau 的新型恒河猴模型”1。
虽然业界对阿尔...
|

|
FDA 回复对阿尔茨海默药审评程序的批评,拒绝在申报...
2021.02.18
美国 FDA 长期以来在可批准的申请方面一直采取协作方式与制药商合作,以将新药推向市场。但当一个药充满争议时,监管者和企业之间的这种关系就容易受到指责。
12 月,消费者倡导组织公共公民(Public Citizen)就 FDA 对 Biogen(渤健)有争议的阿尔茨海默药 aducanumab 上市...
|

|
FDA 推迟对渤健阿尔茨海默药的审批决定
2021.01.30
根据渤健(Biogen) 1 月 29 日的https//investors.biogen.com/news-releases/news-release-details/biogen-and-eisai-announce-fdas-3-month-extension-review-period 消息,美国 FDA 推迟了对其备受关注的阿尔茨海默症治疗药 aducanumab 的批准决定,要求提...
|

|
【周末杂谈】如此鼓励创新?
2021.01.17
阿尔茨海默病症是如此倍受关注,引出了各种新做法和说法
1月11日,在全球影响大的JP Morgan医疗健康会上爆出重大新闻,美国礼来公司宣告其治疗阿尔兹海默病症的单抗药品Donanemab在临床试验中显示了明确的疗效。用药18个月后,早期阿尔兹海默病症患者记忆和自理能力的衰退速度降低了32...
|

|
公益组织要求调查 FDA 阿尔茨海默药审评程序,暂停...
2020.12.10
消费者倡导组织公共公民(Public Citizen)要求美国卫生部(HHS)的总监察长办公室(Office of Inspector General)调查 FDA 与 Biogen(渤健)在准备其有争议的阿尔茨海默症药物的监管上市申请方面进行的“不适当合作”。
公共公民组织在批评 FDA 方面从来毫不手软,而 12 ...
|

|
阿尔茨海默药被 FDA 专家会彻底否决
2020.11.07
编者按: 在半小时前刚刚结束、长达5小时的 FDA 专家委员会上,11 位专家对 Biogen 申报的、治疗阿尔茨海默的单抗新药,提出了尖锐的质疑,矛头直指 FDA 的操守,结果惨不忍睹。
link=13px 【FDA】阿尔茨海默药专家会 2020.11.06
截至发稿的半小时前,美国 FDA ...
|