
|
【更新提示】识林一周回顾(20191229-20200105)
2020.01.06
【NMPA】国家药监局关于发布预防用疫苗临床试验不良事件分级标准指导原则的通告(12.31)
指导原则提供的疫苗临床试验不良事件的分级指标包括两部分,第一部分为临床观察指标,包括接种部位(局部)不良事件、生命体征和非接种部位(全身)不良事件;第二部分为实验室检测指标(包括血...
|
|
FDA 态度大转变,发布 App 拥抱标签外使用信息
2020.01.06
美国FDA 对药品监管的核心是对标签的监管,标签外使用是医疗上的一种惯例操作,但是 FDA 一直以来并不鼓励,并且对于标签外使用推销的监管尤为严格。现在 FDA 和 NIH 合作开发了一个网站和 app,鼓励医务人员和其他人在上面提交标签外使用案例并进行讨论。
美国 FDA 和美国国立...
|

|
2019年 FDA新药审批总结
2020.01.06
Innovation in New Drug Approvals of 2019 Advances Patient Care Across a Broad Range of Diseases
In 2019, the FDA approved a wide variety of new drug therapies to help patients in need.
2019年创新型新药批准推动了一系列疾病的患者...
|
|
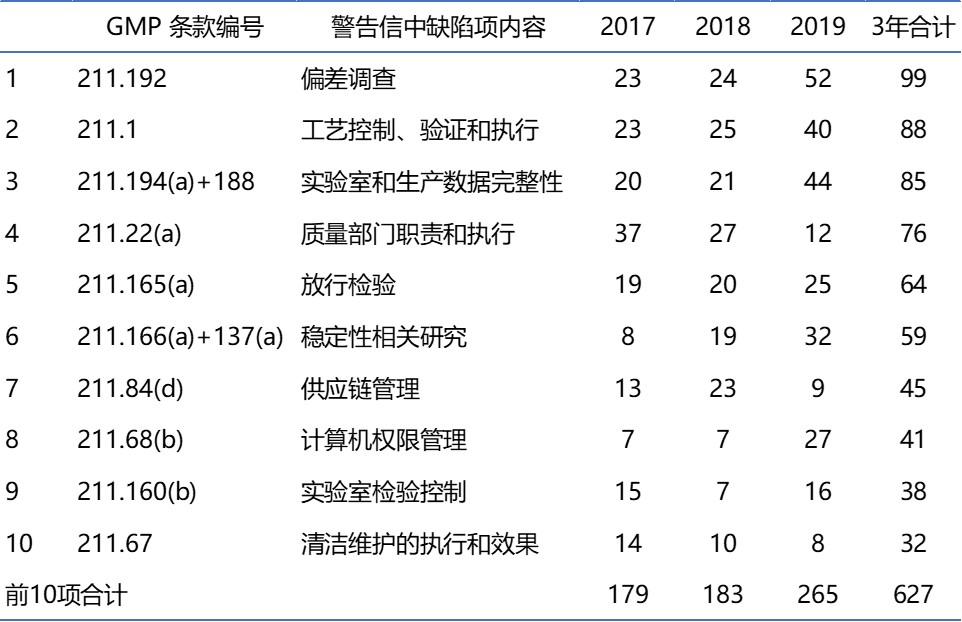
【周末杂谈】从FDA警告信看GMP“软件”部分的重要性
2020.01.05
上周的周末杂谈“判断是否低于成本竞标,不容易”,谈到与药品生产相关的“硬件”成本,包括:设施、设备、物料、能耗、人工及管理费用方便计算;“软件”成本,例如:处方工艺研发、GMP管理和合规运行的费用难于计算。今天的杂谈想说这个“软件”部分,尽管成本难以计算,其重要性不可低...
|

|
FDA 发布指南讨论组合产品申办人与 FDA 沟通的最佳...
2020.01.04
美国 FDA 于 12 月 23 日发布《请求 FDA 对组合产品反馈》的指南草案,讨论了组合产品申办人如何从 FDA 获得有关科学和监管问题的反馈,并介绍了当 FDA 与申办人进行互动时的最佳实践。指南指出,这些互动可以通过基于申请的会议机制(通常是最有效的沟通方法),或者通过组合产品...
|

|
药业的 2010 年代:加速、创新和充满争议的十年
2020.01.03
回顾二十一世纪的第一个十年,我们应如何评判这十年间的制药业?十年的时间跨度不可避免的充斥着成功与失败、飞跃与绝境、协调与冲突,下面我们看看总部在伦敦的全球大型出版商 Informa 的撰稿人 Andrew McConaghie 对这十年制药行业的总结分析。
癌症、丙型肝炎、罕见疾病方面的...
|
|
漏报到 FDA 的药物副作用数量可能被严重低估
2020.01.03
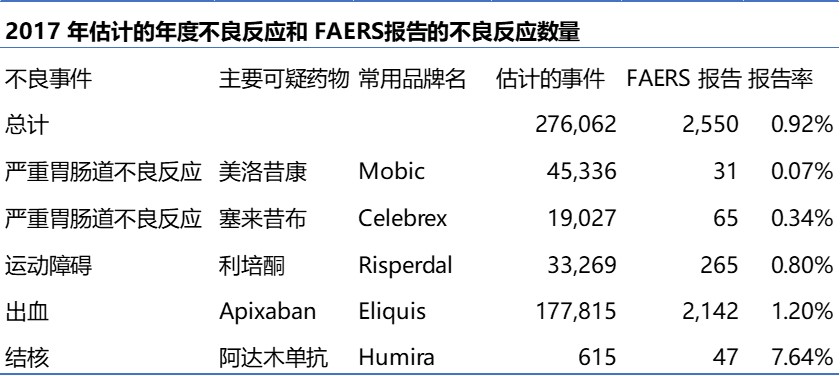
众所周知,很多药物副作用并没有报告到药监局,但具体漏报程度如何,一份新的报告表明问题远超想象。这一问题在非营利组织安全药物实践研究所(Institute for Safe Medicines Practices,ISMP)发布的 QuarterWatch Report 中提出。
报告审查了有关五种广泛使用的药物(两种不同...
|

|
全球政策和战略办公室—欧洲办公室
2020.01.02
Europe Office
Established in May 2009, the Europe Office serves as the lead for the FDA’s on- site presence in Europe. It covers the European Union and individual countries that are not EU members, such as Switzerland and Norway and facilitate...
|

|
FDA警告用于治疗癫痫的gabapentin和pregabalin可能引...
2020.01.02
FDA warns about serious breathing problems with seizure and nerve pain medicines gabapentin (Neurontin, Gralise, Horizant) and pregabalin (Lyrica, Lyrica CR)
https//www.fda.gov/media/133881/download Listen
Welcome to the FDA Drug Safety Podcast f...
|

|
国际检查互认不断拓展,菲律宾加入东盟互认协议
2020.01.02
国际检查合作和互认已是大势所趋,下一步的工作是在深度和广度上的进一步扩展。过去识林多次报道了美国、欧盟、加拿大、英国、澳大利亚、日本之间的合作和互认,今天识林带你来看看我们的邻居 — 东盟,在检查互认方面的工作。
在经过一长段时间包括文件、现场、过程中检查评估的审...
|

|
FDA 副局长谈美欧药品检查互认协议的影响
2020.01.02
美国 FDA 全球政策与战略副局长 Mark Abdoo 最近在 FDA 《全球视角》栏目中谈到了自美国/欧盟互认协议(MRA)实施以来一些影响性数据,并承认 MRA 还需要收集更多数据,纳入更多衡量指标,从而帮助 FDA 分配资源并扩展 MRA 的范围和广度。
当我们首次开始与欧盟讨论互...
|

|
识林年度回顾:2019 热点资讯
2019.12.31
2019 年即将过去,在这最后一天,我们来盘点一下过去一年中读者们关注的热点话题。
1. 质量仍是重中之重
质量一直是制药行业的关注重点,关于药品质量、质量保障、质量文化的思考和研究从未停止过。以下关于质量前沿讨论的系列报道中的第一篇成为识林 2019 年度最热门资讯。
...
|

|
2020 年数字医疗公司需要考虑的三大问题
2019.12.31
从数字上看,2019 年又是数字医疗公司的一个大年。随着公司大量敛钱投资开发新型可穿戴设备、个性化数字服务和机器学习工具以改善疾病的治疗,该领域的总投资预计将达到创纪录的 84 亿美元。几家公司也已进入公开市场,苹果、亚马逊、谷歌和微软等科技巨头加大了对医疗方面的投资,并招...
|

|
吸入器与吸入制剂的当前挑战与开发趋势
2019.12.30
从历史上看,吸入药物递送仅限于呼吸系统疾病的治疗和管理,例如哮喘或慢性阻塞性肺病。然而,这种递送方法已经扩展为许多系统疾病的替代治疗方案,包括内分泌和神经系统疾病,这些疾病可以受益于吸入性递药方案提供的频繁脉冲式给药。
与口服或注射给药相比,吸入性替代方案更好地模拟...
|

|
通过探测 DNA 损伤快速检测化学物质潜在致癌性的新...
2019.12.30
检测细胞中的 DNA 损伤可以预测是否会发展为癌症,但过去对这种损伤的测试灵敏度有限。研究人员现在提出了一种新的筛选方法,可以使这种检测更快、更便捷、更准确。美国国家毒理学计划,一个识别潜在有害物质的政府研究机构目前正在努力采用这一新方法来评估新化合物。
研究的通...
|

|
US-EU 互认协议药品附录的影响力测量
2019.12.30
Measuring the Impact of the Pharmaceutical Annex to the U.S./EU Mutual Recognition Agreement
December 6, 2019
By Mark Abdoo
When we first began discussing the prospects of a mutual recognition agreement with the European Union, in which EU mem...
|

|
【周末杂谈】判断是否低于成本竞标,不容易
2019.12.29
为保证百姓用药安全,不因药品降价而导致药品质量下降、触发安全事件,政府要求企业不得低于成本竞标,并鼓励举报,详见《国家基本医疗卫生与健康促进法》第六十二条和第九十七条。该法于12月28日获得表决通过。低于成本竞标的确容易有质量打折扣的嫌疑,但计算成本并非易事。
其实,低...
|

|
【更新提示】识林一周回顾(20191222-1228)
2019.12.29
【全国人大】中华人民共和国基本医疗卫生与健康促进法 定稿(12.28)
《中华人民共和国基本医疗卫生与健康促进法》12月28日由十三届全国人大常委会第十五次会议表决通过,将于2020年6月1日实施。该法分为总则、基本医疗卫生服务、医疗卫生机构、医疗卫生人员、药品供应保障、健康...
|

|
患者可随身携带的疫苗接种记录:皮下量子点染料图形
2019.12.28
每年缺乏疫苗接种会导致大约 150 万例可预防的死亡,而这些死亡主要存在于发展中国家。在这些国家推广疫苗接种面临的一个困境是:用于存储病历的基础设施很少,因此没有简单的方法来确定哪些人需要接种哪些疫苗。
研究人员现开发出一种新的方式来记录患者的疫苗接种史:将数据存储为...
|

|
器械还是药品?法院限制了 FDA 的自由裁量权
2019.12.27
药品和器械之间的一个关键区别是:药品和器械药遵守不同的监管框架,并且药品的监管繁琐而昂贵。一款仿制药首年的使用者费总计为 30 万美元,而器械仅为 7600 美元左右,而根据 505(b) 途径批准的药品的使用者费更高,2019 财年总计约 250 万美元。另外,药品还需遵守更严格的...
|