
|
FDA药品登记和场地注册最终规定内容摘选
2016.09.07
8月31日美国FDA发布对药品场地注册和药品登记法规修订的https//www.federalregister.gov/articles/2016/08/31/2016-20471/requirements-for-foreign-and-domestic-establishment-registration-and-listing-for-human-drugs?utm_campaign=pi+subscription+mailing+list&utm_medi...
|
|
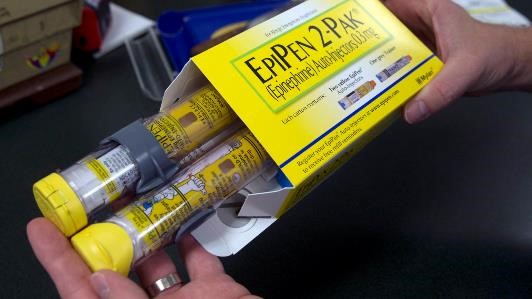
EpiPen价格飞涨III:反垄断违规调查请求铺天盖地
2016.09.06
【编者按】在美国社会、媒体和国会对Mylan公司的肾上腺素自助注射剂EpiPen价格飙升的讨论热烈展开时,STAT于8月25日发布的一篇https//www.statnews.com/2016/08/25/mylan-antitrust-epipen-schools 独家报道提起了人们对于Mylan公司涉嫌反垄断违规关注,继而参众两院议员陆...
|

|
GDUFA II期谈判完成,关键条款一瞥
2016.09.05
在FDA和工业界解决了关于收费方案的遗留问题后,仿制药使用者付费计划重新授权谈判已经完成。除了ANDA审评过程的进一步简化和沟通增强,一些申办人应该还可以看到费用减免,这是在谈判开始工业界要求的主要问题之一。
根据8月31日发布的会议纪要显示,最终协议于8月24日的一个15分钟的...
|

|
FDA宣布对阿片类和苯二氮卓类产品添加黑框警告
2016.09.04
8月31日FDA发布了一份安全警示公告,由于对潜在致命相互作用和严重不良反应的持续担心,在所有阿片类和苯二氮卓类产品上添加黑框警告。警告指出,“FDA审查发现,越来越多的阿片类药品和苯二氮卓类产品或其它抑制中枢神经系统(CNS)药品的组合使用导致严重副作用,包括呼吸减缓或困难和死...
|

|
FDA与工业界定于11月正式讨论标签外使用交流问题
2016.09.03
美国FDA于8月31日宣布将于11月9日-10日安排为期两天的公开听证会,全面审查关于企业已获批药品和医疗器械的未批准使用的标签外交流的法规和政策。https//www.federalregister.gov/articles/2016/09/01/2016-21062/manufacturer-communications-regarding-unapproved-uses-of-approve...
|
|
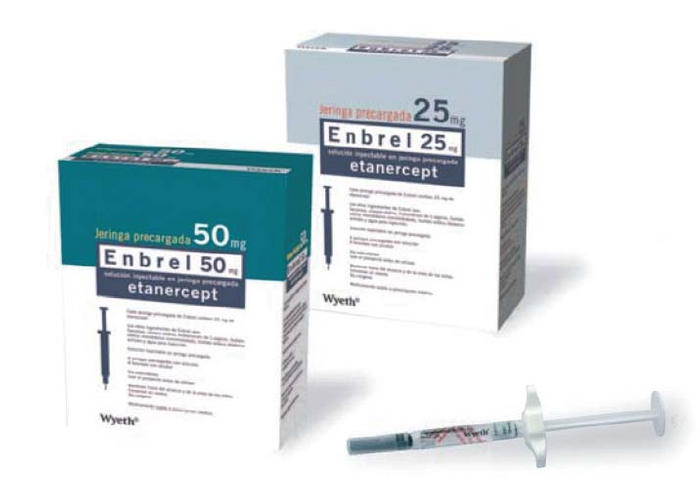
依那西普生物类似药获FDA批准
2016.09.02
美国FDA于8月30日批准了Sandoz公司对Amgen的Enbrel(依那西普)的生物类似药 — Erelzi(etanercept-szzs)。这一批准毫无悬念,Erelzi于7月13日在FDA关节炎咨询委员会专家会审中获得一致投票支持。【识林资讯 - 依那西普生物类似药获专家会审一致通过】
Erelzi的获批适应症包括参照产...
|

|
FDA发布最终规定修订场地注册和药品登记相关法规
2016.09.01
8月31日美国FDA在联邦公报(FR)通告中发布对药品场地注册和药品登记的法规修订,修订后的https//www.federalregister.gov/articles/2016/08/31/2016-20471/requirements-for-foreign-and-domestic-establishment-registration-and-listing-for-human-drugs?utm_campaign=pi+subs...
|

|
7月仿制药计划行动报告更新
2016.08.31
虽然在更新数据方面没有太多新的数据或趋势,但很显然美国FDA仿制药办公室(OGD)正在发布更多完全回应函(CRL)。OGD 7月份发布169封CRL,成为2016财年次高的月份(4月份最高190封)。这些数字也比过去几年显著更高。
Activities Report of the Generic Drug Program (FY 201...
|

|
【更新提示】药政信息摘要2016.08
2016.08.30
总局办公厅关于暂停进口和销售意大利LaboratorioFarmaceutico C.T.S.R.L.公司的注射用还原型谷胱甘肽钠的通知(08.30)
总局办公厅关于加强食品药品检验检测能力验证工作的通知(08.25)
CFDA征求意见稿 - 关于药物临床试验数据核查有关问题处理意见的公告(08.2...
|
|
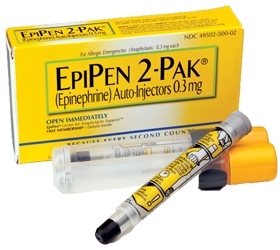
EpiPen价格飞涨II:Mylan连出虚招,国会要求调查
2016.08.30
美参众两院要求调查Mylan公司
众议院监督和政府改革委员会已展开对制药商Mylan公司的调查,由于救命药EpiPen自助注射剂价格暴涨,这家公司正面临着越来越严厉的审查。
本周一(8月29日),该委员会主席,来自犹他州的共和党籍众议员Jason Chaffetz与来自马里兰州的民主党籍资深众议员Eli...
|
|
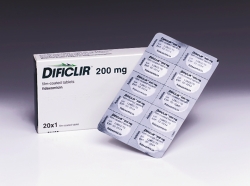
FDA发布非达霉素片剂BE指南并回应原研商请愿
2016.08.29
美国FDA于2011年5月批准Cubist制药公司的Dificid(非达霉素)200mg片剂,如万古霉素一样,用于治疗艰难梭菌相关的腹泻。两种药物均全身吸收差,治疗消化道和肠道局部病症。但是,万古霉素在生理学相关的溶出介质范围内比非达霉素更可溶。非达霉素的原研商Cubist于2015年5月7日提交了一份...
|

|
EpiPen价格飞涨,Mylan、国会、FDA、保险公司“功不可...
2016.08.28
【编者按】EpiPen是上周美国从社会、国会到企业的头条新闻和讨论内容。药品价格问题从去年底的Turing制药前CEO Shkreli事件后,越来越引起社会公愤,也让政客和药商越来越难以回避。总统候选人Hillary Clinton向来对药业态度严厉。这对药业未来的走势可能会产生影响,例如,上周药业的股...
|

|
工业界对FDA咀嚼片指南草案的评议摘选
2016.08.26
FDA于6月16日发布《咀嚼片的质量属性考量要点》指南草案,向公众征询意见,评议期截止于8月16日。通过该指南草案,FDA希望“已获批咀嚼片和非上市申请咀嚼片制造商重新评估关键质量属性,并确保符合适当的规格。”FDA将会对所生产咀嚼片不符合FDA质量监管期望的制造商采取适当措施以降低公...
|
|
缺乏杂质限度依据可能导致ANDA拒收
2016.08.25
8月24日,FDA重新发布《ANDA提交 — 缺乏杂质限度依据的拒绝接收》行业指南,替代了之前于2014年9月发布的《ANDA提交 — 缺乏杂质限度适当依据的拒绝接收》行业指南草案,标题中删除了“适当”一词。FDA在联邦公告通报中解释指出,“在审查了对指南草案提交的评议之后,FDA将‘适当’...
|

|
FDA发布非临床实验室研究GLP拟议规定
2016.08.24
8月23日美国FDA发布拟议规定修订联邦法规第 21 章第 58 节(21CFR58)“非临床实验室研究质量管理规范(GLP,Good Laboratory Practice)”(https//www.federalregister.gov/articles/2016/08/24/2016-19875/good-laboratory-practice-for-nonclinical-laboratory-studies...
|

|
FDA新膳食成分修订指南草案仍充满争议
2016.08.23
8月11日美国FDA向膳食补充剂行业发布了《膳食补充剂:新膳食成分通知及相关问题》修订指南草案,该修订指南替代了FDA于2011年7月发布的同名指南草案,很大程度上重申了FDA先前采取的有争议的观点。FDA 2011年指南草案反映了许多人认为与《膳食补充剂健康和教育法案》(DSHEA)的要求和意...
|

|
膳食补充剂制造商们,准备好迎接FDA检查了吗?
2016.08.22
膳食补充剂行业自20世纪90年代以来一直蓬勃发展,当时美国市场上的产品数量大约为4000种。2015年,药物测试和分析杂志估计美国制造商的数量约为15,000家,占有超过90,000种产品和400亿美元的产业。《膳食补充剂健康和教育法案》(DSHEA)于1994年通过,给了FDA根据21 CFR 111给膳食补...
|

|
MHRA对辉瑞印度工厂签发GMP不符合报告
2016.08.21
在四国监管机构联合检查辉瑞位于印度Chennai附近的工厂发现大量缺陷后,英国药品和卫生产品监管机构(MHRA)于8月19日发布GMP不符合报告(NCR),禁止向欧盟供应来自辉瑞该工厂的非关键无菌产品。
辉瑞于本月初决定暂停该工厂的生产,MHRA现在呼吁欧盟成员国的国家主管部门评估由该生产...
|
|
辉瑞扫除英利昔单抗生物类似药上市障碍
2016.08.20
联邦地区法院击碎了Janssen公司延迟Celltrion和辉瑞公司的Remicade(英利昔单抗)生物类似药在2018年成分专利到期后上市的希望。
8月17日美国麻萨诸塞州联邦地区法院法官Mark Wolf发出口头裁定,6,284,471号专利是无效的。法官在听证会之后批准Celltrion公司的简易判决动议。Celltrio...
|

|
2015年FDA有多少ANDA和505(b)(2)因请愿延迟?
2016.08.19
多年来,原研商使用请愿程序破坏ANDA和505(b)(2)批准过程,并希望推迟FDA对此类申请的批准。由于这个问题,国会被迫通过《2007食品药品管理局修正案》(FDAAA)在《食品、药品和化妆品法案》(FDCA)中新增了505(q)款规定了对请愿的回应审查时限为180天,帮助纠正这一对仿制药、505(b)...
|