
|
葛兰素史克就美国首起雷尼替丁致癌案达成和解
2023.06.26
葛兰素史克(GSK)在一份简短的声明中透露,公司与一名声称其善胃得(商品名:Zantac,通用名:雷尼替丁)胃灼热药物导致癌症的 James Goetz 达成和解,避免了即将在美国审判的首起此类案件。
James Goetz 在美国加利福尼亚州法院提起诉讼。声明表示,和解反映了 GSK“避免因本案...
|
|
亚硝胺新研究,10家国际监管实验室联合检测二甲双胍
2022.06.17
2020年,二甲双胍药品中N-亚硝基二甲胺(NDMA)含量超过了96纳克/天的每日可接受摄入量,因而引发了产品召回。在召回之前,10家国际监管实验室进行了跨国家/地区合作,检测二甲双胍的API和成品剂型(FDF)中的亚硝胺。此次研究历时9个月(2019年11月至2020年7月),使用多种方法检测了21...
|

|
FDA 两项研究发现雷尼替丁不会在体内形成亚硝胺杂质
2021.07.03
最近由 FDA 主导两项针对抗胃酸药雷尼替丁的研究显示,雷尼替丁不会在人体内形成亚硝胺。
美国医学会杂志(JAMA)在线版本于 6 月 28 日发表的评论文章1中表示,这两项 FDA 主导的研究“应该有助于缓解之前对于 N-亚硝基二甲胺(NDMA)可能会在人体内产生的担忧。”评论文章...
|

|
赛诺菲被控广泛损毁与雷尼替丁品牌药召回相关的电子邮...
2021.05.14
随着有关雷尼替丁诉讼的继续进行,代表超过超过 7 万人的律师在联邦法院提交的一份文件显示,赛诺菲销毁了与 2019 年召回的广泛使用的雷尼替丁品牌药 Zantac(善胃得)有关的无数员工电子邮件,使得消费者更难证明赛诺菲和其他生产商知道他们的药物随时间的推移可能会生成高水平的 N...
|

|
两项研究揭示雷尼替丁与亚硝胺生成和癌症风险之间的显...
2021.02.02
美国在线药房 Valisure 曾于 2019 年在胃灼热药 Zantac 及其雷尼替丁仿制药中发现异常高含量的致癌性亚硝胺杂质而引发轩然大波。全球十几个国家采取了召回行动。但对于这种常用且一部分产品是作为非处方药出售的胃灼热药引发的恐慌并不止于此,Valisure 进一步指出,雷尼替丁中的亚...
|

|
缬沙坦制药商因亚硝胺杂质问题面临欺诈指控
2021.02.02
缬沙坦中亚硝胺杂质的诉讼案有了新进展,美国新泽西州一名联邦法官于 1 月 29 日对于消费者诉缬沙坦制药商和分销商一案发布意见书,取消了消费者对于缬沙坦仿制药分销商的欺诈指控,但维持了对于制药商的欺诈指控。
新泽西州联邦地区法院法官 Robert Kugler 在意见书中指出,允...
|

|
制药商提请 FDA 延长亚硝胺风险评估期限
2020.11.25
一些制药公司希望美国 FDA 推迟其亚硝胺风险评估的截止日期(2021年3月1日),要求给予更多时间来评估新产品和已获批产品。
原因多种多样。例如,Perrigo 公司表示,内部检测场地受到新冠(COVID-19)大流行导致的居家令的影响,限制了场地进行检测和风险评估的能力。此外,由于缺...
|

|
美国司法部展开对制药商亚硝胺杂质虚假宣称的调查
2020.08.05
美国司法部已开始调查制药商是否没有透露畅销胃灼热药物雷尼替丁(商品为 Zantac,善胃得)中亚硝胺致癌物的信息而违反《虚假宣称法》。
赛诺菲和葛兰素史克两家公司在上周的证券文件中披露,他们在 6 月份收到了美国司法部对于可能违反《虚假宣称法》(FCA)信息的民事调查要求,...
|
|
FDA 发论文为亚硝胺检测方法辩护,USP 推出检测亚硝...
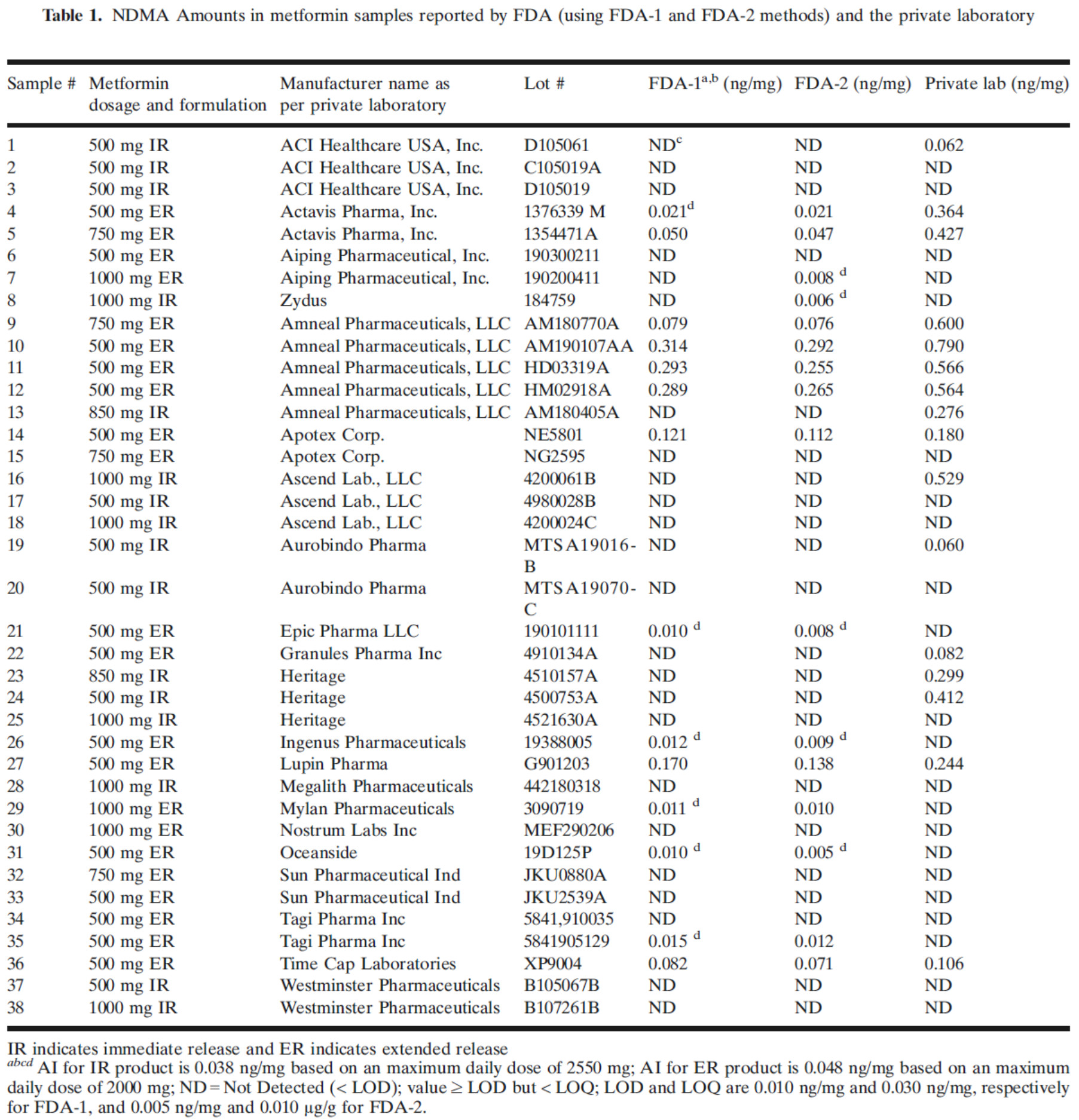
2020.07.28
美国 FDA 认为其对二甲双胍中 N-亚硝基二甲胺(NDMA)的检测结果比私营实验室 Valisure 的结果更准确。7 月份发表在美国药物科学家协会(AAPS)上的一篇论文为 FDA 的检测方法做了辩护。FDA 表示,私营实验室的方法“不适用于对二甲双胍药品中的 NDMA 进行定量分析,原因是存...
|
|
欧盟报告全面总结沙坦类药物中亚硝胺杂质的经验教训
2020.06.25
欧盟药品管理局(EMA)于 6 月 23 日发布题为《从沙坦类药物出现亚硝胺杂质事件学到的经验教训》的报告,这可能是自 2018 年夏天在缬沙坦中发现致癌性亚硝胺杂质以来由监管部门发布的最为全面详细的一份报告。
报告长达 98 页,对整个事件进行了回顾,总结的建议旨在阐明参与药...
|

|
FDA 点名五家公司召回二甲双胍缓释片
2020.06.12
美国 FDA 于今日公布了五家自愿召回二甲双胍缓释片的公司名称以及相关召回批次信息。这是 FDA 自五月末公布二甲双胍缓释片亚硝胺杂质超标,以及 6 月 5 日公布详细实验室检测数据以来短短两周内发布的第三份通告。之前虽可从检测数据和 FDA 召回网页上了解到相关产品召回的公司情...
|
|
FDA 二甲双胍 NDMA 检测结果整体低于独立实验室检...
2020.06.08
美国 FDA 于 6 月 5 日公布了其实验室对于二甲双胍样品的检测数据,我们可以从中了解到目前基于 FDA 目前检测二甲双胍中 N-亚硝基二甲胺(NDMA)杂质的水平。一周前,FDA 发布公告表示在糖尿病治疗药二甲双胍缓释制剂中发现了不可接受水平的 NDMA,并表示根据实验室检测有五家...
|
|
与原料药无关:FDA 公布二甲双胍缓释片亚硝胺杂质超...
2020.05.30
NDMA 问题不断发酵 , 并非同一现象在不同药品的重复,而是反映出行业对该杂质的科学认知不断加深。
美国 FDA 于 5 月 28 日发布通告,表示在糖尿病治疗药物二甲双胍缓释制剂中发现了不可接受水平的致癌物质 N-亚硝基二甲胺(NDMA)。但在速释制剂中尚未发现此类问题。
FD...
|

|
防范胜于补救:药物开发早期主动评估潜在遗传毒性杂质
2020.05.05
继美国 FDA 于 4 月 1 日要求所有雷尼替丁产品撤市后,欧盟也于 5 月 1 日发布通告,因可能含低水平的亚硝胺杂质,暂停所有欧盟境内的雷尼替丁产品销售和使用。近年来,亚硝胺杂质问题一波未平一波又起,一直是监管机构、工业界和公众的关注焦点。今天我们编译了一篇发表在 Pharmaceu...
|
|
FDA 关于雷尼替丁中 NDMA 杂质情况的问答更新
2020.04.03
昨日的资讯中介绍了美国 FDA 要求所有雷尼替丁制药商将产品撤市,今天我们来看看 FDA 在更新的问答文件中对于这一决定的说明。
关于雷尼替丁产品中 NDMA 杂质的重要信息
美国 FDA 已经要求制药商从市场上撤回所有雷尼替丁。这意味着雷尼替丁产品在美国将无法通过新的或现有处...
|

|
FDA 要求所有雷尼替丁产品撤市,亚硝胺杂质可在正常...
2020.04.02
内容提要:
- 在正常贮存条件下,雷尼替丁中 NDMA 含量也会增加
- 较高温度(包括产品在分销和由消费者处置的过程中产品可能暴露的温度)下贮存的样品 NDMA 显著增加
- 雷尼替丁产品越老,或者自生产出厂以来的时间越长,NDMA 的含量就越高
- FDA 向所有雷尼...
|
|
药房质疑FDA对二甲双胍中NDMA的检测结果,要求独立第...
2020.03.07
美国一家在线药房倡导制定法规对药品化学成分进行独立检测和核实,并指出 FDA 评估二甲双胍致癌性风险的检测方法需要改进。
Valisure 是美国一家在分发药品之前开展药品检验的在线药房,其于 3 月 2 日提交公民请愿,呼吁 FDA 颁布新规,要求在药品分发到患者手中之前,必须对...
|
|
FDA 公布对二甲双胍中 NDMA 的检测结果
2020.02.06
美国 FDA 于 2 月 3 日公布了对二甲双胍样品的实验室分析结果,表示,已检测的样品中都没有超出 FDA 对 N-亚硝基二甲胺(NDMA)规定的可接受限度。FDA 不建议在美国召回二甲双胍产品。
FDA 指出,一些样品没有检测到 NDMA,而另一些样品仅检出较低水平的 NDMA。低水平类...
|
|
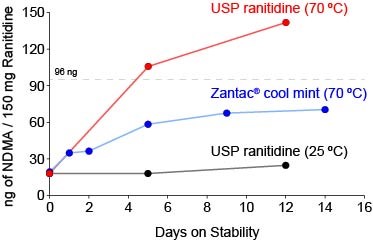
雷尼替丁亚硝胺杂质问题再升级,可在运输和贮存过程中...
2020.01.09
雷尼替丁中致癌性亚硝胺杂质问题再次升级,一家检测实验室向美国 FDA 提交公民请愿,表示经检测,即使药品在包装完好的状态下暴露在高温环境中,可疑致癌物 N-亚硝基二甲胺(NDMA)的含量也会增加,因此呼吁 FDA 召回所有雷尼替丁药物。
该检测实验室为位于加利福尼亚州 Alameda...
|

|
【周末杂谈】致癌杂质与合理监管
2019.12.08
三天前,美国FDA发表的正在调查二甲双胍样品中是否存在不安全水平的致癌物 N-亚硝基二甲胺(NDMA, N-Nitrosodimethylamine)的声明中, 药品审评与研究中心主任Janet Woodcock医学博士说“NDMA 是在水和食物,包括腌制和烧烤肉类、奶制品和蔬菜,中发现的常见污染物。每个人都暴露...
|