
|
ANDA申报流程及材料清单上线了
2018.08.29
自片剂工艺验证流程以来,识林陆续梳理了胶囊剂工艺验证流程、美国FDA DMF申报流程、EDQM-CEP申报流程等场景应用工具,且每个流程的关键步骤都配有参考资料清单,申报资料的编写也做了详细总结。
场景应用工具上线后,用户好评并积极反馈,也有更多专业人士进入识林“植树”,识林...
|

|
从请愿回复看 FDA 的科学监管
2018.08.26
美国 FDA 每年都会收到许多要求 FDA 就撤出或停止销售的产品是否是出于安全或有效性问题做出决定的请愿,FDA 会做出相应回复。这类决定对于是否允许使用参照产品(RLD)作为提交基础的其他获批仿制药申请(ANDA)继续销售,以及 FDA 是否继续接受参照该 RLD 的 ANDA 都至关重要...
|
|
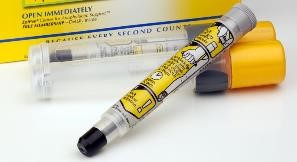
FDA 延长 EpiPen 效期以缓解短缺压力
2018.08.24
由于 EpiPen(肾上腺素自动注射器)间歇性供应中断,美国 FDA 于 8月 21 日采取额外措施,通过将 Mylan 公司的 EpiPen 以及辉瑞旗下公司生产的授权仿制药版本的特定批次的 0.3 毫克产品的有效期延长 4 个月来缓解 Epi Pen 的短缺。
FDA 药品审评与研究中心主任 Janet W...
|

|
缬沙坦事件中美国 FDA 耐人寻味的行动
2018.08.23
【编者按】回顾缬沙坦召回事件发生以来,各类报道铺天盖地,讨论涉及监管、技术、商务和法律等各层面,一位具有 30 多年美国制药业高管和咨询经验的识林资深作者注意到美国 FDA 在次此事件中一些非同寻常的行动,遂撰文与大家分享。这也让编者想起几年前 Woodcock 博士曾在一次药...
|

|
FDA 发布咀嚼片的质量属性考量定稿指南
2018.08.22
美国 FDA 于 8 月 20 日发布《咀嚼片的质量属性考量》定稿指南。该指南向新药申请(NDA)、仿制药申请(ANDA)、一些化学补充剂、IND 的申办人以及非申请的咀嚼产品生产商提供有关可咀嚼速释片剂鉴定和量化应有的关键属性的建议。
该定稿指南的草案版本于 2016 年 6 月 16...
|
|
FDA 高溶解性原料药速释口服固体药溶出度和接受标准...
2018.08.21
在 IND、NDA、ANDA 申请中,有关含高溶解性原料药的口服速释(Immediate Release, IR)产品可以使用标准释放试验和标准去替代大量的方法开发和可接受标准制定工作,这些标准的可用性将有助于快速开发溶出方法和相关接受标准,而不要求在药品研发阶段证明这些溶出方法对产品的分辨能力...
|

|
IPEM 十周年专题报告会
2018.08.21
Regulate sensibly 合理监管,develop scientifically 科学研发,manufacture competitively 高效生产,compete respectfully 尊矩竞争,and manage responsibly 尽责管理 — 摘自IPEM招生简介
IPEM所学与所用 — IPEM十周年专题报告会
2018年8月31日(周五)
...
|

|
信誉比专业更重要,前西门子人士出任诺华首席道德官
2018.08.20
Klaus Moosmayer 出任诺华首席道德、风险与合规官,以重塑丑闻后的公司信誉。
Moosmayer 将于今年 12 月 1 日加入诺华,直接向首席执行官汇报。诺华在其任命公告中将 Moosmayer 称为“道德与合规领域公认的全球领导者”。他的简历包括在经济合作与发展组织担任工商业咨询委员...
|
|
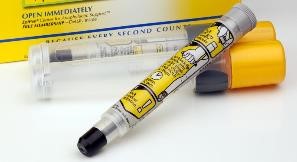
复杂仿制药研发的胜利 — 首个 EpiPen 仿制药获批
2018.08.18
【编者按】对药械组合产品的仿制药,疗效等效意味着不仅要药物等效,在装置使用方便性上,也要同样好使。但达到使用装置上的等效不易。FDA 在去年的药械组合仿制产品指南中曾严格这方面的要求,今年 4 月份 FDA 表示可能会重新考虑这一要求,允许某些装置差异。EpiPen 仿制品的获...
|

|
国际危机事件管理的法律、商务和技术考虑
2018.08.17
“尚质学社”学习交流会 — 国际危机事件管理的法律、商务和技术考虑
2018年9月2日 (周日) 900-1330
数据可靠性(DI)引起的进口禁令和警告信危机还未趋缓,原料药杂质引起的全球产品召回危机又至。快速升级的中美贸易战更是雪上加霜。了解美欧市场的监管风险、商务风险、...
|

|
公众对生似药与复杂仿制药的接受程度不尽如人意?
2018.08.16
许多文章都曾谴责这样一个事实,即,对生物类似药的使用程度远低于美国 FDA 或业界预期。我已经在这个行业以不同身份工作了 46 年(药剂师、监管者和顾问),见惯了这样的情况。有人说历史再次重演,但今天的观念和力量与 Hatch-Waxman 法案首次颁布时的是一样的。什么观念和力量?...
|

|
贸易战下的合规风险 — 美国新法案可能影响我国制药...
2018.08.15
【编者按】随着贸易战的不断升级,专业人士开始认识到贸易战绝不是加税减税这么简单,高科技产品和技术不仅面临准入风险,合规帐全面清算,将产生更为深远的影响,在中国企业近期的召回事件中,FDA 高层领导的频繁表态,表明技术因素不是FDA的唯一考虑,君合是国内权威律所,他们近期在...
|

|
2018 年 FDA 首仿药清单小结
2018.08.14
【编者按】多年来,首仿药意味着价格比品牌药略低但远高于一般仿制药,意味着抢占市场……现如今对于越来越多的复杂产品来说,首仿更意味着一种鼓励、一种证明,当前技术可以成功地开发出与复杂产品等效的仿制药。FDA多批快批首仿药,并提高透明度,有助于企业,更有益于民众。
“首仿...
|

|
识林原料药注册指导三大工具:第二部分“初始递交材料...
2018.08.13
法规环境日益严格和复杂,注册的责任和压力也越来越大,既要对内准确传递监管的要求,又要对外严格满足监管的要求,例如:
- 官方缺陷信回复的时限日益紧迫,企业面临缺陷大海捞针查指南,耗费宝贵时间;
- 不同监管机构、不同指南之间内容重复但不重合,容易顾此失彼;
...
|

|
WHO 生物类似药问答指南草案中文翻译
2018.08.12
两周前,WHO 发布《生物类似药问答指南草案》,识林对指南内容做了简要介绍【WHO 就八年来生物类似药的常见问题给出指导 2018/07/31 】。识林现已将指南草案译成中文。
问答草案涉及概念、参照生物药、质量、非临床、临床和药物警戒六大块共 48 个问题。其中包括对于在什么情况...
|

|
FDA 首个获得竞争性仿制药认定的产品获批
2018.08.09
美国 FDA 于 8 月 8 日批准了几种规格的氯化钾口服液,成为通过竞争性仿制药(CGT)认定批准的首例仿制药。这一新批准路径旨在加快针对缺乏竞争产品的仿制药的研发和审评。氯化钾是一种口服治疗药物,适用于治疗和预防使用利尿剂患者在缺少富钾饮食或无法减少利尿剂用量时的低钾血症...
|

|
业界探讨如何使 ICH Q12 的价值最大化
2018.08.07
行业正在探索 ICH Q12 生命周期管理概念如何在内部实施中以及在与监管机构的互动中最大化实践价值。ICH 专家工作组(EWG)成员鼓励业界与工作组分享其经验、实施挑战以及如何改进指南草案。工作组还有兴趣听取行业对于证明有效的实施策略的反馈,从而可以作为培训工作的一部分更广泛地...
|

|
美国药品代码格式迎来新变化
2018.08.06
美国国家药品代码(NDC)是处方药产品的唯一标识符。FDA 在联邦公报发布https//www.federalregister.gov/documents/2018/08/07/2018-16807/hearings-future-format-of-the-national-drug-code 通告表示未来几年内将改变 NDC 格式以适应更多厂商进入美国市场的需要。FDA...
|

|
FDA 向三个连续制造项目提供近六百万美元资金
2018.08.03
根据美国 FDA 8 月 1 日公布的消息,FDA 根据《21 世纪医药法案》向高等教育机构和非营利组织提供了三项资金支持,以研究和建议改进药品和生物制品连续制造的改进,以及类似的创新监测和控制技术。获得资金支持的机构和项目分别是:
• 罗格斯大学,工业 4.0 在连续药品制造中...
|

|
WHO 发布生物类似药问答指南草案
2018.07.31
世界卫生组织(WHO)于 7 月 26 日发布生物类似药问答指南草案,邀请利益攸关方提出反馈意见。该指南草案一经定稿将有助于进一步支持 2009 年生物类似药评估指南的实施。问答草案基于监管机构在过去八年中关于如何落实 2009 年指南的常见问题。WHO 将在 9 月 20 日之前接收有...
|