
|
制药巨头放弃抗生素开发,靠政府资本还是监管手段?
2022.07.26
Covid-19病毒广受关注,特朗普政府为了预防新冠病毒在美国继续传播,发起了“曲速行动”(Operation Warp Speed)计划,以加快疫苗的开发并且能够达成大规模制造和销售。但除了新冠病毒之外,细菌耐药性不断增强也使得感染病的风险增加。经过几十年的努力,新型抗生素仍然处于严重缺乏...
|
|
老药新用亟需有效激励措施,开启药物研发新模式
2022.04.25
美国FDA于1984年颁布《药品价格竞争和专利期恢复法案》(Drug Price Competition and Patent Term Restoration Act),即人们熟知的Hatch-Waxman法案,从此开启仿制药监管的新篇章。如今,仿制药占处方药总量的90%左右,为医保系统节省大量成本。
根据PharmaProject和DrugBank...
|

|
【全文翻译】2021 年 FDA 新药审批总结报告
2022.01.10
美国 FDA 于 2022 年 1 月 6 日发布了其 2021 年度 FDA 新药审批总结报告。报告汇总了 FDA 药品审评与研究中心(CDER)去年一年中批准的所有新药、新用途和新使用人群以及生物类似药和可互换生物类似药、新配方和新剂型以及儿科人群扩展,概述了一系列值得注意的批准,提供了...
|
|
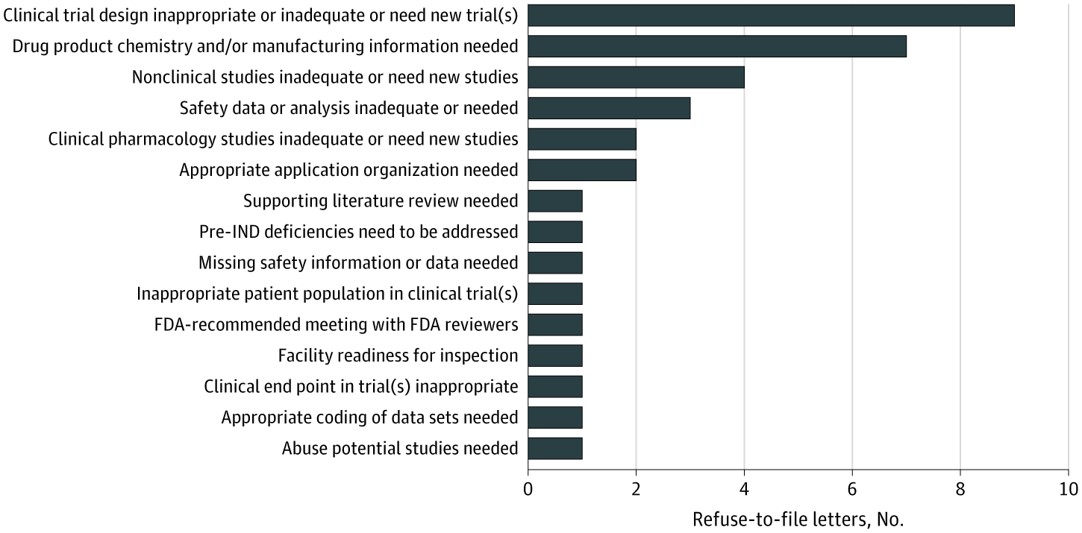
FDA 立卷审查拒收原因和公开披露情况分析
2021.02.19
日前发表在《美国医学会杂志》内科医学研究上的一项研究1发现,美国 FDA 通常会针对“实质性”缺陷发出立卷审查拒收(refuse-to-,RTF)函,这些缺陷包括缺少产品质量、安全性和有效性所需的信息。
这项研究的主要作者是 FDA 局长办公室公共卫生策略和分析人员 Harinder Singh Ch...
|
|
FDA 对非酒精性脂肪性肝炎(NASH)药物开发问题的解...
2021.02.16
在最近美国 FDA 举行的非酒精性脂肪性肝炎(NASH)的新药开发网络研讨会上,与会者提出了众多问题,显示了这一药物研发领域的热度。申办人们关心的问题涵盖从生物标志物的使用到试验时长。
在 1 月 29 日的研讨会上,FDA 药品审评与研究中心(CDER)免疫与炎症办公室肝病与营养...
|

|
【全文翻译】2020 年 FDA 新药审批总结报告
2021.01.12
美国 FDA 于 2021 年 1 月 8 日发布了其 2020 年度 FDA 新药审批总结报告。报告汇总了 FDA 药品审评与研究中心(CDER)去年一年中批准的所有新药、新用途和新使用人群以及生物类似药、新配方和新剂型,概述了一系列值得注意的批准,提供了许多 CDER 批准的新治疗药物促进患...
|

|
FDA 发布关于 ANDA 完全回应函延期回复的指南草案
2020.09.29
美国 FDA 于 9 月 28 日发布《在监管期限内未能回复 ANDA 完全回应函》的行业指南草案,旨在帮助提交简化新药申请(ANDA)申请人请求延长对 FDA 完全回应函(CRL)的回复。指南描述了 ANDA 申请人在 CRL 发布后必须采取的行动,以及如果申请人未能对 CRL 做出回复 FDA 可能...
|
|
阿达木单抗的 BE 试验经验总结
2020.09.04
9月3日,信达生物的阿达木单抗注射液获国家药监局批准,成为继百奥泰和海正药业之后第三个国产阿达木单抗生物类似药。
艾伯维的修美乐(阿达木单抗)于2002年12月31日首次获得美国FDA批准上市,2010年2月26日首次国内获批进口。修美乐自2014年开始,已经连续6年成为全球药品销售冠军,20...
|

|
识林药品数据库上线啦!
2020.08.31
同步更新全球新药审评报告
截至2020年8月20日,识林药品数据库收录了近3万个CDER批准的人用药(包括生物制品)和EMA集中审评批准/拒绝的人用药的10万余份审评和支持资料,并每周更新,经本地化处理,访问速度快。
数据库包括产品的规格、剂型、市场状态、审评资料、说明书等各类信息...
|
|
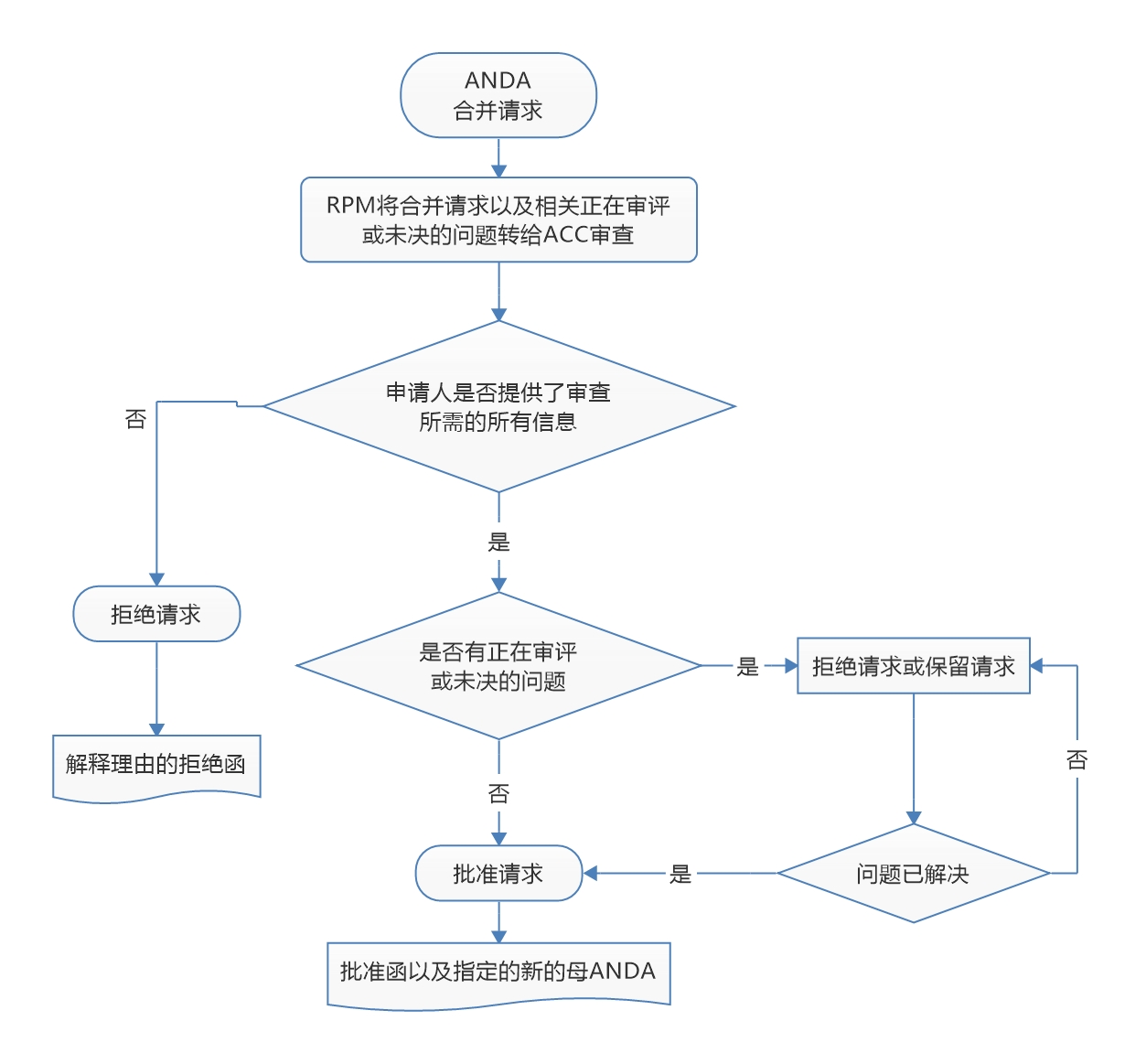
FDA 发布同一产品不同规格 ANDA 号合并的修订程序...
2020.08.21
美国 FDA 仿制药办公室(OGD)于 8 月 19 日发布了修订政策与程序手册(MAPP 5241.2 Rev.1)《仿制药办公室的ANDA合并》,介绍了相同厂家、同一药品、不同规格的多个 ANDA 申请号合并为一个 ANDA 申请号的政策和程序。
该手册的最初版本于 2015 年 10 月发布,此次发...
|
|
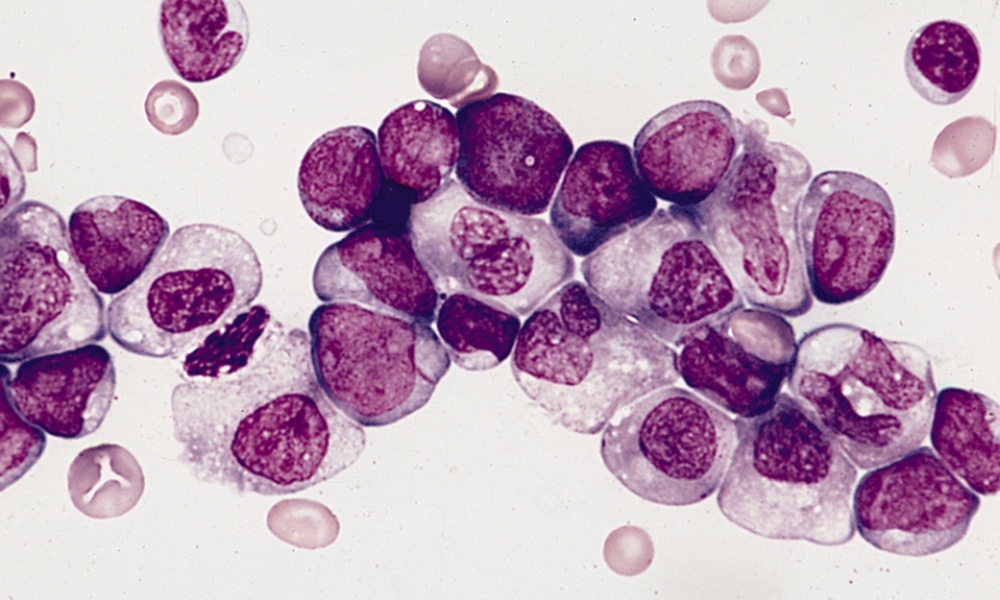
FDA 新发布急性髓细胞白血病治疗药开发指南草案
2020.08.19
美国 FDA 于 8 月 17 日发布了《急性髓细胞白血病:开发用于治疗的药品和生物制品》新指南草案,协助申办人对治疗急性髓细胞白血病(AML)的药品和生物制品进行临床开发。指南草案涉及 FDA 对于支持 AML 治疗适应症(包括仅限于单独治疗阶段的适应症,例如,维持、移植准备方案...
|

|
FDA 定稿指南明确对未能公开临床数据的企业罚款
2020.08.18
美国 FDA 发布了《有关 ClinicalTrials.gov 数据库的民事处罚》定稿指南。指南解决了 FDA 各中心应如何应对违反联邦法规要求,未能准确、完整地登记注册临床试验并在 Clinicaltrials.gov 网站上报告结果的责任方的问题。FDA 各中心包括药品中心、生物制品中心和器械中心。
FD...
|
|
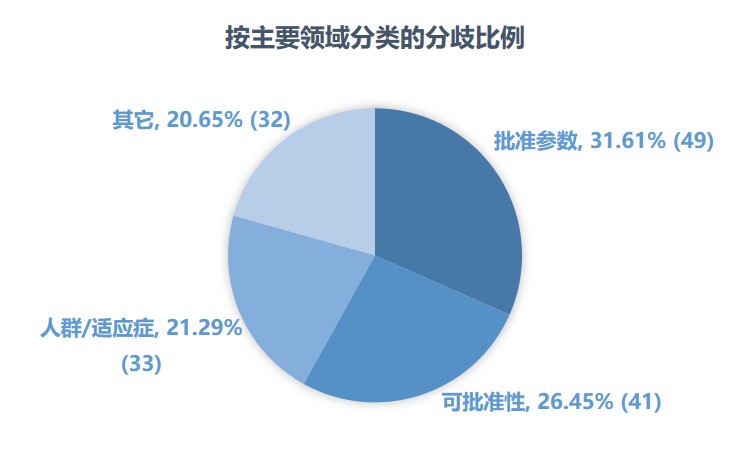
FDA 新药批准近四分之一存在内部审评意见分歧
2020.08.15
自美国 FDA 于去年夏天宣布以综合审评文件取代基于学科的审评文件包以来,研究人员和利益相关者们就一直持反对意见,担心能看到的公开信息会随之减少,一些有价值的信息将无法轻易获得,其中 FDA 内部审评意见的分歧就是最有价值的信息之一。研究人员最近发表的一项分析就反映了这方面...
|
|
糖尿病药上市前安全性争论不停,FDA 新指南草案受质...
2020.07.21
美国 FDA 于 3 月份发布《2 型糖尿病:评估新药的安全性以改善血糖控制》指南草案向公众征询意见,指南中关于糖尿病药物 III 期安全性数据库的规模和组成引发了业界的担忧。企业认为,指南对 III 期试验安全性的建议过于严苛,并且规模不必要的大,且缺乏正当性。
利益相关者...
|

|
FDA 四篇定稿指南扩大癌症试验特殊人群入组标准
2020.07.13
美国 FDA 7 月 10 日发布了四篇定稿指南,分别针对脑转移瘤患者、HIV或乙肝或丙肝患者、器官功能障碍或既往和并发恶性肿瘤患者、儿童患者人群的癌症试验资格标准给出了指导意见,并给出了针对将儿童患者纳入癌症试验的最低年龄考虑。
这些指南由 FDA 药品审评与研究中心(CDER)...
|

|
药品申请数据化:抛弃 PDF,拥抱结构化持续更新数据...
2020.07.07
美国 FDA 最近数据策略现代化公开会议上,一个由多家制药公司发起的项目 — Accumulus 项目崭露头角。这一项目正在努力通过终止对“数字化纸质文件”(PDF 文件)的依赖来简化申请的提交和审评。
Accumulus 涉及创建一个平台,允许滚动数据流,而不是现在提交的在单个时间点的数...
|
|
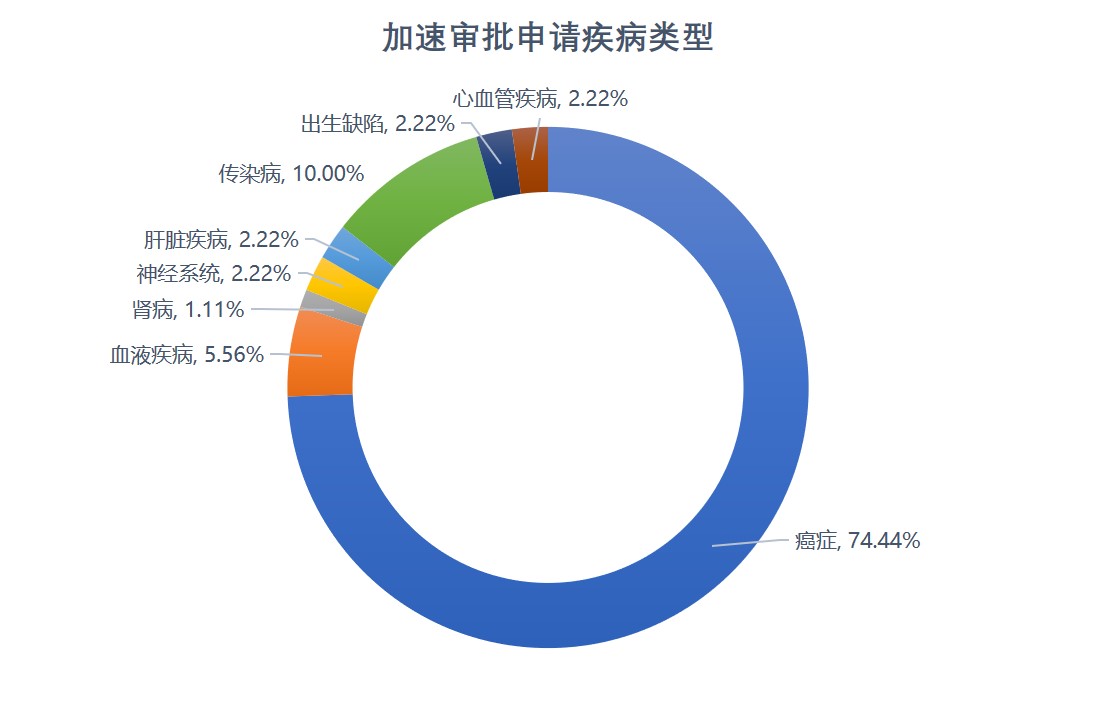
FDA 加速审批现状:问题与热度并存,抗癌药占大多数
2020.07.07
美国 FDA 加速审批计划实施已经超过 25 年了,FDA 正在着手评估该计划的未来,但是根据统计数据显示,2020 年可能出现创纪录的加速审批申请。
据 Pharma Intelligence 统计,FDA 2020 年到目前为止批准的新药和生物制品申请以及有效性补充申请中,超 14% 获得了加速审批,远高...
|

|
仿制药研发现代化:定量方法和建模
2020.06.24
如何将建模方法与目前研发过程中收集的数据和信息相整合证明仿制药生物等效性,降低成本缩短研发时间,助力仿制药研发?FDA 药品审评与研究办公室(CDER)最近发布的一篇关于定量方法和建模的介绍“Impact Story Modeling Tools Could Modernize Generic Drug Development”提...
|

|
基因治疗产品开发瓶颈:缺乏明确灵活的监管框架
2020.06.23
监管者承认缺乏明确的监管框架阻碍了基因治疗产品的开发和加速,而业界则认为监管应该灵活一些以适应产品不断变化的技术。
美国 FDA 生物制品审评与研究中心主任 Peter Marks 于 6 月 15 日在药物信息年会(DIA)在线会议上表示,需要新指导手册来确保对基因治疗产品执行一致...
|

|
美欧加三监管机构官员谈加速审批计划
2020.06.20
来自美国 FDA、欧盟药品管理局(EMA)和加拿大卫生部(Health Canada)的监管者们日前在药物信息协会(DIA)全球年会上就各自管辖区中加速批准路径有关的不同问题发表了看法。
所有三个监管机构都提供与传统上市批准所要求的相比较不全面的临床数据的加速批准形式。在美国,该路径被...
|