|
韩国呼吁为新冠疫苗接种者提供全面赔偿机制
2021.04.27
韩国医学协会(KMA)敦促韩国卫生当局对被认为遭受新冠疫苗不良影响的人提供更积极、更全面的保护机制,而不是仅对因果关系明确的人提供补偿。
目前韩国一名 40 多岁护士助手的丈夫在接种阿斯利康新冠疫苗后被诊断出患有急性弥漫性脑脊髓炎,并表现出瘫痪症状,在接种疫苗后住院 19...
|
|
美国疾控中心建议恢复使用强生新冠疫苗
2021.04.24
美国疾病控制与预防中心(CDC)免疫实践咨询委员会于周五(4 月 23 日)下午投票得出结论,建议在美国恢复使用强生新冠疫苗。
此前由于接种强生疫苗后出现的六例严重血栓病例,美国 FDA 和 CDC 于 4 月 13 日共同建议暂停在美国使用强生新冠疫苗【美国因罕见血栓病例叫停强生新...
|

|
FDA 代理局长谈卓越中心、疫情工作重点及加速批准审...
2021.04.20
首先需从疫情中恢复,不宜大刀阔斧改革
美国FDA 代理局长 Janet Woodcock 4 月 14 日在对更强 FDA 联盟(Alliance for a Stronger FDA)发表讲话时表示,当前的大环境不是在 FDA 进行大刀阔斧改革的合适时机,并讨论了 FDA 将如何使用其新获得的疫情资金以及对加速批...
|
|
强生希望与竞争对手联合研究血栓问题:或避之不及,或...
2021.04.19
根据美国《华尔街日报》4 月 16 日援引知情人士的消息,强生公司上周与其新冠疫苗竞争对手阿斯利康、Moderna 和辉瑞联系,希望联合起来研究在一些疫苗接种者中罕见和严重的血栓病例。目标是,组建一个联盟,交流疫苗的获益和风险,以减轻公众的恐惧。
监管机构已经在调查可能与阿斯...
|
|
美国因罕见血栓病例叫停强生新冠疫苗,WHO 将等待欧...
2021.04.14
美国疾病控制和预防中心(CDC)和 FDA 于美国时间周二早(4 月 13 日)共同建议各州停止使用强生下属子公司杨森的新冠疫苗,同时对六例严重血栓病例进行调查。
这些罕见的血栓病例与使用阿斯利康新冠疫苗后报告的问题相似。【欧盟宣告阿斯利康新冠疫苗与血栓事件之间存在关联,可...
|

|
辉瑞推出首个新冠病毒主蛋白酶靶向口服药,尚处早期试...
2021.04.14
辉瑞公司于 4 月 6 日在 2021 年美国化学会春季会议上透露了其口服新冠抗病毒临床候选药物 PF-07321332 的当前开发情况,共享了化合物结构和临床前数据。
该化合物当前处于 I 期临床试验,是临床上首个口服给药的化合物,该化合物靶向新冠病毒 SARS-CoV-2 的主蛋白酶 — ...
|

|
欧盟宣告阿斯利康新冠疫苗与血栓事件之间存在关联,可...
2021.04.08
欧洲药品管理局(EMA)已经得出结论,阿斯利康的新冠疫苗与在许多使用该疫苗的国家/地区报告的罕见但危险的血栓事件之间存在联系。
EMA 于 4 月 7 日发布公告,其安全性委员会(PRAC)得出结论认为,该疫苗“应将异常的低血小板血栓列为非常罕见的副作用。”前一天已有欧盟官员透露...
|

|
FDA 发布疫情期间仿制药研发和申报问答指南
2021.04.07
美国 FDA 于 4 月 5 日发布了针对仿制药生产商的新问答指南,以解决新冠(COVID-19)公共卫生紧急事件期间仿制药开发以及简化新药申请(ANDA)申报和评价相关问题。
FDA 表示,“FDA 认识到 COVID-19 公共卫生紧急事件可能会影响仿制药产品的开发,中断或延迟 ANDA 申请...
|

|
欧盟官员首次表示阿斯利康新冠疫苗与罕见血栓事件之间...
2021.04.07
欧洲药品管理局(EMA)的一名官员于 4 月 6 日首次承认阿斯利康/牛津大学新冠疫苗与疫苗接受者中罕见血栓之间存在联系。但他表示接种疫苗的获益仍超出风险。
据路透社报道,随着血栓报告数量的增加,EMA 疫苗负责人 Marco Cavaleri 对意大利报纸 il Messaggero 表示,“我...
|

|
FDA 公布新冠应对五大重点,探索远程检查改革紧急使...
2021.04.06
美国 FDA 于 4 月 2 日发布了有关新冠大流行恢复和应对计划(PREPP)倡议的更新报告,表示将努力改善大流行应对的五个方面,以使 FDA 在当前和未来的公共卫生紧急情况中更具灵活性。
FDA 代理局长 Janet Woodcock 表示,“随着我们持续应对新冠疫情,至关重要的是,我们必...
|

|
阿斯利康发布新冠疫苗最新分析数据百分之七十六保护效...
2021.03.26
阿斯利康于 3 月 24 日公布了其新冠(COVID-19)疫苗临床试验的最新分析数据,显示其疫苗在降低有症状 COVID-19 方面的保护效力为 76%,对严重疾病的保护效力为 100%。
关注阿斯利康新冠疫苗信息的人们最近恐怕感觉有点戏剧性,先是阿斯利康于周一公布其美国 III 期临床...
|

|
NIH 深夜罕发声明质疑阿斯利康发布过时新冠疫苗信息...
2021.03.24
无论数据相差多少,只要有这种事情发生,就会削弱公众的信任
美国国立卫生研究院(NIH)采取罕见举动,于 3 月 23 日凌晨发布声明对阿斯利康于前一天发布的在美国的新冠(COVID-19)疫苗 III 期试验的数据提出了新的质疑。
声明表示,周一(阿斯利康公布初步结果的当天)晚些...
|

|
阿斯利康新冠疫苗美国试验结果公布,保护效力优于预期
2021.03.23
阿斯利康于 3 月 22 日(本周一)发布新闻稿宣布了其与牛津大学合作的新冠(COVID-19)疫苗 AZD1222 美国 III 期临床试验的期中分析结果:有症状 COVID-19 方面的保护效力为 79%,重症 COVID-19 与预防住院方面的保护效力为 100%,65 岁及以上人群的保护效力为 80%...
|
|
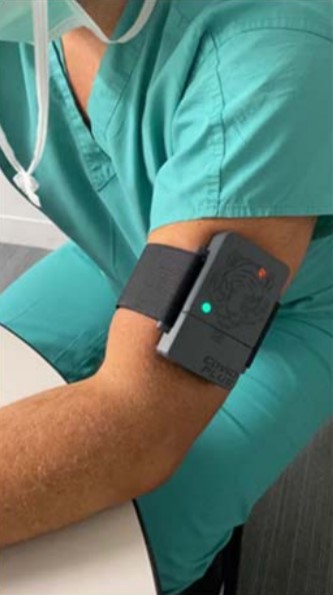
FDA 授权首个基于机器学习的新冠筛查臂带设备
2021.03.23
美国 FDA 于 3 月 19 日对首个基于机器学习的新冠(COVID-19)非诊断性筛查设备“Tiger Tech COVID Plus Monitor”发布了紧急使用授权(EUA),该设备可鉴别指示某些症状类型的生物标志物,例如血液高凝状态(一种导致血液比正常情况更容易凝结的状况)。该设备的设计目的是在...
|
|
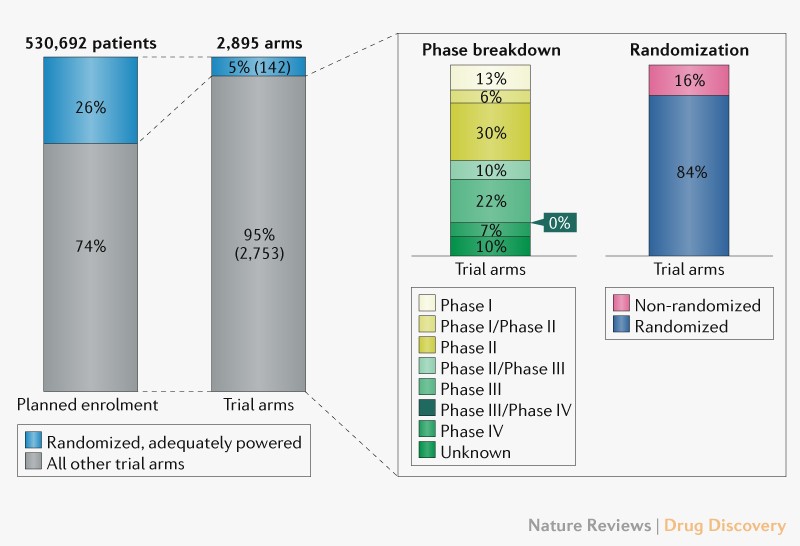
FDA 代理局长与卫生研究院院长谈新冠疫情给医药行业...
2021.03.15
新冠(COVID-19)大流行之后,生物制药研究将何去何从?美国 Milken 研究所组织了来自联邦机构、非营利组织和制药行业的领导人召开了为期一小时的讨论会,回答了从 COVID-19 学到的经验教训,以及在大流行后生物医学创新是否存一线光明。
美国 FDA 代理局长 Janet Woodcock ...
|
|
从 mRNA 疫苗具体生产步骤看为何难以放大
2021.03.05
【编者按】昨日发表在《华尔街日报》卫生板块下的一篇文章以辉瑞/BioNTech 新冠疫苗的生产过程为例,试图通过简洁和图形化的方式向公众介绍为何 mRNA 新冠疫苗难以放大生产。对于制药人来说可能相对浅显,但其中不乏一些有意思的细节。现编译如下,供大家参考。
辉瑞及其合作伙伴 Bio...
|

|
请来厂里检查吧?FDA:等等再说
2021.03.03
美国 FDA 的现场检查工作随着新冠(COVID-19)疫情的持续仍处于不确定状态。药品申办人急于想了解如何才能向 FDA 保证其场地可以安全地进行检查,以期让已经延迟的产品批准尽快走向正轨。
一种想法是制定详细的现场检查接待计划。Hyman, Phelps and McNamara 律所律师 Douglas Fa...
|
|
如何看待和沟通新冠疫苗保护效力差异?
2021.03.02
强生下属杨森(Janssen)公司的腺病毒载体新冠(COVID-19)疫苗已于周六获得美国 FDA 的紧急使用授权(EUA),下一步面临的问题可能是与已获授权的两款 mRNA 疫苗的效果比较和公众教育。因为单从目前临床试验得出的数据上看,杨森的疫苗为 66.1%,而辉瑞/BioNTech 和 Moderna 的...
|

|
欧盟发布针对新冠病毒变体的疫苗开发指南
2021.03.01
欧洲药品管理局(EMA)近日发布了一份思考性指南文件列出了支持预防新冠病毒(SARS-CoV-2)变体的疫苗许可所需的数据和要求。EMA 在宣布新指南的新闻稿中表示,“为疫苗的适应性制定快速监管程序,以保护公众免受当前或未来变体的侵害是当务之急。”
在此之前 2 月 10 日,国际...
|

|
【快讯】杨森新冠疫苗专家会意见,22-0 全票支持紧...
2021.02.27
北京时间 2 月 27 日早 6 点 10 分,美国 FDA 就杨森(Janssen)新冠疫苗Ad26.COV2.S的紧急使用授权(EUA)召开的专家会刚刚结束。在结束了一整天对杨森新冠疫苗的广泛讨论后,外部专家全票(22赞成,0 反对)通过,认为基于可用全部科学证据,杨森的新冠疫苗在 18 岁及以...
|