
|
FDA 前局长谈促进仿制药竞争等问题
2019.11.09
前美国 FDA 局长 Gottlieb 于 11 月 6 日在普享药协会(AAM)举办的 GRx+Biosims 2019会议上表示,FDA 对风险评估与减轻策略(REMS)滥用等方面的关注可能会促使某些品牌药申办人将策略重点转向商业领域来阻止仿制药竞争进入市场。
Gottlieb 现在已回到私营企业工作,他在...
|

|
CRO 相关临床数据欺诈正日益受到美国司法部重视
2019.11.05
美国司法部的执法重点日益集中在与临床试验数据欺诈有关的问题上,尤其是在涉及合同研究组织(CRO)的情况下。司法部消费者保护部门负责人 Gustav Eyler 在食品药品法律研究所(FDLI)最近举行的有关医药产品广告和促销的会议上表达了上述担忧,并指出,在调查涉及虚假和误导性营销的潜...
|

|
FDA 希望通过数字健康工作组解决药品软件组合产品相...
2019.11.02
随着软件和药之间的联系日益紧密,美国 FDA 已调集其专家人员成立数字健康工作组,以做出政策决定并帮助申请审评人员。该工作组将解决与药品共同使用的软件有关的政策问题。工作组包括来自器械与放射健康中心(CDRH)和药品审评与研究中心(CDER)以及组合产品办公室的代表。
CDER ...
|

|
FDA 因生物等效性数据问题撤销两 ANDA
2019.10.31
美国 FDA 于 10 月 28 日在《联邦公报》上发布了两份关于撤销简化新药申请(ANDA)批准的通告,原因是 FDA 对申请中所含生物等效性数据缺乏信心。FDA 表示,撤销拟议的依据是,“ANDA 持有人一再未能提交所需的数据来支持对 ANDA 生物等效性的发现。
撤销涉及生物等效性测试实...
|

|
FDA 允许某些组合产品软件通过 DMF 提交
2019.10.30
美国 FDA 于 10 月 28 日发布《CDER 主导的使用电子或软件的器械组成部分的组合产品的 V 类 DMF》指南草案,允许将某些电子或软件组成部分作为药物主文件(DMF)提交来进一步简化组合产品批准流程。
当 FDA 药品审评与研究中心(CDER)主导申请评价时,申报人可以使用 V 类...
|

|
FDA 发布关于上市后研究和临床试验要求的指南草案
2019.10.25
美国 FDA 于 10 月 24 日发布题为《上市后研究和临床试验 — 联邦食品、药品和化妆品法案 505(o)(3) 的实施》修订指南草案。如果企业的任何产品有批准后研究要求,则应密切关注该指南文件。
FDA 在介绍指南时表示,“该指南阐述了 FDA 根据 FD&C 法案第 505(o)(...
|

|
EMA 指明亚硝胺污染的潜在来源
2019.10.23
欧洲药品管理局(EMA)于 10 月 18 日更新“对上市许可持有人(MAH)关于亚硝胺信息”的问答指南,增加第 12 个问题,列出了药品中亚硝胺污染的潜在来源,以帮助企业遵守 EMA 最近对于企业在亚硝胺污染方面的审查和评估要求。
在上月初美国一家在线药房发现赛诺菲的抗酸药 Zant...
|

|
临床早期药品生产的 GMP 合规是避免申请被拒的关键
2019.10.22
为避免日益增加的与 GMP 相关的新药批准延迟,企业应更早开始遵守美国 GMP 要求,Covington Burling 律所合伙人 Tom Cosgrove 在 9 月 19 日的 PDA 数据可靠性研讨会上如是表示。他指出,企业应在就 I 期临床研究递交研究用新药申请时就开始遵守 GMP,但目前大多数企业等到...
|

|
FDA 三十年来首次更新 DMF 指南
2019.10.21
美国 FDA 于 10 月 18 日发布《药物主文件(DMF)》指南草案,待最终定稿后该指南将取代 1989 年发布的《药物主文件:指南》。指南基于新的法律、政策和程序,以及与 GDUFA 承诺函相关的程序和电子提交要求,对 DMF 的要求和程序做了许多修改。指南文件还提供了关于指南的新联...
|
|
FDA批准治疗囊性纤维化的新突破性治疗 20191021
2019.10.21
The U.S. Food and Drug Administration today approved Trikafta (elexacaftor/ivacaftor/tezacaftor), the first triple combination therapy available to treat patients with the most common cystic fibrosis mutation. Trikafta is approved for patients 12 years...
|
|
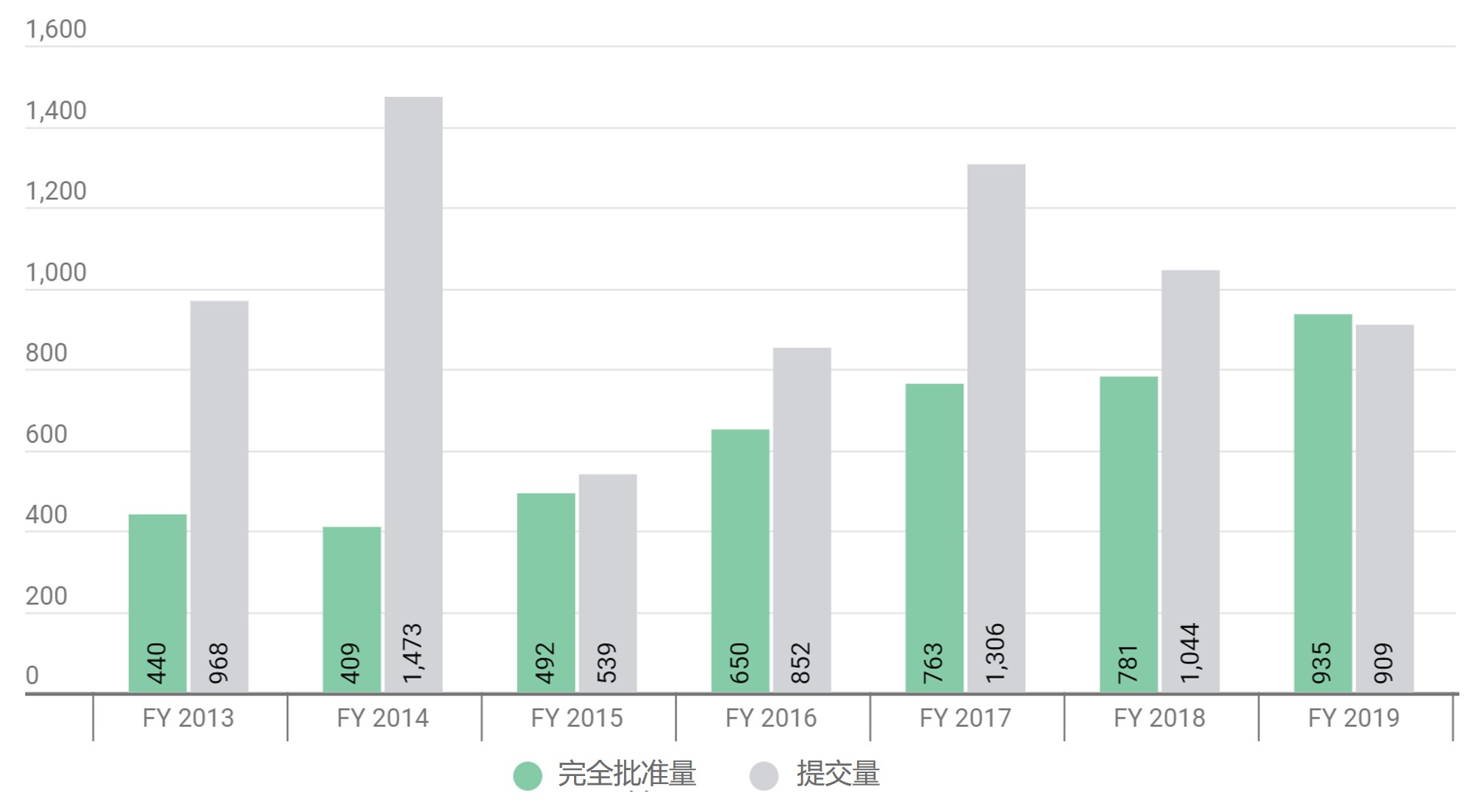
FDA 2019 财年仿制药批准破 900,批准量首超提交量
2019.10.19
2019 财年已经结束,自美国仿制药使用者付费计划(GDUFA)实施以来,这是 ANDA 批准行动数量首次超过提交数量(935 件批准,909 件新 ANDA 提交)。此外,FDA 仿制药办公室(OGD) 2019 财年以 935 件批准的成绩再次打破了批准记录,比 2018 财年 的 781 件批准多出 154 件(...
|

|
欧盟发布有关先进治疗产品的 GCP 指南
2019.10.18
欧盟委员会(EC)于 10 月 16 日根据 2007 先进治疗医药产品(ATMP)法规发布了关于这些复杂和创新产品临床试验质量管理规范(GCP)的新指南。
指南指出,ATMP 是可能会对临床试验的设计和执行提出特定挑战的复杂和创新产品。例如,制造方面的限制和产品的短保质期可能会要求对...
|
|
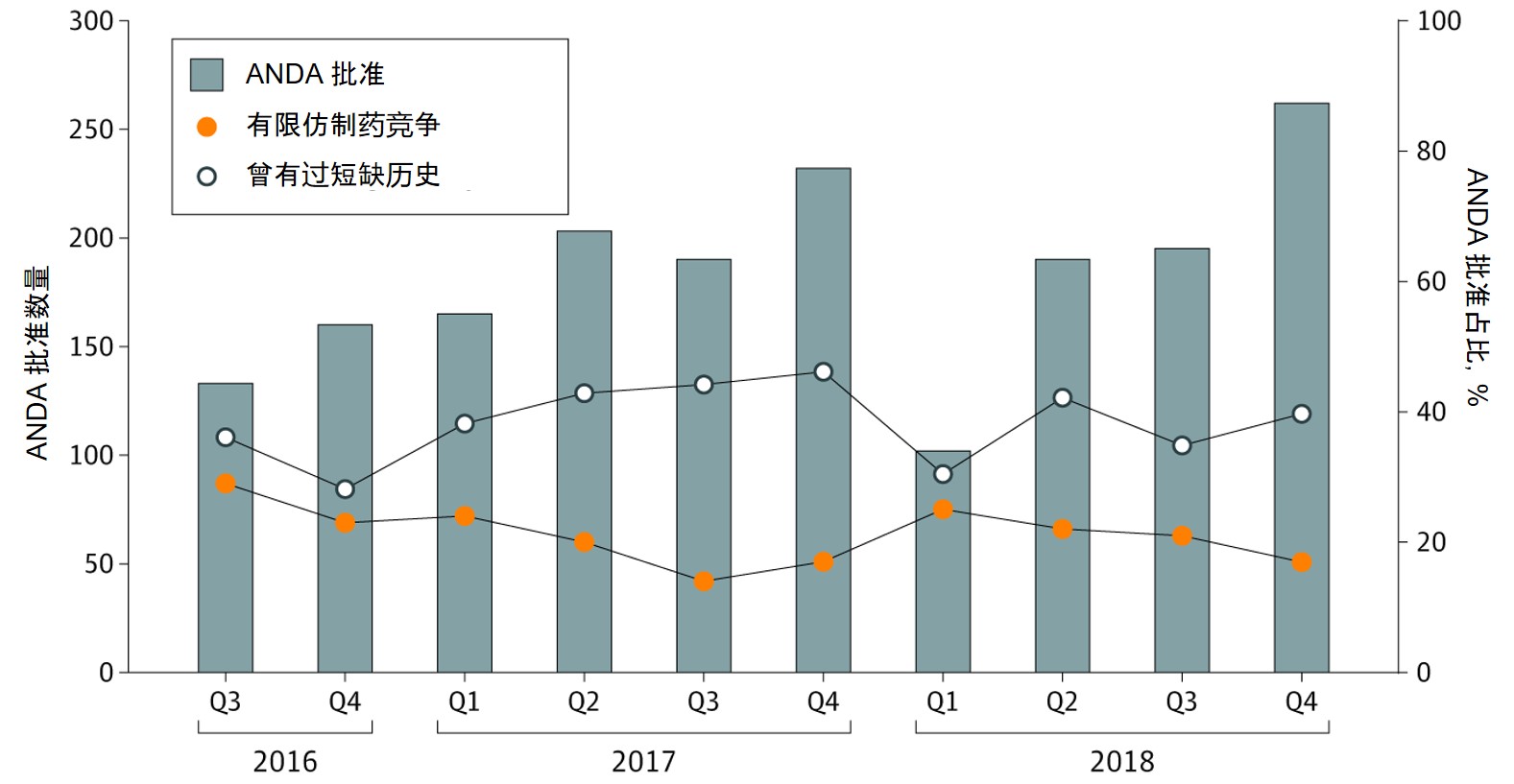
FDA 促进仿制药竞争政策的效果如何?言之过早
2019.10.15
10 月 11 日发表在美国医学会杂志(JAMA)Network Open 上的一篇文章指出,美国 FDA 增加简化新药申请(ANDA)审批的政策对于促进缺乏竞争和易发短缺领域的仿制药发展方面尚未产生明显效果。
FDA 自 2017 年以来采取了一系列行动,包括发布药品竞争行动计划,落实《FDA 重授...
|

|
2019 IPEM 年会(二轮通知)
2019.10.12
合理监管 Regulate Sensibly ,科学研发 Develop Scientifically ,高效生产 Manufacture Competitively ,尽责管理 Manage Responsibly
大家好,
与首轮通知相比,会议第二天上午提早半小时开始,下午取消了一次间歇,目的是增加报告和问答讨论时间。在拿到Marten Ritz和Bla...
|

|
FDA 三大中心主任讨论:药品批准标准是否过于宽松?
2019.10.11
从行业到学术界很多批评者都认为美国 FDA 的药品批准标准正在不适当地变低,并且所要求的批准后评估要么不充分,要么已被取消。但在 10 月 7 日在预见政策(Prevision Policy)和癌症研究之友(Friends of Cancer Research)主办的第五届生物制药大会上,三位 FDA 主任提出了反对...
|

|
WHO 发布 2019 抗生素分类数据库加大力度应对耐药...
2019.10.09
世界卫生组织(WHO)于 10 月 1 日宣布已上线最新版本的 AWaRe 抗生素分类数据库,该数据库是一种管理工具,供各国政府在制定有关处方和监测抗生素政策时使用。
WHO 表示,该数据库不仅可以被政策制定者用来“支持制定绩效目标并指导各国对抗生素的最佳使用”,还可以被临床医生...
|
|
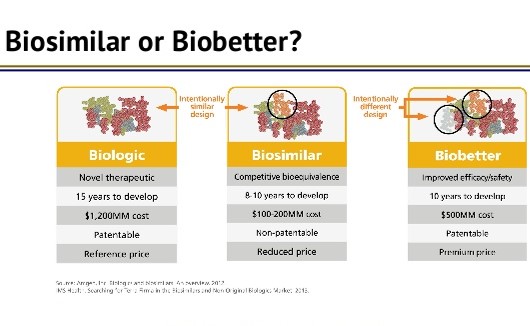
FDA 药品中心主任关注 biobetter,乐观看待生物类似...
2019.10.05
美国 FDA 药品审评与研究中心(CDER)主任 Janet Woodcock 于 9 月 23 日在药物信息协会(DIA)生物类似药会议上发表演讲,对美国生物类似药市场的未来表达了总体乐观的态度,但同时也惋惜地指出《生物制品价格竞争和创新法案》(BPCIA)缺乏“biobetter”路径。
Woodcock 表示,...
|

|
FDA 重要更新:ANDA 行动函转为仅电子邮件发送
2019.10.03
美国 FDA 于 10 月 1 日通过邮件通知表示,从本月起,拥有安全电子邮件账户的简化新药申请(ANDA)申请人将仅通过安全电子通讯收到行动函(包括:批准、暂时品准、完全回应函),因为 FDA,包括仿制药办公室(OGD)在内正在持续努力摆脱纸质通讯。
为帮助确保及时收到 FDA OGD...
|

|
FDA 发布系列数字医疗指南澄清重点监管和放权领域
2019.10.01
美国 FDA 于9 月 26 日发布了一系列指南,旨在持续鼓励数字医疗工具的创新方法开发,并确保 FDA 监管这些技术的方法与时俱进。这些指南目的是在加速实验和对人工智能和数字医疗产品投资的同时,在确保安全和支持创新之间寻求微妙的平衡。
这些发布的指南是 FDA “数字医疗创新...
|

|
FDA 新药办公室改组方案获批,将于 2020 年初全面...
2019.09.28
美国 FDA 于 9 月 26 日宣布,国会已经批准了机构改组计划,该计划将把新药办公室(OND)转变为以疾病治疗领域为中心的结构。新组织架构预计将于 2020 年初全面实施。
OND 将把办公室数量从 6 个增加到 8 个,并将其临床部门从 19 个增加到 27 个。还将增加 6 个非...
|