
|
科学家批评印度在缺乏有效性数据的情况下匆忙批准新冠...
2021.01.08
《科学》(Science)杂志网站近日发文指出,印度药品监管机构在没有等待确定的有效性和安全性 III 期试验结果的情况下,于 1 月 3 日授权了印度 Bharat Biotech 公司开发的新冠(COVID-19)疫苗 Covaxin,这一行动引发了一些科学家和患者倡导组织的严厉批评。
在周日的新闻...
|

|
英国和印度或于下周批准阿斯利康新冠疫苗
2020.12.24
印度很可能在下周批准牛津/阿斯利康的新冠(COVID-19)疫苗用于紧急使用,可能成为第一个为阿斯利康疫苗提供监管许可的国家。而英国紧急情况科学顾问小组成员本周三也表示英国政府可能会在圣诞节之后授权阿斯利康疫苗。
据路透社报道,印度作为世界上最大的疫苗生产国,希望在下个月...
|

|
印度新冠疫苗试验不良反应引发质疑,辉瑞疫苗需要在印...
2020.12.22
印度药品管理总局(DCGI)可能会要求辉瑞/BioNTech 寻求在印度的加速批准(类似于紧急使用授权)之前进行本地临床试验。
这可能是辉瑞/BioNTech 在全球批准道路上遇到的第一个关卡。在 12 月 9 日 DCGI 的专家委员会上,辉瑞印度公司曾希望有更多时间做介绍。在那之后,辉瑞...
|
|
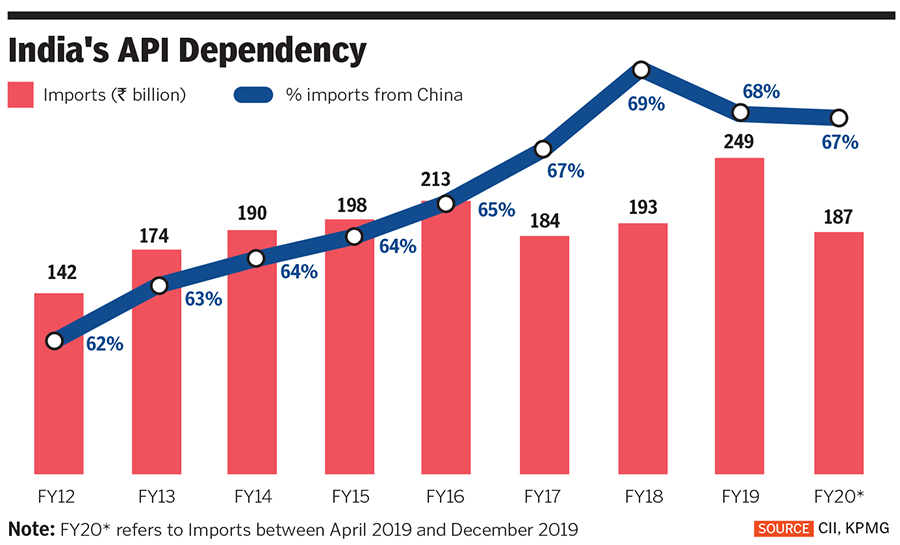
印度制药业反思对中国的依赖,希冀重获全球 API 主...
2020.09.07
一场疫情改变了整个世界的形势,也让潜藏的矛盾迅速浮出水面。全球对供应链,尤其是事关生命健康的医药产品供应链的关注日益增加,印度也不例外。在大势所趋之下,知己知彼、未雨绸缪才能做到因势利导、适时调整、合理应对。
近日,福布斯印度网站上刊发了一篇特别报告,详细介绍了印...
|

|
印度药企呼吁 FDA 在疫情期间执行虚拟现场检查
2020.05.06
作为全球最大的药品出口国之一的印度正受到新型冠状病毒疫情的沉重打击,原因是全球旅行限制使得药厂日常运行复杂化,其中一个原因就是,FDA 对国外检查已暂停将近两个月,并且没有丝毫的恢复迹象。印度药企正在努力寻找解决方案,希望 FDA 在疫情期间对生产场地执行虚拟检查。
根据...
|

|
印度加大力度降低对中国原料药的依赖,禁止羟氯喹出口
2020.03.28
最近印度有两条消息值得制药业加以关注。
首先,印度商务部对外贸易总局于 3 月 25 日发布通知,禁止将任何羟氯喹药物和制剂运出国外,必须履行现有合同的公司以及出于人道主义理由必须由外交事务部逐案批准的公司除外。
其次,印度政府为确保长期药物安全已拨款 13.2 亿美元促...
|

|
美国印度开展双边执法行动查处非法药品快递
2020.02.20
2月18日美国 FDA 宣布了与印度政府于 1 月份开展的首次双边执法行动,这次行动阻止了约 500 批次非法的、潜在危险的、未经批准的处方药和组合器械运抵美国。
FDA 局长 Stephen Hahn 表示,“由于每个国家/地区的标准和法规不尽相同,美国消费者在从未经授权的国外来源订购药品...
|
|
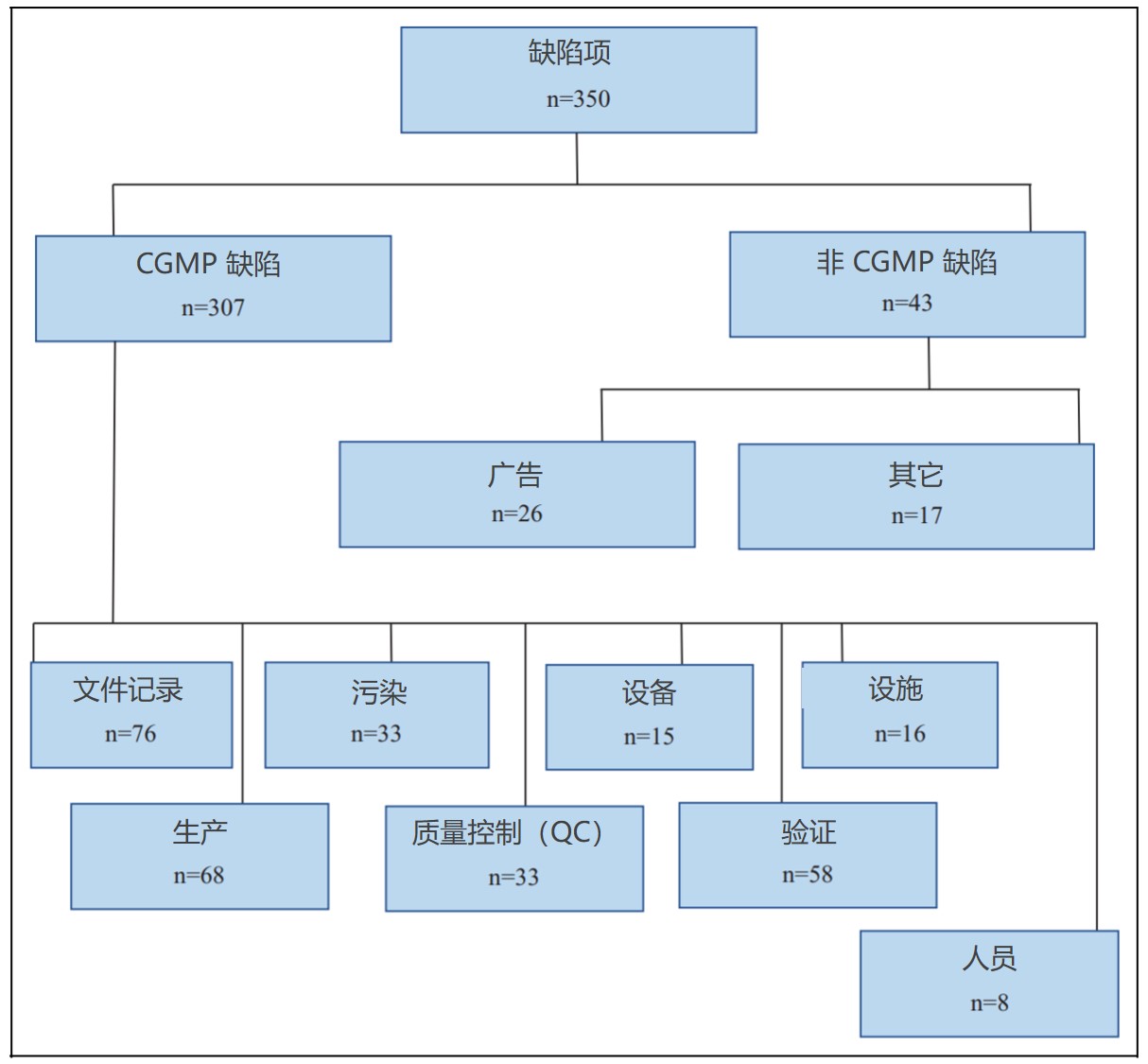
美国 FDA 向印度制药与器械企业发布的警告信分析
2019.11.21
在过去 14 年内,FDA 向印度制药和器械企业发出的警告信数量逐渐增多。在警告信列出的所有违规行为中,85.87% 与 CGMP 不合规有关。此外,在这些警告信中有 80.72% 在之后没有关闭函。
这一回顾性研究于 11 月 5 日发布于 DIA 《治疗创新与监管科学杂志》上,分析回顾了 20...
|

|
印度药业反击质量问题指责,兰伯西揭发者尖锐回应
2019.08.02
关于印度制药业数据可靠性和质量管理的问题,我们经常看到的是监管机构的视角,现在我们换个角度,从当事人的视角来看看,本文摘选整理了印度 Biocon 药业掌门人 Kiran Mazumdar Shaw 发表在印度媒体上的公开言论,以及原兰伯西(Ranbaxy)高级管理层、Ranbaxy 案件的揭发者 Dinesh ...
|

|
数据可靠性危机导致 Apotex 撤销 31 件已获批 AND...
2019.07.11
加拿大制药商 Apotex 公司因其在印度班加罗尔的两家工厂持续存在数据可靠性和质量部门失效问题,而要求撤销美国的 31 个获批仿制药申请。美国 FDA 于 7 月 10 日在联邦公报上发布撤销通告,并列出具体撤销名单。
Apotex 公司撤销仿制药申请的决定是近年来数据可靠性危机所...
|

|
印度太阳药业鼓励员工检举的新政策:说一套做一套?
2019.05.13
世界最大的仿制药供应商之一 — 印度太阳药业(Sun Pharma)于 4 月 17 日发布了一封内部电子邮件,鼓励员工检举包括内部交易在内的不当行为。但结合之前发生在该公司的内幕交易指控和解案,公司似乎在采用说一套做一套的双重标准。
首先,整个故事要从一件内幕交易指控说起。该...
|
|
印度仿制药获 FDA 批准数据一瞥
2019.05.08
昨日印度时报(the Times of India)商业版上刊登的一篇短小文章颇为有意思,或许能帮助大家从另一个角度更深入地了解仿制药业目前的形势,因为大家并不经常能看到这些统计数据。文章概述了印度制药公司获得的批准数量以及警告信数量。
印度时报文章中的数据是基于财政年度(请注意...
|

|
印度 CRO Semler 就数据可靠性问题起诉 FDA 后续:...
2018.12.01
今年1月份识林曾发布资讯,印度合同研究机构(CRO)Semler 研究中心因美国 FDA 公开“莫须有的”数据欺诈问题破坏了其声誉并造成其业务损失而起诉 FDA。1 日前,FDA 对于该起诉做出回应表示,该诉讼应被驳回,因为诉讼可能破坏 FDA 的公共卫生使命和《联邦食品、药品和化妆品法案...
|

|
印度仿制药目标:从全球领跑者到全球主导者
2018.06.10
在截止于 2017 年 9 月 30 日的 2017 财年中,美国 FDA 批准了创纪录的仿制药,其中印度公司占据了所有批准的近 40%。虽然 FDA 的报告没有给出按申请人所属国家计数的详细信息,但一份按申请人所属国家计数的月度仿制药批准行业分析报告表明,在获批的总共 763 件 ANDA 中...
|
|
亚洲监管综述:印度限制使用进口器械
2018.03.23
本综述的重点在于印度制定分组器械申请指南,马来西亚为器械制造商制定监管途径。
印度限制公共项目使用进口医疗器械
印度制药部门(DoP)正在计划限制公共项目从外国制造商获得医疗器械的比例。DoP建议建立在去年发布的更广泛的文件上,以促进“印度制造”活动。
2017年的文...
|
|
印度 CRO Semler 就数据可靠性问题起诉美国 FDA
2018.01.25
印度合同研究机构(CRO) Semler 研究中心(SRC)于 1 月 22 日在美国加利福尼亚中区地区法院提交起诉书,起诉美国 FDA 公开 CRO 称之为莫须有的关于数据欺诈的声明的决定,破坏了其声誉并损害了其业务。Semler 在起诉中称,由于 FDA 2016 年 4 月关于申办人必须对于他们...
|

|
印度继续在 2017 美国首仿药批准清单中占据显著地位
2018.01.09
印度公司在 2017 年美国 FDA 批准的首仿药中占了四分之一以上。批准包括一些有限竞争的药品和复杂产品,部分反映了小型和大型印度公司正在将其投资组合向着这些有着很大渗透空间和更多利润的投资组合调整。
“首仿药”代表 FDA 首次批准允许制造商在美国市场上销售一款仿制药 —...
|

|
印度希望结束对中国原料药依赖的政策草案仍待改进
2017.09.27
【编者按】近年来印度政府一直在寻求降低对中国原料药进口的重度依赖,设法鼓励印度本土制药业生产 API。虽然目前看来这些政策的成效不大,但是作为中国原料药企业是否也是时候认真考虑未来发展和转型了?
印度提出一项政策提案草案,终止印度的仿制药行业对中国大宗药物进口的依赖,...
|

|
FDA近年来对印度BA BE研究检查大幅增加
2017.06.26
2002 年美国 FDA 没有在印度对仿制药申请执行任何生物利用度(BA)或生物等效性(BE)研究检查。而十几年后,几乎一半的 FDA BA/BE 研究检查在印度开展。检查数量的急剧上升导致重大数据质量问题的大幅上升,这是 6 月 19 日 DIA 年会教育分会的关注点。会议召集了三名 FDA...
|

|
FDA在印度 – 捍卫质量文化
2017.03.30
【编者按】在FDA的重压下,过去几年印度药业和药监在质量问题上有明显的态度转变。至于是否真正在质量管理上痛改前非了,难说。至少在对外宣传上态度积极,且有效果,例如FDA刚刚撤销的对Ranbaxy的进口禁令。印度这方面的经验教训也许值得借鉴。
(译自FDA Voice “https//blogs.fda....
|