
|
国内药政每周导读:医保局促进创新药,电子申报和 eCT...
2025.07.07
【早期开发与临床】
6.30,【CDE】关于再次公开征求《多联疫苗临床研究技术指导原则(征求意见稿)》意见的通知
7.2,【CDE】关于发布《抗 HIV 感染药物临床耐药性研究及数据递交指导原则》的通告(2025年第23号)
【药学研究】
7.1,【CDE】关于公开征求《细胞治疗药...
|

|
【周末杂谈】创新药专利滥用的恶化
2025.07.06
单个药品就可拥有上百项专利的保护,让专利挑战愈加不易
时任FDA代理局长Janet Woodcock医师曾于2021年致函美国专利局Andrew Hirshfeld局长,建议联手遏制专利滥用、鼓励竞争。信中罗列了“专利丛林”、“专利长青”及“产品跳转”等创新药公司常见滥用专利的手段,及FDA对此的关注。 ...
|

|
【轻松一刻】原来我就是质量文化
2025.07.05
识林轻松一刻,意在以漫画形式,展现药企人酸甜苦辣,博得识林读者会心一笑之余,也希望带来些许回味与思索。
识林欢迎读者提供素材,可以是几段对话,也可以是一个故事。有合适的,识林会与您联系,一起优化完善,并由我们的设计师转化为漫画,在识林平台上分享给大家。
识林...
|

|
【招聘】识林求贤 共建药业 AI 应用的新生态
2025.07.05
大语言模型(Deepseek, ChatGPT)为代表的AI工具,为识林十五年来建立的结构化药业知识库融合大语言模型的AI赋能应用带来了潜力。识林正在探索构建“AI赋能 + 知识工程”的企业级AI应用生态,并已有优化效果,提升效率的落地案例:
基于全生命周期、动态更新的权威知识库,支持法...
|

|
EFPIA 调研2024全球官方检查,看 PICS 和各国境外...
2025.07.04
6月10日,欧洲制药工业协会联合会(EFPIA)发布了《2024年度监管 GMP/GDP 检查调查数据》,汇总了27家全球创新型制药企业及两家国家贸易协会提供的数据。
报告显示,全球药品生产监管检查正逐步从疫情期间的远程模式回归传统现场检查,实时远程检查在疫情后逐年减少,但整体检查数...
|
|
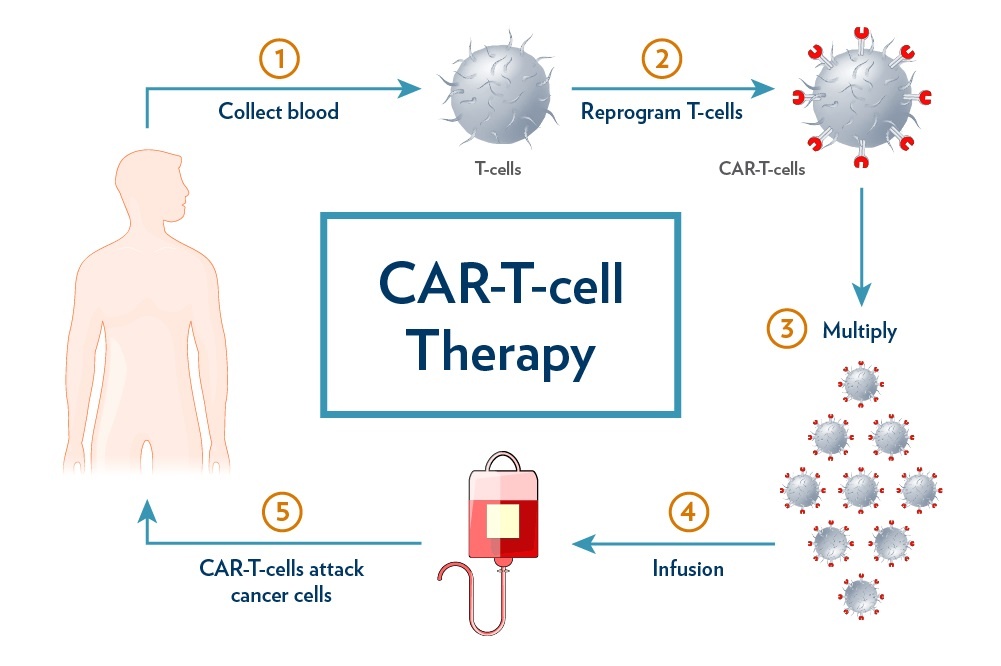
FDA 取消自体 CAR-T 细胞免疫疗法的 REMS 要求
2025.07.04
6月26日,FDA发布安全通讯,取消目前获批的BCMA和CD19靶向自体嵌合抗原受体T细胞(CAR-T)免疫疗法的风险评估与减轻策略(REMS)。
REMS是FDA的一种安全计划。FDA可以要求某些具有严重安全问题的药物实施REMS,以确保药物的获益超过其风险。此前,由于自体CAR-T细胞免疫疗法复杂的...
|

|
FDA 临床药理学办公室2024年报,公开审评总结及大量...
2025.07.03
6月13日,FDA发布了《临床药理学办公室2024年度报告》。该报告详细展示了临床药理学办公室(Office of Clinical Pharmacology,OCP)在过去一年中在药物监管、临床药理学研究以及推动创新药物开发等方面的工作成果与进展。对于我国监管与药企,OCP的大量研究文献具有独特的参考价值。
...
|
|
FDA 肿瘤卓越中心2024年报,丰富工具促进前沿创新
2025.07.03
6月25日,FDA肿瘤卓越中心(Oncology Center of Excellence,OCE)发布2024年报,显示其在肿瘤药品及生物制品的监管审评与推动肿瘤治疗领域发展方面的成果。
OCE监管的肿瘤领域是一直以来的药物开发热点。从其年报即可看出,OCE在曾见证信达礼来PD-1折戟的Pazdur领导下相当活跃,...
|

|
FDA 定稿远程监管评估问答指南,不是检查但需早做准...
2025.07.02
6月26日,FDA定稿了《进行远程监管评估 - 问答》指南,共计16个问答,为制药行业及其他受FDA监管的行业提供关于远程监管评估(Remote Regulatory Assessment,RRA)的明确指导。该指南曾于2022年7月和2024年1月两次征求意见。相比上次征求意见,定稿指南没有显著修订。
RRA是源...
|

|
独立调查报告揭示印度产伪劣抗癌药物被销往全球超百个...
2025.07.02
6月25日,由盖茨基金会资助的独立调查新闻社(The Bureau of Investigative Journalism,TBIJ)发布报告,披露了一起令大众震惊而令研究人员“心碎”(heartbreaking)的全球性药品质量问题。报告显示,多个关键化疗仿制药未能通过质量检测,可能致使全球超100个国家的癌症患者面临...
|

|
国际药政每周概要:ICH E20 临床适应性设计,FDA ...
2025.07.02
【早期开发与临床】
6.24,【FDA】以游走性红斑为表现的早期莱姆病:开发治疗药物
6.25,【MHRA】药物临床试验:通知类(notifiable)临床试验
6.25,【ICH】E20 临床试验适应性设计
6.26,【FDA】存在未满足医疗需求的严重细菌性疾病患者的抗菌治疗 - 问答
【生产质量】...
|

|
BIO 2025上的不确定性:监管变革,药价承压和资源削...
2025.07.01
2025年6月16日至19日,生物技术创新组织(BIO)在波士顿迎举办2025年度BIO国际大会(BIO International Convention)。大会为期四天,涵盖超过180场会议和1100名演讲者,涉及20个重点领域,包括人工智能和数字健康、下一代生物治疗、商业发展等。参与者包括领先的生物技术公司、投资者...
|
|
不赚钱也得有路可走,Woodcock 谈仿制药老药新用监管...
2025.07.01
近日,Duke Margolis健康政策研究所举办了一场研讨会,来自非营利组织(NPO)人员以及一位业界十分熟悉且广受尊敬的前FDA高官Janet Woodcock齐聚一堂,共同探讨了如何激励NPO基于现有仿制药开发老药新用(repurposing)。
与会者称,尽管目前有4000种疾病已经有相应的治疗药物,但仍有1...
|

|
不决策,人工去幻觉,离线缺训练:FDA 的 Elsa 仍...
2025.06.30
6月份,在DIA年会,FDA首席AI官Jeremy Walsh和数据科学与AI政策副主任Tala Fakhouri均谈及了刚刚在6月初发布的FDA内部AI工具Elsa,对业界的诸多疑问进行了不同程度的回应。近期发布的一篇针对AI用于审评的FDA研究文献也提供了一些参考信息。但Elsa的面目对于业界来说仍不明朗。此外,FD...
|

|
专家会5:4投票反对,FDA 批准膀胱癌新药 Zusduri
2025.06.30
6月12日,FDA批准了UroGen Pharma公司的丝裂霉素膀胱内灌注液产品Zusduri,用于治疗复发性低级别中危非肌层浸润性膀胱癌(LG-IR-NMIBC)成人患者。而在一个月前,肿瘤药专家咨询委员会以54的投票结果反对该药的批准。
Zusduri是一种改良剂型的丝裂霉素产品,通过水凝胶技术实现更...
|

|
国内药政每周导读:医保法征求意见
2025.06.30
【监管综合】
6.27,【国家医疗保障局】医疗保障法(草案)征求意见
【新药批准和报产】
6.23-6.29,NMPA未发布新药批准,CDE受理4个新药上市申请
【监管综合】
6.27,【国家医疗保障局】医疗保障法(草案)征求意见
在中华人民共和国境内从事医疗保障相关的...
|

|
【周末杂谈】FDA 的监管信息化,总算要做点实事了?
2025.06.29
参众两院两党联合提案,授权FDA信息化监管标签和说明书
本专栏已有一段时间不怎么谈及美国FDA了,因为实在是觉得没啥可说的。待FDA内部整顿完毕,明确了下一步的监管政策,且若有值得国内药企或药监关注的内容,再讨论不迟。
今天讨论的事,不是出于FDA自身的所作所为(至少表面上不是...
|

|
FDA 延长亚硝胺相关杂质限度实施提交期限
2025.06.27
6月23日,FDA在其“亚硝胺杂质可接受摄入量限度”页面上发布消息,鉴于药企在应对亚硝胺药物成分相关杂质(NDSRIs)限度实施工作时面临挑战,决定延长提交的期限,为药企提供了更充裕的时间来完善相关限度实施与控制策略。
亚硝胺类杂质问题最早可追溯至2018年,当时在缬沙坦(valsart...
|

|
2024财年 GDUFA 报告:856个 ANDA 获批,解除警告信...
2025.06.27
6月13日,FDA发布了《2024财年 GDUFA 绩效报告》(GDUFA,仿制药使用者付费修正案),详细展示上个财年仿制药审批及相关领域的工作成果。
出于对GDUFA收取费用的承诺,FDA每年都要发布绩效报告,以向立法者和业界证明费用收支的合理性。报告中有关批准数据、审评审批时限达成率以及...
|

|
线上讲座:FDA 近期趋势对中国药业的影响——人员机...
2025.06.26
FDA近期的系列变化对中国药业有重大影响。例如,FDA正在大力推动制药回归美国,同时加紧对海外工厂的监管力度。5月5日,FDA美国总统特朗普签署了要求 FDA “内松外紧”的“促进国内关键药品生产的监管减负”(Regulatory Relief to Promote Domestic Production of Critical Medicin...
|