
|
IPEM 课程 无菌污染控制:从表面到空气污染防控的设...
2026.05.07
无菌污染控制:从表面到空气污染防控的设计、验证和运行维护
授课老师:Ian Thrussell、James Drinkwater
上课日期:5月21-24日(周四 - 周日)
授课方式:中英交传
上课地点:上海
老师简介
Ian Thrussell,曾任世界卫生组织GMP和无菌药品检查专家,首席检查员。20...
|

|
2026年度 FDA 仿制药论坛简报
2026.05.07
4月22-23日,FDA召开了一年一度的仿制药论坛(GDF)。
仿制药办公室(OGD)副主任Darby Kozak称2025财年FDA批准或暂时批准了939个仿制药申请(ANDA),其中包括125个复杂仿制药、92个首仿药和107个竞争性仿制药疗法(CGT)。这一数字高于2024年的900个ANDA批准量(包含92个复杂仿制药...
|

|
FDA 试点“一日检查”AI 挑选的低风险设施
2026.05.07
FDA于5月6日宣布启动一日检查评估试点(One-Day Inspectional Assessments),识林此前报道过试点已经开始。据FDA透露,截至4月底其已完成46次一日检查,大多数结果为"无行动指示"(NAI)。FDA表示试点将在2026财年持续运行,跨越多个项目领域,包括人类和动物食品、生物制品、医疗...
|
|
FDA 公开的已批准药品的283封完全回应函缺陷分析
2026.05.06
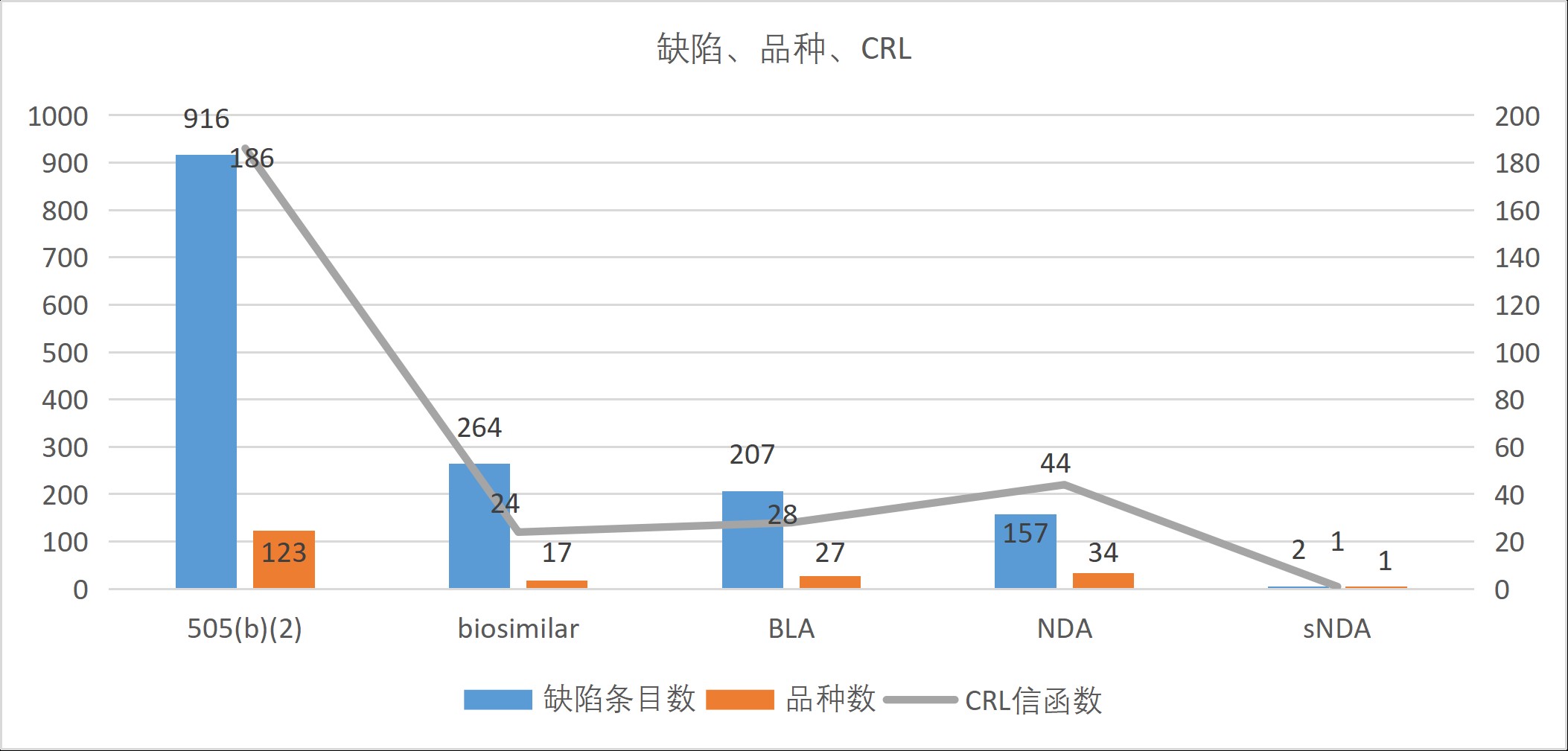
自宣称将公开完全回应函(CRL)之后,FDA首批试探性公开了一批已批准药品的CRL,共有202份PDF文档(截至2026年4月30日,已公开了216份PDF文档)。经过对这一数据包的分析,识林提取药品申请编号以及对应的缺陷内容,统计得到202个品种,涉及283封CRL信函,合计产生1,546条缺陷条目。
基...
|
|
CGT 儿科研究两难:成人数据非必须但风险高企
2026.05.06
4月9日,FDA与再生医学联盟联合举办专题研讨会,探讨细胞和基因治疗(CGT)儿科患者临床试验的科学和伦理复杂性。研讨会揭示了两难处境:对于某些仅在儿童中发病的遗传疾病,FDA并不强求必须先有成人数据才能启动儿童研究,但让儿童——尤其是无症状儿童——成为首批临床试验受试者,仍...
|

|
CNPV “超速”审批附带更多上市后研究要求
2026.05.05
FDA似乎倾向于对“局长国家优先审评券”(CNPV)“超速”批准的产品提出额外的上市后安全研究要求。以业界广泛关注的GLP-1药物为例。礼来的Foundayo(orforglipron,奥氟格列隆)是CNPV计划下批准的第一个新分子实体,审批仅耗时50天。FDA近日公开了其审评卷宗(识林会员可至“药品数据...
|

|
国内药政每周导读:生物医学新技术的界定与审批,临床...
2026.05.04
【非临床和临床研究】
4.28,【CDE】关于公开征求《硼中子俘获治疗药物临床研发技术指导原则(征求意见稿)》意见的通知
4.29,【CDE】关于公开征求《药物临床试验生物样品分析实验室合规性回顾报告(征求意见稿)》意见的通知
4.30,【海南局】关于印发《乐城先行区临床真...
|
|
欧盟法院里程碑式裁决打通“化仿生”路径
2026.05.04
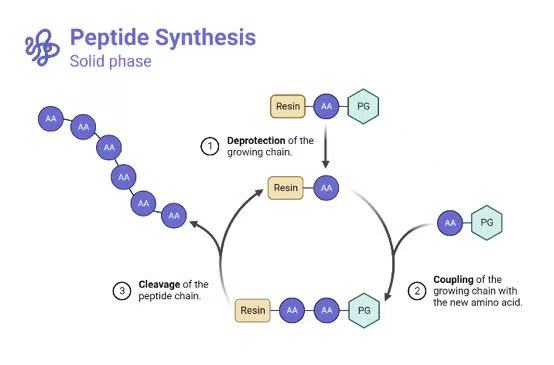
4月23日,欧盟法院(CJEU)作出里程碑式裁决,以生物制品为对照药品的化学合成多肽药物可以通过简化的仿制药途径获得批准(“化仿生”)。这一裁决打破了欧盟多肽药物监管的模糊局面,可能重塑介于小分子和生物药之间的多肽药物欧洲市场格局。
法院明确,2001/83/EC指令第10条并不阻...
|

|
三图庆五一
2026.05.03
作者:识林-榆木疙瘩
识林®版权所有,未经许可不得转载。
...
|

|
【轻松一刻】带幻觉的 AI 并非真正风险
2026.05.02
*改编自GMP专家Ian Thrussell分享的素材。
AI为什么会有幻觉?
AI不懂,只是一味地猜。
它选最“靠近”的词,不是最靠谱的话。
文字有空,它就填。
数据有缺,它就编。
它没有“不知道”这个选项——
宁可胡说,绝不沉默。
其实,我们也有份
我们...
|

|
美待定法案禁止 IND 采用中国临床数据
2026.05.01
*识林读者和会员五一节日快乐!识林将在假期保持每日一篇更新。
4月29日,美国国会众议院拨款委员会在FDA相关的联邦支出法案报告中添加条款,禁止FDA"接受、审评或考虑"来自中国、俄罗斯、伊朗或朝鲜的临床试验数据。该禁令明确适用于新药临床试验申请(IND)。
委员会在报告中...
|

|
AI 加持下,FDA 试点“实时临床试验”
2026.04.30
4月28日,FDA宣布实施"实时临床试验"(Real-Time Clinical Trials,RTCT)试点,基于其已开展的两个概念验证临床试验,计划于今年夏天启动更大范围的RTCT试点项目。
简言之,FDA设想的RTCT是利用AI和电子健康记录技术的进步,将临床试验中原本需要人工从试验记录中提取、手动录...
|

|
FDA 强令 Tavneos 撤市,严厉指控药企操纵临床数据
2026.04.30
4月27日,FDA在一封信函中严厉指控ChemoCentryx(现为安进Amgen旗下公司)操纵了Tavneos(阿伐可泮)的关键临床试验数据,并要求安进将该药撤出市场。安进再次明确拒绝撤市,使其与监管机构陷入罕见的高风险对峙。
Tavneos用于治疗活动性抗中性粒细胞胞浆抗体(ANCA)相关性血管炎,...
|

|
英国落地临床试验全面改革,聚焦 FIH 启动速度
2026.04.29
4月28日,备受期待的英国临床试验新法规正式生效。其被视为该国二十多年来最重要的临床试验法规全面修订,引入了全新的试验审批和监管方法。
英国药品和健康产品管理局(MHRA)在公告中指出,将加速评估首次人体试验(First in Human,FIH),并引入“可通知试验”(notifiable tri...
|

|
FDA 年报显示药企稳定履行 PMR 和 PMC
2026.04.29
4月24日,FDA发布《2024财年药品和生物制品公司在执行上市后要求和承诺方面的绩效报告》。报告显示药企对于上市后要求和承诺(PMR/PMC)的履行情况整体良好可控。
PMR是根据法规要求必须开展的研究或临床试验,而PMC是申请人自愿承诺且书面同意开展的研究或临床试验。临床试验成本高...
|

|
GMP 环境中用 AI:案例分析与合规范式转变
2026.04.28
近日,路易斯安那大学拉法叶分校的研究者发表文章《制药中的人工智能:应用、案例研究及 GxP 实施考量》,综述了AI在药品制造领域应用的最新进展,包括8个案例分析以及在应对GMP合规挑战方面的洞见,可为我国药企在生产线上合规且高效地应用AI提供参考。
站在药企角度,研究者指出...
|

|
FDA 合规办公室年报:警告信激增至314封,主因并非生...
2026.04.28
4月23日,FDA合规办公室(OC)发布《2025年合规办公室年度报告》(本该去年发布的2024年报被跳过),概述了该办公室在药品生产设施合规监管、临床试验监管、生物研究监测等方面的工作成果。报告显示,FDA在2025年的合规行动显著增加,特别是针对未经批准或错标的药品违规行为以及药品掺...
|

|
国际药政每周概要:FDA 总结动物试验减免,合规办公...
2026.04.28
【非临床与临床研究】
4.20,【FDA】减少非临床研究中的动物试验:首年进展与未来之路
4.20,【SFDA】利用真实世界数据(RWD)和真实世界证据(RWE)支持药品上市许可有效性与安全性的框架
【药学研究】
4.24,【WHO】口服速释制剂的生物等效性(征求意见稿)
本周BE指...
|

|
《药品附条件批准上市申请审评审批工作程序》的要点沿...
2026.04.27
4月24日,NMPA定稿了业界瞩目的《药品附条件批准上市申请审评审批工作程序》(“41号文”),取代了2020年7月发布的原版文件(“82号文”)。文件经历过2023年8月和2025年7月两次征求意见,可谓慎重。
另外特别值得一提的是,两份意见稿以及现行版均附带相应的“政策解读”,对正文内...
|

|
再生元终签 MFN 协议,其基因疗法获61天快速批准
2026.04.27
4月23日,再生元(Regeneron)成为第17家与特朗普政府签署最惠国(Most Favored Nation,MFN)药价协议的大型药企,也是收到特朗普邀请的最后一家。
同日FDA批准其基因治疗药物Otarmeni用于OTOF基因相关听力损失的超罕见病,美国每年约有50名新生儿受此影响。这是全球首个用于听力...
|