
|
国际医疗器械监管机构论坛发布医疗器械人工智能和机器...
2024.07.03
国际医疗器械监管机构论坛(IMDRF)于 7 月 1 日发布了医疗器械开发中机器学习质量管理规范指导原则,共包含 10 条指导原则,确保充分了解器械的预期用途和目的,并在产品的整个生命周期内让一系列专家参与评估。
IMDRF 发布的指导原则与美国、英国和加拿大监管机构 2021 ...
|

|
美加英三国发布机器学习医疗器械透明度指导原则
2024.06.17
美国 FDA、加拿大卫生部和英国 MHRA 发布了针对机器学习医疗器械(machine learning-enabled medical devices,MLMD)的指导原则,重点关注与器械交互的利益相关者的信息透明度。
FDA 器械和放射健康中心数字健康卓越中心主任 Troy Tazbaz 在新闻稿中表示,“这些指导原则的...
|

|
机器学习代替动物实验用于临床病理学评估
2023.11.14
2023年11月6日,FDA国家毒理学研究中心Weida Tong等人在nature communication上发表名为《A generative adversarial network model alternative to animal studies for clinical pathology assessment》的文章,旨在讨论利用生成对抗网络(generative adversarial network,...
|

|
美加英三监管机构发布AI ML型医疗器械预定变更控制...
2023.10.27
美国 FDA、加拿大卫生部和英国 MHRA 于 10 月 24 日联合发布了一份指南文件,概述医疗技术开发人员在开发使用预定变更控制计划(predetermined change control plans,PCCP)的人工智能/机器学习(AI/ML)产品时应考虑的原则,为支持 AI/ML 的医疗器械(MLMD)奠定了统一的基础...
|

|
审评范式变革正在路上,FDA研究AI语言模型处理药品说...
2023.08.28
FDA监管文档,包括IND、NDA和BLA中的大量文件,通常需要多学科审评人员关注与其审评领域相关的信息,因此药企提交的申报资料需按特定结构组织信息以方便分配、检索和审评。事实上,监管部门为了解决这个问题,从CTD,eCTD,到近几年的KASA,申报资料的结构化越来越强,信息颗粒度也越来越...
|

|
行业团体呼吁 FDA 采用基于风险的方法监管 AI-ML...
2023.08.14
行业团体和研究人员呼吁美国 FDA 与其他监管机构协调一致,与自己的专家协调,并在考虑在开发中如何透明地使用人工智能和机器学习(AI/ML)工具时采用基于风险的方法。
FDA 于 5 月 10 日发布了题为“在药品和生物制品研发中使用人工智能和机器学习”的讨论文件,就 AI/ML ...
|

|
FDA 收到的含人工智能和机器学习的药品申请数量激增
2023.07.14
美国 FDA 药品审评与研究中心(CDER)定量药理学处处长 Hao Zhu 上个月在 DIA 全球年会上表示,结合人工智能和机器学习(AI/ML)元素的药物申请数量在过去五年内急剧增加。
他表示,2022 年 FDA 收到了 170 件包含 AI/ML 的申报材料。而 2018 年只有 3 份申报内容包含 A...
|

|
FDA 发文讨论在药品研发中使用人工智能和机器学习
2023.05.12
美国 FDA 于 5 月 10 日发布了题为“在药品和生物制品研发中使用人工智能和机器学习”的讨论文件,概述了从药物靶点识别和早期发现工作到上市后监督和先进制造的过程中,如何使用人工智能和机器学习(AI/ML)的关键建议,这是 FDA 试图更好地理解药物开发的两个新的关键组成部分。
...
|

|
辉瑞发力人工智能和机器学习,以期发现变革性药物
2022.12.22
辉瑞正在带头进入通过人工智能和机器学习(AI/ML)来实现药物发现和开发的创新浪潮,公司正在迅速扩大规模并招募人才、开展合作,希望更快地为患者提供变革性药物。
辉瑞表示其愿景包括三个方面:用人工智能揭示疾病生物学;利用这些见解来设计正确的分子;为临床试验的成功确定合适的...
|

|
FDA临床决策支持软件定稿指南解读:进一步退两步,问...
2022.11.03
美国 FDA 于 9 月底发布了一系列于软件、自动化和人工智能相关的指南文件,其中包括一份关于临床决策支持(CDS)软件的定稿指南,10 月 18 日 FDA 举行了一次网络研讨会对该定稿指南提供了更多说明。盛德律所最近发布了对这一指南的解读,下面我们详细来看看。
盛德指出,这...
|

|
FDA 人工智能和机器学习器械标签应如何监管?行业和...
2021.11.20
医疗器械行业团体正在敦促美国 FDA 不要急于对包含人工智能或机器学习(AI/ML)的医疗器械的标签制定新的监管要求,而临床医生团体则希望对器械算法和训练数据集有更高的透明度。
在 FDA 于 10 月中旬举办的关于支持 AI/ML 的医疗器械透明度的网络公开研讨会之后,总共有 15...
|

|
美加英三国联合发布医疗器械开发机器学习质量规范十项...
2021.10.28
美国 FDA、加拿大卫生部(HC)以及英国 MHRA 共同确定了 10 项指导原则,为机器学习质量管理规范(Good Machine Learning Practice,GMLP)的制定提供指导pdf。这些指导原则将有助于推广使用人工智能和机器学习(AI/ML)的安全、有效和高质量的医疗器械。
人工智能和机器学习...
|
|
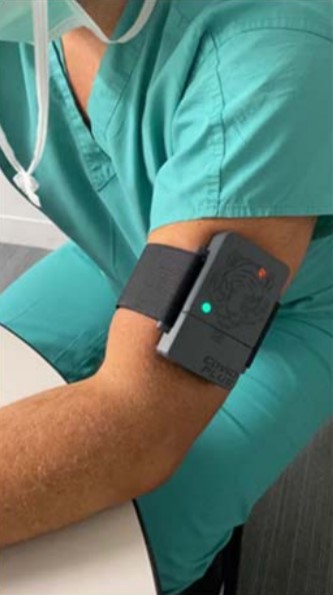
FDA 授权首个基于机器学习的新冠筛查臂带设备
2021.03.23
美国 FDA 于 3 月 19 日对首个基于机器学习的新冠(COVID-19)非诊断性筛查设备“Tiger Tech COVID Plus Monitor”发布了紧急使用授权(EUA),该设备可鉴别指示某些症状类型的生物标志物,例如血液高凝状态(一种导致血液比正常情况更容易凝结的状况)。该设备的设计目的是在...
|
|
丹麦药监局起草 GxP 人工智能和机器学习算法标准
2021.03.16
丹麦药品管理局最近发布了一份问题清单公开征求意见,以定义适用于各种关键 GxP 监管领域(例如,生产、分销和临床试验)的人工智能(AI)/机器学习(ML)算法的标准。丹麦药监局表示,其拟议的标准不是“完整清单”,应被视为“成熟草案”的提案,邀请利益相关者在 4 月 30 日之前...
|

|
FDA 发布首份人工智能和机器学习行动计划
2021.01.13
美国 FDA 于 1 月 12 日发布了首份《基于人工智能/机器学习(AI/ML)的软件作为医疗器械(Software as a Medical Device, SaMD)行动计划》。行动计划介绍了多管齐下的方法,推进 FDA 对基于 AI/ML 的医疗软件的监督。
FDA 医疗器械与放射健康中心(CDRH)数字医疗卓越中心主...
|

|
FDA 研究揭示可用来预测仿制药申报可能性的因素
2020.10.30
美国 FDA 药品审评与研究中心(CDER)研究人员正在研究药物特性、监管行动和经济因素如何影响品牌药是否有仿制药可用。
据估计,在过去十年中,仿制药已为美国节约了约 2.2 万亿美元的医疗费用。【2020 美国仿制药和生物类似药节约报告 2020/10/02】但是许多品牌药产品并未面...
|

|
FDA 现场警示报告预测性分析试点,机器学习助力质量...
2020.04.15
美国 FDA 药品质量办公室(OPQ)下的质量监视办公室最近开展了一项预测性分析(Predictive Analytics)试点,使用现场警示报告(Field Alert Report, FAR)中的信息来衡量药品质量。给那些调查时间短并且能够发现不合格的根本原因的公司打高分,而给那些调查时间长并且无法找到不合...
|
|
FDA 预测机器学习将在药物研发和审评中发挥更加重要...
2020.03.03
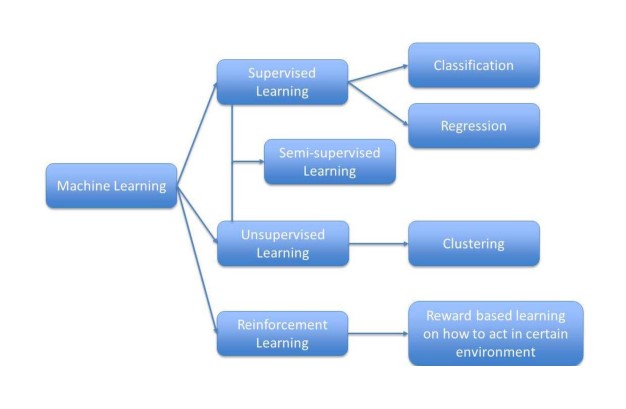
机器学习(machine learning,ML),第一个正式的定义来自卡内基梅隆大学的Tom Mitchell教授,他认为一个计算机程序在完成一项具体任务时,其性能可随着经验的积累而不断自我完善,那么这个程序是在从经验中学习。在过去十年中,由于互联网的发展带动了大量数据的生成, ML几乎为我们...
|

|
FDA 开始构建制药行业研发活动预测工具
2019.06.26
为改善招聘需求、资源分配和使用者付费的计算,美国 FDA 正试图预测整个制药行业的药物开发活动。
FDA 药品审评与研究中心(CDER)计划与战略分析办公室资源能力规划团队主管 Josh Barton 于 6 月 7 日在 FDA 关于使用者付费计划财务管理和透明度的公开会议上表示,使用内部 F...
|

|
FDA 使用机器学习建模预测 ANDA 申报
2019.06.08
美国 FDA 研究人员 4 月 22 日在线发表在《临床药理学和治疗学杂志》上的一篇文章指出,利用药品、监管和药物经济学信息可以准确地预测新化学实体的首个简化新药申请(ANDA)申报的时间。这种建模方法可以帮助 FDA 优化其在仿制药使用者付费(GDUFA)计划下的资源分配和工作量,并...
|