|
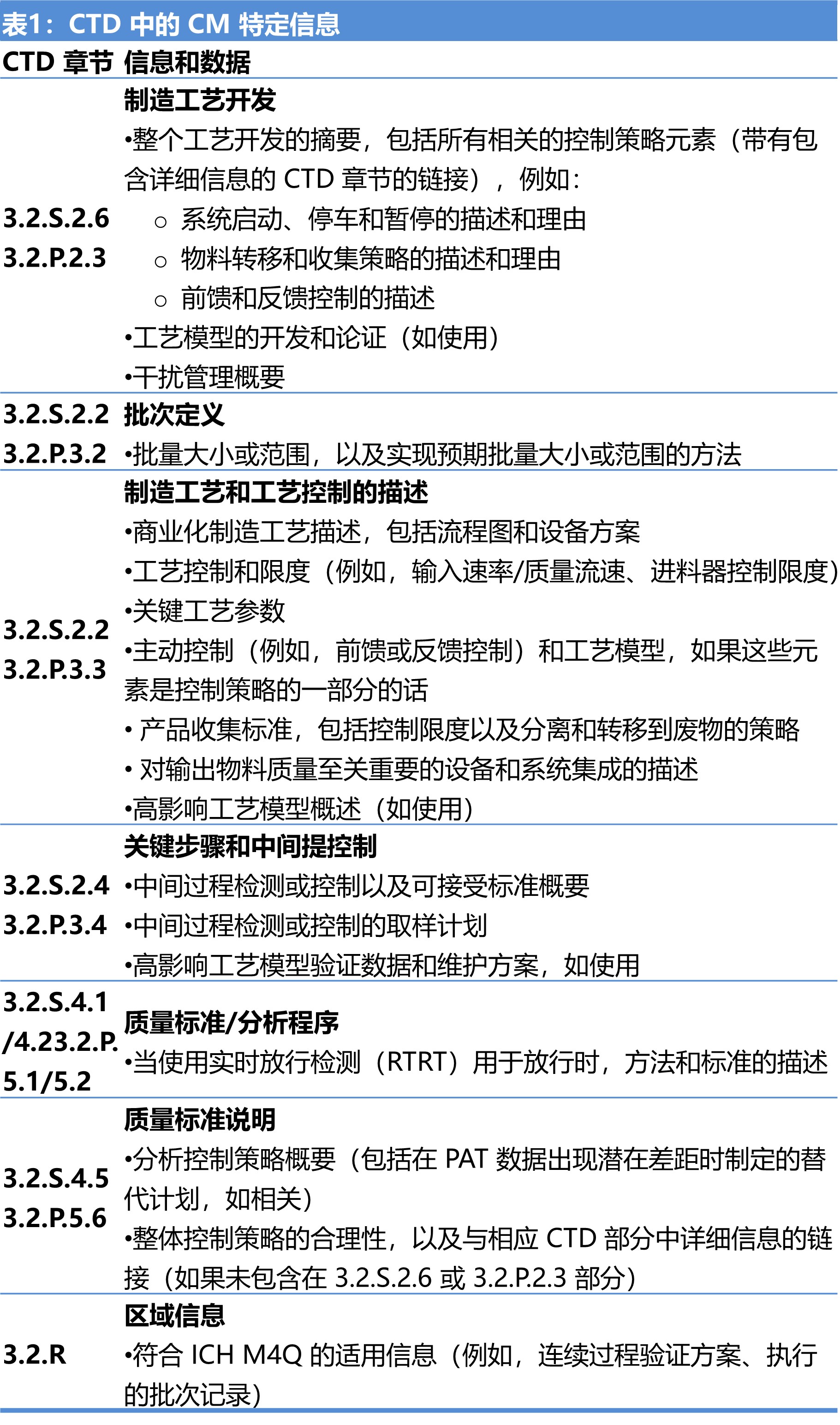
ICH Q13 连续制造指南正式发布
2021.07.29
ICH 于 7 月 27 日正式发布了广受期待的 Q13 《原料药与制剂的连续制造》指南,公开征询意见。指南“描述了连续制造(CM)的开发、实施、操作和生命周期管理的科学和监管考虑因素。”指南还“澄清了 CM 的概念,描述了科学方法,并提出了针对原料药和制剂连续制造的监管考量。”...
|
|
FDA 批准首个可互换生物类似甘精胰岛素产品
2021.07.29
美国 FDA 于 7 月 28 日宣布批准了首个可互换的生物类似药 Mylan 公司的 Semglee(甘精胰岛素-yfgn)。Semglee 与其参照生物药赛诺菲的 Lantus(甘精胰岛素)生物类似且可互换。Semglee 是一种长效人胰岛素类似物,用于改善成人和儿童 1 型糖尿病患者以及成人 2 型糖尿病患者的...
|

|
欧盟发布药械组合产品的质量申报要求定稿指南
2021.07.28
欧洲药品管理局(EMA)最近定稿了有关申办人应在药械组合产品上市许可申请的质量部分提交的信息类型的指南。
该指南将于明年 1 月 1 日生效,重点关注可能对药品质量、安全性和有效性产生影响的医疗器械的产品特定质量方面的信息。指南指定了需要在初始上市许可申请以及后续产品生...
|

|
FDA 开发新免疫分析和动物模型以评估疫苗对新发疾病...
2021.07.28
行业和学术研究人员正在开发针对各种病毒的新疫苗,包括禽流感病毒株(H5N1、H7N7、H7N9、H9N9)、呼吸道合胞病毒(RSV)、埃博拉、寨卡病毒和现在的新冠(SARS-CoV-2)病毒。新型“通用流感疫苗”也在开发中。许多这些疫苗正在与新型佐剂(刺激或增加对疫苗的免疫反应的试剂)一起开发...
|

|
多数临床试验披露情况欠佳,大企业比小企业更透明
2021.07.27
最近一项对临床试验透明度的最新研究发现,2016-2017 两年间,只有 26% 的制药商公开了所有用于获得药物批准的研究结果。67% 的药物在获得 FDA 批准后 6 个月内公布了临床试验结果,但只有 58% 符合《FDA 修正案》的临床试验披露要求。11% 的药物在批准时没有公布任何法...
|
|
从新公布的问答文件看 FDA 似并不准备在亚硝胺合规...
2021.07.27
上周我们报道了有关药业协会要求美国 FDA 修改对亚硝胺的政策,认为当前政策企业负担太重且可能导致关键药物短缺的资讯【三大药业协会呼吁 FDA 修改对亚硝胺的政策,减轻企业负担】,引发了很多读者的共鸣。今天我们通过 FDA 公布的另一份文件来看看 FDA 目前的态度如何。
FDA 于今...
|

|
【一周回顾】2021.07.19-07.25
2021.07.26
药审中心发布风险分析与管理计划撰写指导原则和人纤维蛋白原临床试验技术指导征求意见稿。美国 FDA 发布现场警示报告提交问答定稿指南,公布两份礼来工厂的设施检查报告,FDA 要求取消对妊娠期间使用降胆固醇他汀类药物的最强烈警告。
上周热点资讯:
【周末杂谈】破坏信任的代价...
|

|
【周末杂谈】破坏信任的代价
2021.07.25
临床试验伦理委员会的起因 – 历时40年的塔斯基吉梅毒试验
新冠笼罩中的东京奥运会,有来自全球的1.1万运动员参加,算上各国的教练、工作和随行人员,总数也不过10万人。奥组委不要求他们接种新冠疫苗,但免费提供中国奥委会和辉瑞-BioNTech捐献的疫苗。即使这样,还是有相当数量的...
|

|
三大药业协会呼吁 FDA 修改对亚硝胺的政策,减轻企...
2021.07.24
药物中出现潜在致癌性杂质自 2018 年以来一直是制药行业的一大关注点,也是一大挑战。但一些制药贸易协会对 FDA 监控亚硝胺杂质的新规则感到犹豫,认为这些旨在防止药品中亚硝胺杂质的政策可能导致关键药物短缺。
代表美国仿制药和生物类似药行业的普享药协会(AAM)、代表美国品牌...
|

|
FDA 疫情期间放松数字疗法规定,抑郁症治疗处方应用...
2021.07.23
最近以消费者健康应用程序而闻名的 Happify Health 宣布将利用疫情期间放松的 FDA 法规推出新的处方软件来治疗抑郁症。
Happify 成立于 2012 年,最近宣布已筹集了 7300 万美元加强其在数字治疗领域的工作。随着资金雄厚的公司向监管机构、保险公司和临床医生证明软件可被用...
|

|
FDA 定稿现场警示报告问答指南
2021.07.23
美国 FDA 于 7 月 22 日发布《现场警示报告提交:问题与解答》行业指南,提供了 FDA 目前对新药申请(NDA)和简化新药申请(ANDA)申请人提交现场警示报告(FAR)的要求的最新看法,并概述了 FDA 对 FAR 提交的建议,以帮助提高 FAR 提交的一致性和相关性。
指南定稿了 201...
|

|
国际药品监管机构联盟强调全球药品质量知识管理,增强...
2021.07.22
国际药品监管机构联盟(ICMRA)最近就建立药品质量知识管理系统(PQKMS)起草了联合声明,让公众和行业利益相关者更好地了解联盟为改善全球监管协调和统一所做的努力。
ICMRA 认识到,制药商寻求敏捷性来维持稳健的供应链,并随着设备老化、供应商变更、创新发展和知识获取不断更新制...
|

|
英国和加拿大联合发布指南提高研发期间安全性更新报告...
2021.07.22
英国和加拿大的药品监管机构联合发布了新指南,要求申办人更改在年度定期安全报告,或称为研发期间安全性更新报告(DSUR)中呈现某些信息的方式,以进一步提高临床试验参与者的安全性。
新西兰药品管理局 MedSafe 也同意该指南的建议,并将在对其国家立法进行更改时将指南的内容考虑...
|

|
另辟蹊径:渤健大幅广告积极宣传早期阿尔茨海默病检测
2021.07.21
如何销售因有争议的获益而深陷论战之中的阿尔茨海默病新药?渤健(Biogen)近日给出了答案。
渤健和日本合作伙伴卫材将一对年迈夫妇吉姆和简努力与夺取记忆的病魔做斗争的事例推到了“是时候知道了”主题营销活动的聚光灯下。这一营销活动旨在提醒人们筛查早期阿尔茨海默病症状或轻度认...
|

|
荷兰监管机构因罕见病药物定价过高对制药商处以 2300...
2021.07.21
荷兰反垄断监管机构因一家制药商的罕见病药物多年来“过度”涨价而对其处以 2300 万美元的罚款,成为欧洲监管当局打击制药业价格虚高的最新案例。
荷兰消费者和市场管理局指出 Leadiant 对一种用于治疗罕见遗传代谢疾病 脑腱黄瘤病(CTX)的 CDCA 药物进行了一系列复杂的操作,...
|

|
欧盟、WHO 和各监管机构关注如何确定第二代新冠疫苗...
2021.07.20
欧洲药品管理局(EMA)正在与制药企业对话,以解释在安慰剂对照试验越来越难以进行的情况下,如何确定下一代新冠疫苗的保护效力。EMA 表示,将要求企业执行免疫桥接研究,直到为新冠疾病确定可接受的保护“免疫标志物”,该标志物可用作有效性的替代终点。
EMA 生物健康威胁和疫苗战...
|

|
强生或考虑“两步破产”以解决数十亿美元的婴儿爽身粉...
2021.07.20
根据 7 月 18 日路透社报道,据七名知情人士透露,强生公司正在探索一项计划,将广泛的婴儿爽身粉诉讼中的债务转移到一家新成立的公司,然后该公司将寻求破产保护。
据知情人士表示,在和解讨论中,强生的一名律师告诉原告律师,强生可能会推行破产计划,这可能会导致未事先和解的...
|

|
【一周回顾】2021.07.12-07.18
2021.07.19
药审中心就 ICH S12 基因治疗产品的生物分布研究征求意见。WHO 发布医药产品研究和研发设施的良好实践以及试验用药品 GMP 等多篇指南修订草案,发布人类基因组编辑建议。PIC/S 发布基于风险的变更管理相关的药品质量体系有效性指南以及新冠风险评估指南。识林发布 5-6 月 FDA ...
|

|
PICS 变更管理相关的质量体系有效性评估建议以及现场...
2021.07.19
国际认证合作组织(PIC/S)于 7 月 15 日发布了《关于如何评估/证明药品质量体系在基于风险的变更管理方面的有效性的建议》和《用于国家常规现场检查的新冠风险评估》两份指南,为 GMP 检查员在评估企业与基于风险的变更管理相关的药品质量体系(PQS)的有效性方面以及为在新冠疫...
|

|
【周末杂谈】基因治疗的新希望?
2021.07.18
先天性基因缺陷导致的发育性疾病,出生8-9年后还可以修复
周末杂谈,多是谈政策相关的话题,今天换个新的,基因治疗。这方面笔者是外行,是看热闹,但看热闹有时更有兴致。产品研发是生产力,政策是生产关系,为生产力服务。就像看球,球员是生产力,裁判是生产关系。观众的兴奋点通常...
|