
|
欧洲监察员敦促EMA在临床数据修编方面采取强硬手段
2016.06.21
在为期两年的调查之后,欧洲监察员认为欧洲药品管理局(EMA)不应为了解决临床试验数据披露方面的法律诉讼而允许AbbVie修编其关于Humira药品的某些信息。
监察员Emily O'Reilly建议,EMA官员应对声称某些试验数据是商业机密以争取修编的公司采取更强硬的立场。她发出了严厉提醒,在考...
|

|
FDA发布咀嚼片的质量属性考量要点指南草案
2016.06.20
6月16日,FDA发布《咀嚼片的质量属性考量要点》指南草案,用于指导企业在研发这类产品时应满足的咀嚼片预期特性和FDA需要评估的属性。该指南主要针对新药申请(NDA)、简化新药申请(ANDA)和一些化学、生产和控制(CMC)补充申请。某些对于研发信息递交的建议同样适用于研究用新药申请(IN...
|

|
美国会议员寻求阻止制药商阻碍仿制药竞争
2016.06.19
在不到两年的时间内,美国国会议员第三次提出旨在结束仿制药生产商指控的品牌药品竞争对手用于阻挠竞争做法的法案。
品牌药生产商有时拒绝向仿制药公司提供样品,在这样的做法遭到不断投诉之际,由民主、共和两党联合提出的这一名为《创建和重建公平获取等效样品法案》)用于仿制药。为...
|
|
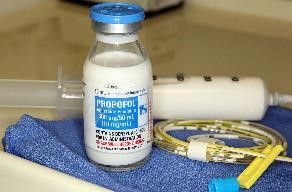
FDA对异丙酚注射剂的新BE要求
2016.06.19
6月16日FDA新发布19种药品的生物等效性(BE)指南,同时修订了另外19种药品的BE指南,其中一篇关于异丙酚注射剂的新发布BE指南引人关注。
所关注的问题涉及对产品配方定量(Q1)和定性(Q2)相同超出过去要求的新规定。对于大多数非肠道产品,只要申请人“鉴别和表征出存在的差异,并提...
|

|
CREATES议案能否帮助仿制药企业获得所需参照样品
2016.06.18
美国参议院司法委员会于6月14日提出《2016创建和重建公平获取等效样品法案(CREATES)》,旨在阻止对受限制的分销系统和风险评估与减轻策略(REMS)计划的滥用。这两个手段会如何阻碍可负担得起的仿制药的市场准入?
品牌药公司拒绝将产品样品销售给潜在的仿制药竞争者,从而使得仿制药...
|

|
WHO数据可靠性指南定稿前后对比
2016.06.17
WHO 2015年9月公布了数据可靠性(data integrity)指南的草案,与英国MHRA偏重定义和基本概念,和美国FDA偏重实际问题的指南不同,WHO的指南涵盖从管理体系到质量审计,从外部(供应商、服务商)到内部(人员培训),从数据生命周期到管理的原则性要求,到问题处理的完整框架,受到业界...
|

|
FDA前副主任被控内幕交易泄漏非公开批准信息
2016.06.16
6月22日更新:
据路透社报道,6月20日对冲基金经理之一Sanjay Valvani被妻子发现死在纽约布鲁克林的家中,颈部有伤口,同时找到一封自杀遗书和一把刀。
本周三美国FDA仿制药办公室(OGD)前副主任被指控向Visium资产管理公司对冲基金经理提供非公开的药品批准信息使得对冲基金...
|

|
FDA设想构建临床前研究数据库
2016.06.15
实验室动物实验的官方数据库能否帮助医学科学解决一些最紧要的问题?
FDA局长Robert Califf提议构建实验室研究数据库,作为与已经在收集临床试验信息的数据库相对应的数据库。一些研究人员对这一想法感兴趣。但如果政府官员认真推动这一概念,将面临一些棘手的问题 — 尤其是关于早...
|

|
Janssen连续制造线批准前检查曾收到FDA483
2016.06.14
【编者按】这份483是FDA针对由批制造转向连续制造的补充申请所做的批准前检查(PAI)中所发现的观察项,该企业也犯有常见的GMP错误,并非连续制造就一切GMP合规了。现在我们已经知道结果,该补充申请已获得FDA批准成为首个生产中转变生产方式的批准。回过头去看这些观察项,希望对学习这...
|

|
Teva匈牙利工厂停产敲响大药企警钟
2016.06.13
Teva制药公司在匈牙利的工厂收到美国FDA的出口禁令已经停产。该停产问题在匈牙利监管机构 — 匈牙利国家药品研究所(OGYEI)于6月3日发布试图应对药品短缺问题的https//www.ogyei.gov.hu/page.php?item=1506 通知(匈牙利语)后曝光。在OGYEI通告该消息之前,FDA于5月27日发布...
|

|
FDA发布用于配药的待包装原料药定稿指南
2016.06.12
【相关资讯】:FDA发布待包装原料药用于配药的临时执法政策 2015-10-27
随着大量活动仍围绕着配药药房和外包设施,以及执法行动仍在增加,6月9日FDA发布两份定稿指南文件描述了可以根据503A(药房)和503B(外包设施)用于配药而不采取FDA执法行动的待包装原料药类型(FDA官网通知)...
|

|
欧盟对德国药品网上销售定价的裁定
2016.06.11
6月2日,欧盟总法律顾问Szpunar签发意见书,就有关处方药跨境互联网销售的诉讼向欧盟法院(CJEU)提出建议。1
这起诉讼涉及消费者组织试图与德国以外的网上药店合作,使德国患者获得更为优惠的价格条件。德国法律规定,无论这些产品是否在传统的德国药房出售,或者由德国以外的供应商在...
|

|
ISPE发布质量量度二期试点报告
2016.06.10
在2016年6月6日至8日的国际制药工程协会(ISPE,International Society of Pharmaceutical Engineering)、FDA和药品质量研究学会(PQRI,Product Quality Research Institute)联合举办的质量制造会议上,ISPE发布了质量量度二期试点报告。ISPE的质量量度二期试点继续与国际知名的...
|

|
基于数据可靠性的持续改进和知识管理
2016.06.09
Letter of the law versus the spirit of the law(法律条文与法律精神)的说法由来已久,当关注点在遵守法律条文而不是法律精神时,反映在行为上就只是遵从字面解释,而不在乎法律意图。相反,当关注点是法律精神而不是条文,由此产生的行为所反映的正是法律所意指,尽管不一定...
|

|
FDA 2016财年5月ANDA批准数据
2016.06.08
仿制药办公室(OGD)5月完全批准54件ANDA,暂时批准20件。5月原始ANDA的接收量为58件,本财年只有三个月的接收量高出这一数字。
使用目前8个月批准总量的平均值估计2016财年可能总共批准676件ANDA,比之前的预估略少。按目前平均值对接收量的预估也下降到879件,比我们之前认为可能接近10...
|

|
因批准前检查缺陷导致的完全回应函将会更多?
2016.06.05
过去两个月中,FDA对两个潜在的重磅炸弹药物的申请发布完全回应函(CRL)。收到CRL几乎是申请人在焦急的等待申请命运时等来的最糟糕的FDA沟通信件。自2008年完全回应函最终规定的生产观察项。将来是否会有更多CRL基于药品质量办公室新的整合审评程序来自于检查和生产缺陷?FDA是否真正通过...
|

|
患者需为疼痛治疗支付更多费用?
2016.06.04
我们都了解有偿延迟(pay-for-delay),即仿制药企业达成专利和解并同意一段时间内不上市销售产品而获得一些回报。美国联邦贸易委员会(FTC)正积极追踪这类案件作为反竞争行为,但这并不是今天的主题。现在有一个“有偿疼痛”(pay-for-pain)的提案在国会流传。我阅读了由西弗吉尼亚...
|

|
FDA发布透皮给药系统ANDA黏附力评估指南草案
2016.06.03
5月31日FDA发布题为《透皮给药系统和局部贴剂简化新药申请的黏附力评估》指南草案。草案文件讨论了申办人证明其拟定产品的黏附力与参照产品(RLD)类似的方法。
显然,对于一个仿制透皮给药系统(TDS)产品与RLD治疗等效,必须具有类似于RLD的黏附力。这是因为被吸收进入全身循环的药物...
|

|
美国卫生部被指拖延FDA对标签外使用推销指南的发布
2016.06.02
【编者按】 两个法官和一个陪审团在过去三年中做出的三次允许标签外推销的裁决,是对FDA药品监管根基的冲击,因为标签是药品监管的重中之重。在公众对联邦政府和垄断企业不满情绪日益高涨的今天,国会议员又火上加油,强迫FDA制定标签外推销的指南。事态的发展越来越值得关注了。
制...
|

|
制药和医疗保健行业的CEO们去年薪酬如何?
2016.06.01
镜子,镜子,告诉我,谁是收入最高的首席执行官(CEO)?
一份来自美联社和研究公司Equilar的最新报告给出了一些答案,并再次表明,运营大型企业的高管中许多最高收入者是制药和医疗保健CEO。(Equilar是总部位于加州的一家私营公司,提供上市公司和非营利组织的高管的总薪酬信息。)
...
|