
|
欧盟公布第一版关键药物清单以预防短缺
2023.12.14
欧洲药品管理局(EMA)于 12 月 12 日发布了第一版欧盟关键药物清单,其中包含 200 多种被认为对整个欧盟医疗保健系统至关重要的人用药原料药,应优先考虑这些药物的供应连续性,避免短缺。
EMA 表示,此清单是支持欧盟确保供应安全和防止关键药品短缺的重要工具,是对 10 月...
|

|
国际药政每周概要:FDA首批两款镰状细胞病基因疗法,...
2023.12.13
【监管综合】
12.07【FDA】指南定稿 药品供应链安全法案要求的某些处方药的确证系统
【注册、审评、审批】
12.08【FDA】FDA 首次批准治疗镰状细胞病患者的基因疗法
【创新研发与临床】
【GxP 与检查】
12.05【FDA】Untitled Letter 美国 Novartis Pharmaceuticals C...
|

|
细胞治疗产品常见的 CMC 和 GMP 检查缺陷分析
2023.12.13
最近细胞治疗产品企业的 CMC 和 GMP 问题可能给药企带来了深刻的教训。识林分享一篇今年 9 月份给企业会员发送的分析文章,希望大家能够吸取经验教训,早做准备。
另外,还可参考识林去年发布的 FDA 对细胞和基因治疗产品的检查和常见缺陷统计以及最近 FDA 因 CGMP 问题向诺华 C...
|

|
FDA 发布先进制造技术认定计划指南草案
2023.12.13
美国 FDA 于 12 月 12 日发布了题为“先进制造技术认定计划”的指南草案,针对那些希望在药物开发中使用先进制造技术(AMT)以缩短和改善美国供应链的制药公司。
AMT 可以被定义为一种尚未在小分子药物或生物制剂的制药过程中使用的“新颖”技术,旨在提高流程效率。FDA 鼓励使...
|

|
美价格机构分析报告显示八种药物在无新获益证据的情况...
2023.12.12
根据美国临床与经济评价研究所(ICER)于 12 月 11 日发表的一份题为“不受支持的涨价报告”分析报告显示,在 2022 年期间,制药商在没有任何新临床证据证明价格上涨合理性的情况下大幅提高了 8 种广泛使用的药物的价格,导致美国患者和医疗保险公司去年额外花费了 12.7 亿美元。
...
|

|
美国众议院提出新法案,未按时完成儿科研究可能会受到...
2023.12.12
美国国会众议院两党议员代表正在寻求通过新立法来促进儿科药物开发,立法将优先考虑将儿科患者纳入新药试验。
由加州民主党众议员 Anna Eshoo 和德州共和党众议员 Michael McCaul 牵头的《2023 儿科药物创新法案》将收紧药物开发的要求,以将儿科人群纳入进来。
具体来说,法...
|

|
国内药政每周导读:2020年药典问答,药械GSP,特医食...
2023.12.11
【创新与临床研究】
12.7,【CDE】关于公开征求《脑膜炎球菌疫苗临床试验技术指导原则(征求意见稿)》意见的通知
【CMC与仿制药】
12.7,【药典会】新增多篇标准草案的公示
【注册与审评】
12.7,【CDE】关于公开征求《化学仿制药参比制剂目录(第七十七批)》(征...
|

|
FDA 首次批准的两款镰状细胞基因疗法对比与后续需要...
2023.12.11
美国 FDA 于 12 月 8 日批准了两种治疗镰状细胞病(SCD)的基因疗法,包括 Bluebird Bio 的 Lyfgenia 和 Vertex 药业的 Casgevy,其中 Casgevy 是 FDA 批准的首个使用 CRISPR/Cas9 技术的疗法。
在镰状细胞病中,突变导致血红蛋白分子粘在一起并使血细胞扭曲成新...
|

|
FDA生物制品中心主任:需要更多人手满足基因治疗产品...
2023.12.11
美国 FDA 生物制品审评与研究中心(CBER)主任 Peter Marks 表示,如果 FDA 希望其罕见病治疗“曲速行动”(Operation Warp Speed)能够取得成功,那么 FDA 还需要增加数十名审评员。
今年 9 月份 FDA 启动了名为“支持推进罕见疾病治疗临床试验”(START)的罕见病试点...
|

|
【周末杂谈】上市难,撤市更难,为何?
2023.12.10
从两药品的撤市,费解FDA的药品获益和风险权衡
药品获批上市不易,众所周知。获批药品撤市也难,但有此经历的企业不多。这一上一下,反映了药品监管对患者获益和风险的权衡,是药品监管的核心考量。近几个月,FDA 在两起药品撤市案件上的做法,为了解 FDA 对获益和风险的权衡,提供...
|

|
【更新】“岗位知识地图”内容更新
2023.12.09
下列岗位更新,收录近期相关法规指南和知识内容。岗位知识地图入口
新的岗位地图正在绘制中,大家也可提出需求,反馈意见和建议。
相关阅读:【识林新模块】“岗位知识地图”试运行:岗位工作做到哪,识林知识学到哪
无菌制剂QA
原料药QA
中国化学药创新药注册
...
|

|
【识林主题词】新增:首过空气,RABS,设计审核;修订...
2023.12.09
— 主题词,是识林针对制药行业的关键概念,基于大量资料的综合分析,从定义、工作流程、法规指南、文献案例等多个维度梳理的系统知识纲要。截至目前,识林【主题词库】已上线超过1000个主题词,还在陆续增补当中。
— 从主题词入手,也是使用识林的最佳方式之一。主题词的系统性、...
|

|
【识林新解读】中国、欧盟、PICS、WHO无菌附录对比,A...
2023.12.09
在官方法规指南之外,识林或原创、或整理了大量对比解读、案例解析等内容,作为识林用户的参考资料,提供更多视角,且与岗位实务联系更为紧密。
这类资料,全部收录在专门为此开发的“对比解读案例解析”数据库内,通过“业务标签”和“知识标签”的交叉索引,用户可迅速查阅学习本岗...
|

|
WHO、PICS和欧盟无菌附录差异分析
2023.12.08
欧盟、WHO和PIC/S分别于2022年8月,2022年12月和2023年8月陆续发布了GMP无菌附录的最终稿。对于这三个版本的无菌附录,识林以PIC/S版本为基础进行了对比并以花脸稿的形式呈现。
三个版本实质内容基本一致,其中欧盟版本相比于PIC/S 版本,几乎无差异(仅一两处同义词替换);而WHO版...
|

|
FDA 因抗生素耐药性等原因撤销对 100mg 环丙沙星片...
2023.12.08
美国 FDA 于 12 月 7 日在《联邦公报》上发布通告,撤销对环丙沙星 100mg 片剂的批准,因为目前的证据表明,大肠杆菌(E.coli)对低浓度环丙沙星的耐药性增加,使其对于治疗急性单纯性膀胱炎不再有效。
从历史角度看,1987 年 10 月 22 日,FDA 批准了 CIPRO(盐酸环丙沙星)口...
|

|
线上讲座:从霉菌污染调查看微生物控制
2023.12.07
《制药工业微生物控制及无菌保障》读书分享会
微生物控制是无菌保障的关键点,也是无菌生产真正的特殊之处。PIC/S和欧盟无菌附录1提出污染控制策略(CCS),也指明需要从系统控制的维度,关注微生物。
王晓明医学博士于2023年4月出版的《制药工业微生物控制及无菌保障》一书,依据...
|

|
FDA就CAR-T Kymriah生产CGMP问题向诺华发布无标题信
2023.12.07
美国 FDA 于 12 月 5 日公布了一封 8 月份发给诺华的无标题信,信中概述了 FDA 检查人员在诺华新泽西 Morris Plains 工厂发现的 Kymriah(tisagenlecleucel)生产过程中与 CGMP 要求的重大偏离。
无标题信(Untitled Letter)可认为是 483 以上而警告信未满的情况下发...
|

|
稳定性研究相关缺陷、检查关注点和案例分享
2023.12.06
识林最近汇总了2013-2023财年FDA 483 年度审计缺陷列表,并发布了对2023财年483缺陷项的统计梳理。值得注意的是,在“实验室控制”一类中,有一条关于稳定性研究的缺陷项,是首次出现的全新表述。该缺陷项描述为:顺势疗法药品的稳定性评估并非基于药品上市时的同一容器密闭系统(21 CFR ...
|
|
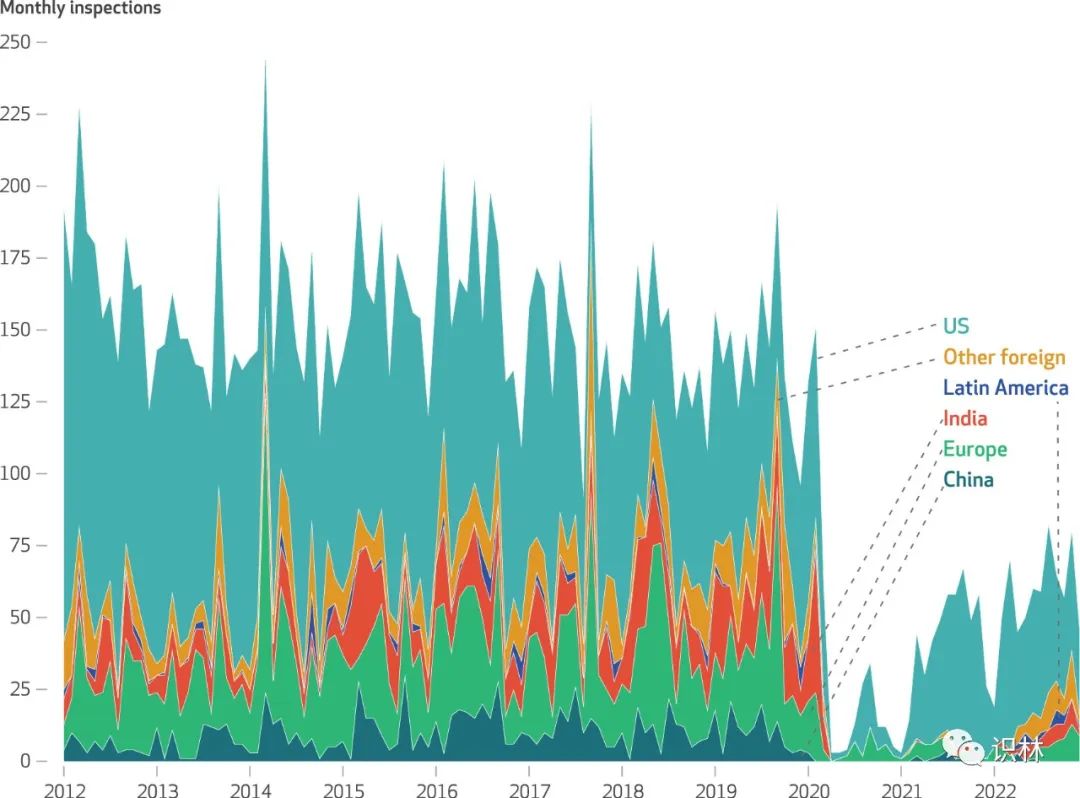
分析报告显示 FDA 对海外药品生产监管力度仍远低于...
2023.12.06
根据 12 月 4 日发表在《卫生事务》(Health Affairs)上的一篇题为“FDA 全球药品检查:对生产企业的监督仍远低于新冠(COVID-19)之前的水平”(FDA Global Drug Inspections Surveillance Of Manufacturing Establishments Remains Well Below Pre-COVID-19 Level...
|

|
国际药政每周概要:ICH Q5A(R2) 病毒安全性评价指...
2023.12.05
【监管综合】
11.29【ICH】Q5A(R2) 来源于人或动物细胞系生物技术产品的病毒安全性评价
【注册、审评、审批】
【创新研发与临床】
11.29【FDA】计算模拟揭示了鼻用喷雾剂分布的影响因素
11.29【WHO】首届 WHO 全球临床试验论坛提出了可持续的临床研究基础设施的全球愿...
|