
|
制药业新方向:Teva 出售与药物可及性和气候目标相关...
2021.11.19
作为制药商的首创举措,Teva 制药最近出售了 50 亿美元的债券,这些债券与其在实现与气候变化相关的目标和使某些中低收入国家药物可及性方面取得的进展直接相关。
目标是到 2025 年将提交给中低收入国家监管机构的上市申请的累计数量以及捐赠药物的数量与前五年相比增加 150%。...
|

|
FDA 总结影响批准后变更申请的常见缺陷及改进意见
2021.11.18
美国 FDA 在 2021 年 11 月 10 日普享药协会(AAM)GRx+Biosim 会议上提供了帮助确保简化新药申请(ANDA)批准后补充申请的审评更顺畅的一些建议,并解决了如何对某些变更进行分类的问题。
FDA 官员介绍了影响 ANDA 批准后化学、生产和控制(CMC)提交的一些常见问题,并讨论...
|

|
欧洲监管机构表示渤健阿尔茨海默病新药 Aduhelm 不...
2021.11.18
渤健(Biogen)于 2021 年 11 月 17 日公布,一个欧洲药物审评小组通知渤健,其阿尔茨海默病治疗药 Aduhelm 不太可能在欧洲获得批准。Aduhelm 在欧洲药品管理局(EMA)的口头解释听证会之后收到了来自 EMA 专家的“负面投票”。
在 11 月 9 日举行的口头解释听证会上,...
|

|
WHO 发布口服新冠抗病毒药 Molnupiravir 生物等效...
2021.11.17
WHO 于 2021 年 11 月 15 日发布了关于默沙东口服新冠抗病毒药 Molnupiravir(莫纳皮拉韦) 的生物等效性(BE)指南,以帮助制药商开发向 WHO 预认证小组提交申请的产品。
Molnupiravir 是默沙东和合作伙伴 Ridgeback Biotherapeutics 研发的首个显示成功治疗新冠的口服...
|

|
国际药政每周概要 2021.11.08-11.14
2021.11.16
11.09 FDA 发布 27 篇新增和 21 篇修订 BE 指南
这一批 48 篇具体产品指南包括:27 篇新增(针对 24 种活性成分)和 21 篇修订(针对 20 种活性成分)。28 篇(其中 10 篇是复杂产品)针对的是尚无获批 ANDA 的产品。复杂产品相关指南共 13 篇(8 篇新增,5...
|

|
国内药政每周导读 2021.11.08-11.14
2021.11.15
11.08,不良反应监测中心公开征求《药物警戒体系主文件撰写指南(征求意见稿)》意见
【目的与要点】
2021年5月7日,NMPA正式发布《药物警戒质量管理规范》,此次专门为该主文件发布撰写指南的征求意见稿,目的是“指导持有人撰写药物警戒体系主文件的技术文件,也是药品监督管理部...
|

|
渤健发布更多 Aduhelm 生物标志物数据及其与阿尔茨...
2021.11.15
渤健因其阿尔茨海默病新药 Aduhelm 有争议地批准而饱受批评,最近,渤健提交了另一生物标志物的数据以及公司的一项分析,该分析显示该生物标志物与疾病进展的减缓有关。
渤健在阿尔茨海默病临床试验(CTAD)会议上公布的两项支持 FDA 批准的 3 期试验中,在 FDA 批准的剂量下,Adu...
|

|
【质量对话】对“干货”和“湿货”的一点看法
2021.11.14
故事本身是“干货”,而听故事还可以学习讲者的思维方式,是“湿货”
刺槐: 多年前,我供职的一家创新型生物制药公司的细胞生物学总监因与研发副总裁不和,突然离职。总监是守规矩的人,工作笔记、实验记录及电脑文档,都有详细记录并完整地保留下来了,但很多实验设计背后的思考,...
|

|
FDA 前局长 Robert Califf 再次被提名为 FDA 局...
2021.11.13
美国总统拜登于 2021 年 11 月 12 日(周五)提名 FDA 前局长 Robert Califf 医学博士再次领导 FDA。此举结束了近一年的政治角力。
此前,白宫审查了几名候选人,但由于收到抱怨这些候选人与制药行业走得太近而最终放弃。最后,白宫官员可能得出结论,他们找不到没有行业联...
|

|
最新阿尔茨海默药临床试验结果喜忧参半,tau 靶向抗...
2021.11.12
在一项涉及轻度至中度阿尔茨海默病患者的中期研究中,与安慰剂相比,一个名为 semorinemab 的抗 tau 抗体治疗确实使认知能力下降的速度降低了近 44%,实现了该研究的主要目标之一。但与安慰剂相比,该药并没有改善研究中患者的功能 — 阿尔茨海默病合作研究-日常生活活动(未能实...
|
|
谁发明了新冠 mRNA 疫苗?Moderna 和美国政府各执...
2021.11.11
根据 2021 年 11 月 9 日下午《纽约时报》公布的一份最新报道显示,Moderna 声称三名美国国立卫生研究院(NIH)科学家并没有参与发明新冠疫苗的关键成分。该声称来自Moderna 于今年 7 月份向美国专利商标局提交的文件。
在提交的文件中,Moderna 表示,已经“达成信实的决定”...
|

|
电子健康记录中真实世界证据的自动提取用于支持抗生素...
2021.11.11
根据美国 FDA 的 2021 年 11 月 9 日发布的最新研究报告显示,从电子健康记录(EHR)中提取真实世界数据的自动化系统在收集真实世界数据支持抗生素耐药性研究方面与手动数据提取一样有效。
数据提取项目由 FDA 通过抗击抗生素耐药细菌(CARB)国家行动计划提供支持。该项目始...
|

|
研究发现 FDA 计划撤销的早产预防药 Makena 与后...
2021.11.10
最近一项新的研究表明,用于预防早产的有争议药物 Makena 的关键成分 17 α-己酸羟孕酮(又称 17-OHPC)与在子宫内接受治疗的人患癌症的风险较高相关。
具体来说,与未接触 17-OHPC 的人相比,接触 17-OHPC 的人患任何癌症的风险几乎翻了一番,不过风险水平似乎因癌症而异。例如...
|

|
FDA 2021 财年仿制药批准数据趋势与分析
2021.11.09
美国 FDA 仿制药办公室(OGD)公布了 2021 财年全部仿制药使用者付费(GDUFA)批准数据。2021 财年 FDA 报告了 679 件完全批准,这是自 2016 财年(650 件批准)以来最低的年度总数(见图 1)。2021 财年的批准总数比 2020 财年减少 58 件,比 2019 财年(935 件,创...
|

|
FDA 发布 27 篇新 BE 指南和 21 篇修订指南
2021.11.09
美国 FDA 于 11 月 8 日发布了新一批 48 篇具体产品指南(PSG),为仿制药的开发和生成支持简化新药申请(ANDA)批准所需的证据提供建议,从而帮助简化企业仿制药开发和 FDA 的 ANDA 审评。
这一批 48 篇具体产品指南包括:27 篇新增(针对 24 种活性成分)和 21 篇修订...
|

|
【一周回顾】2021.11.01-11.07
2021.11.08
国家局启用原料药生产供应信息采集模块、短缺药品生产供应及停产报告信息采集模块。药审中心公开征求审评计时中止与恢复管理规范的意见,征求 ICH E14 及问答和 Q3C(R8) 指导原则的实施建议。英国批准首个新冠口服抗病毒药物。WHO 发布第八种新冠疫苗的紧急使用清单。
上周热...
|
|
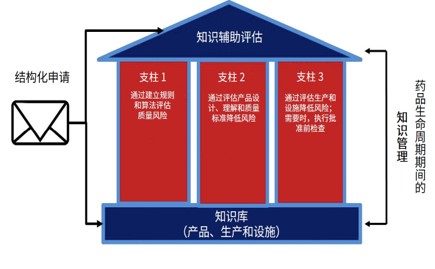
FDA 将逐步扩大 KASA 审评计划的使用,正在开发生...
2021.11.08
美国 FDA 正采取“逐步”方法来实施其知识辅助评价和结构化评价(KASA)药品审评计划。该审评计划已针对固体口服制剂的简化新药申请(ANDA)启动,最终将在 2023 财年针对新药申请(NDA)和 ANDA 液体制剂推出。
KASA 将在 2024 年分阶段用于研究用新药申请(IND)和批准后变更,...
|

|
【质量对话】生产质量管理领域的专业化
2021.11.07
要赢得他人在专业上的尊重,首先需要有值得尊重的思想和做法
刺槐: 对药企尤其是创新型药企来说,生产和质量的重要性,恐怕是要排在营销和研发后面,而质量又排在生产后面,垫底。
编辑: 不是常听企业说“质量重于山”吗?
刺槐: 是的,都是这么“说”的。记得几年前,在一...
|

|
默沙东口服抗新冠药 Molnupiravir 首获英国授权,作...
2021.11.05
2021 年 11 月 4 日,英国对迄今为止首个显示成功治疗新冠的药物默沙东的 Molnupiravir 授予有条件许可,成为首个许可该药的国家。
该药在英国获准用于 18 岁及以上新冠检测呈阳性并且至少有一种患严重疾病的风险因素(例如,肥胖或心脏病)。轻度至中度新冠患者需要服用四片...
|

|
研究人员举报辉瑞新冠疫苗试验数据可靠性问题,FDA ...
2021.11.05
2021 年 11 月 2 日发表在英国医学杂志(BMJ)上的一篇调查文章1备受关注,文章报告了内部举报人对帮助开展辉瑞关键新冠疫苗试验的合同研究公司的不良做法的揭露,引发了人们对于数据完整性和 FDA 监管监督有效性的担忧。
文章的信息来自于研究组织 Ventavia 研究集团的一名地...
|