|
LIVIVO 有望成为 PubMed 替代,学界警惕系统偏见
2026.01.02
识林读者元旦快乐!
元旦期间识林继续发布国际动态,减少至单篇,节后恢复日常更新。
此前识林曾报道德国计划开发一个开放、可持续且具主权性的替代方案,以对标美国国家医学图书馆(National Library of Medicine)旗下的免费生物医学文献数据库PubMed。该项目由ZB MED牵头,...
|

|
识林祝大家2026新年快乐!
2026.01.01
识林®版权所有,未经许可不得转载
...
|

|
FDA 重提创新制造技术战略,当前进展迟缓
2025.12.31
12月17日,FDA发布了《FDA创新制造技术的战略文件》最终版,以履行其在PDUFA VII中的承诺。该文件基于2023年6月8日由杜克-马戈利斯卫生政策中心主办的公开研讨会意见,并整合了FDA在审评涉及先进制造技术的申报资料中获得的经验。文件更多的是梳理现状,并未提出特别具体的改进举措,...
|
|
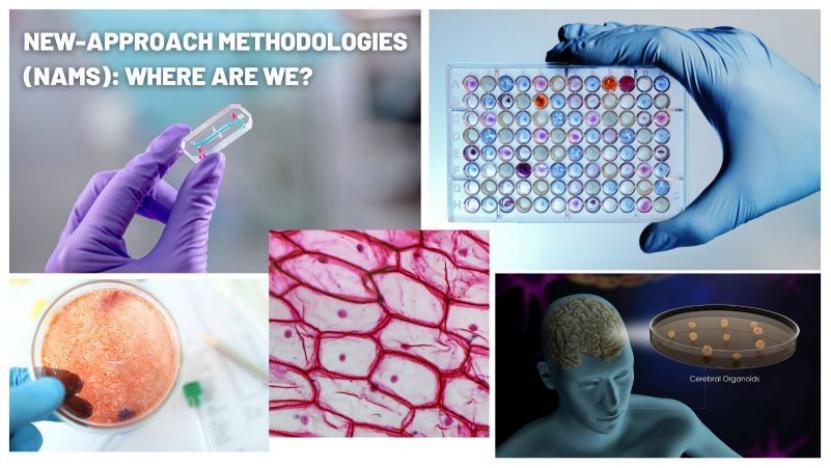
仅0.5%申报资料含 NAM,CDER 分析显示动物试验替...
2025.12.31
FDA CDER在12月发表研究文章《CDER 视角:药品开发项目中提交的新方法(NAM)的情况》,系统分析了过去15年间(2010-2024年)申报至FDA的药品中NAM的应用现状与提交趋势。研究基于CDER内部开发的检索工具,对电子通用技术文档(eCTD)中非临床研究模块(Module 4)进行关键词挖掘,涵盖...
|

|
国际药政每周概要:WHO 生物制品和疫苗变更情形,加...
2025.12.31
【早期开发与临床】
12.23,【HC】关于去中心化临床试验的指南草案
【注册与变更】
12.24,【WHO】已获批生物制品变更的程序与数据要求指南
12.25,【ICH】M2建议与技术参考
【生产质量】
12.24,【WHO】关于 WHO 生物标准物质的制备、表征、建立和使用的建议
...
|

|
行业协会批评 FDA 生物标志物认定滞后,呼吁接入 PDU...
2025.12.30
近日,FDA在生物标志物(Biomarker)审评领域的进展引发专业界广泛讨论。根据癌症研究之友(Friends of Cancer Research)于10月底发表在《治疗创新与监管科学》(Therapeutic Innovation and Regulatory Science)上的分析报告,FDA通过《21世纪治愈法案》(21st Century Cures ...
|

|
白皮书探讨罕见癌症的无缝临床试验设计
2025.12.30
美国癌症研究之友(Friends of Cancer Research)近期发布白皮书《罕见癌症的无缝临床试验设计:利用操作性和适应性策略加速药物开发》,指出无缝临床试验(Seamless Clinical Trial)的实践应用仍不充分,并系统阐述了如何通过整合传统分阶段研发流程,在罕见癌症领域加速创新疗法...
|

|
生物制品立卷审查程序更新,FDA 新增 Checklist
2025.12.29
继10月份更新适用于药品审评与研究中心(CDER)的立卷审查拒收MAPP后,FDA紧接着在12月份发布并生效了《SOPP 8404:立卷审查拒收程序》,该程序明确了生物制品审评与研究中心(CBER)对生物制品许可申请(BLA)、新药申请(NDA)及相关补充申请进行立卷审查拒收(RTF)的标准操作,以避...
|

|
WHO 更新生物制品变更指南,整合疫苗,推动监管信赖
2025.12.29
12月24日,WHO发布《已获批生物制品变更的程序与数据要求指南》征求意见稿,征求意见截至2026年1月30日。
意见稿整合2013年与2017年分别发布的疫苗及治疗性生物制品变更指南,形成了一份统一的技术指导文件,为各国家监管机构(National Regulatory Authority, NRA)建立或更新本...
|

|
国内药政每周导读:ICH GCP 明年3月31日适用,eCTD...
2025.12.29
【早期研发与临床】
12.22,【CFDI】关于发布《生物等效性试验电子化记录技术指南(试行)》的通告
12.24,【NMPA】关于适用《E6 (R3) :药物临床试验质量管理规范技术指导原则》国际人用药品注册技术协调会指导原则的公告(2025年第125号)
12.24,【CFDI】关于提醒填报2...
|

|
【周末杂谈】科学史上坚持原则和践行道德的故事
2025.12.28
科学的发展既需要巨匠,也需要捍卫科学制度的仁人志士
年底了,说点轻松有趣的事吧。
杨振宁先生于今年10月去世,全球悼念。在泛读相关历史时,笔者偶然发现了一则有趣的故事,它揭示了科学的发展既需要杨先生这样的科学巨匠,也需要捍卫科学制度的仁人志士。
爱因斯坦是伟大的物理...
|

|
从识到实-识林 君实 AI应用项目上线
2025.12.27
近期,识林为君实生物开发的、以“大语言模型 + 药业专业知识库”为核心架构的AI-GxP平台正式上线。经过两期近一年半的开发、与君实团队的反复测试和调优,法规通、翻译、偏差调查、变更管理和迎检助手五个紧扣质量部门核心业务需求的AI应用场景落地履职。
一、从“识”启程:AI在药...
|
|
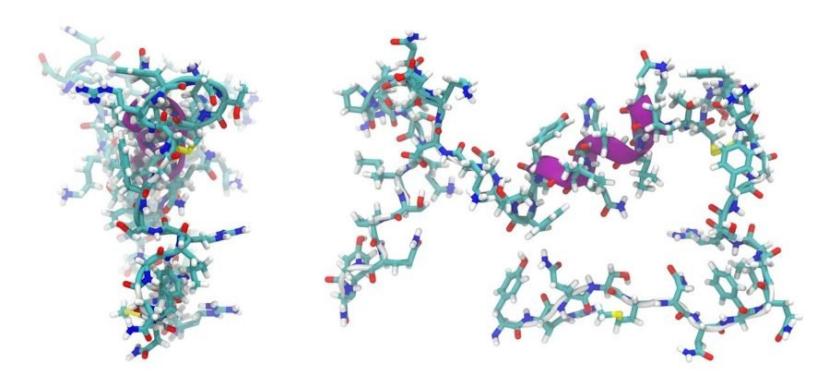
EMA 定稿合成多肽 CMC 开发和 CTD 申报要求
2025.12.26
12月9日,EMA定稿发布《合成多肽研发和生产指南》,明确药用合成多肽(无论是现有化学实体还是新化学实体)在CMC药学和质量方面的要求以及CTD申报所需的信息。2026年6月1日生效。
EMA认识到合成多肽因其分子大小和结构复杂性处于小分子药物与蛋白质药物之间,从质量角度看需要特定的...
|

|
减免临床后的生物类似药:新 BsUFA 和“仿制药化”...
2025.12.26
12月初,FDA召开了关于生物类似药用户费用法案重新授权(即BsUFA IV)的公开会议,监管机构、生产企业及其他利益相关方共同探讨生物类似药的未来(2028-2032)优先事项。
目前,BsUFA为FDA生物类似药审评活动提供了约61%的资金支持,并已推动81个生物类似药获批上市。BsUFA IV正式...
|
|
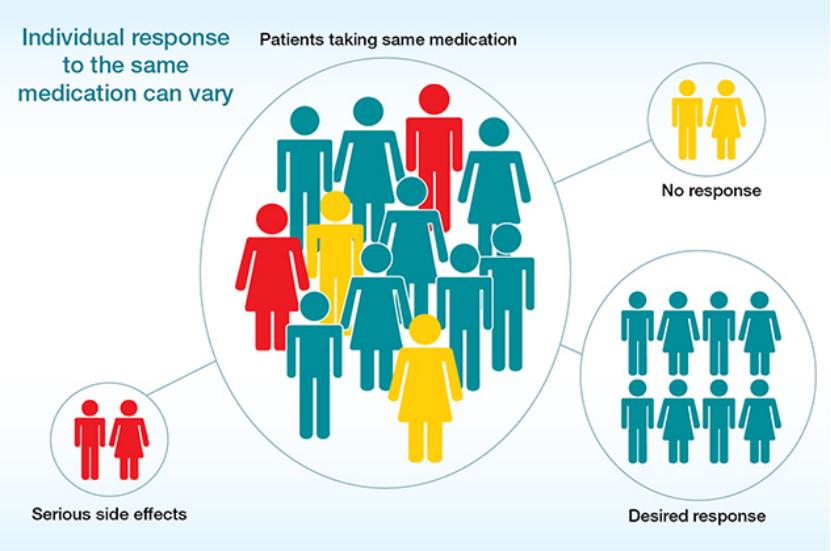
EMA 拟修订2018年药物基因组学研究质量管理规范
2025.12.25
12月8日,EMA发布了一份概念性文件,启动修订2018年3月发布的现行《药物基因组学研究质量管理规范》(Good Pharmacogenomic Practice, GPP)指南。本次修订旨在纳入新的科学证据、方法论与最佳实践,重点聚焦方法论、数据解读与研究设计三大核心领域。
药物基因组学方法论更新:...
|

|
WHO 解析34年来全球基因组学临床研究格局
2025.12.25
基因组学技术正逐步融入生物医学研究与医疗健康体系,其通过识别疾病相关变异、提升诊断精度、推动个体化医疗发展,深刻改变了疾病诊疗模式。12月14日,WHO发布《临床研究中的人类基因组学技术 – 研究全景:1990-2024年报告》,基于国际临床试验注册平台(ICTRP)1990年至2024年注册的6...
|
|
BIMO 指南定稿,FDA 详述非临床和临床设施检查流程
2025.12.24
12月19日,FDA发布《适用于生物研究监测检查的流程和实践》定稿指南,旨在为接受FDA生物研究监测(Bioresearch Monitoring,BIMO)项目检查的设施提供关于检查流程、实践以及与FDA沟通的明确建议。
FDA的BIMO项目是一个综合性的监管项目组合。该项目旨在通过现场检查、调查以及远程...
|

|
前 FDA 检查副局长:以“检查准备度”应对“突击检...
2025.12.24
12月17日,前FDA主管检查的副局长、现任咨询公司Canal Row Advisors质量与合规部门负责人Michael Rogers在领英发表文章《FDA检查策略进化:两大变革形塑监管未来》(FDA's Evolving Inspection Strategy Two Shifts That Will Shape the Future of Regulatory Oversight)...
|

|
FDA 拟直接对接初创技术公司,合作开发 AI 等新技...
2025.12.23
12月19日,FDA发布了一份有些特别的信息请求(RFI),专门征求风险投资(Venture Capital,VC)机构的专业意见,旨在就建立一种新型合作模式强化FDA与美国最具创新力的初创技术公司之间的协作,以推动人工智能(AI)、生物技术、医疗器械及监管技术等领域的公共卫生创新。
FDA在公告...
|

|
FDA 与辉瑞合作综述当前 AI 在药物研发中的代表性...
2025.12.23
FDA CDER研究人员与辉瑞研发中心在11月联合发布了综述文章《人工智能在临床与转化科学中的应用:从实验室洞见到临床影响》,该文汇集了来自全球的30多篇研究论文,系统梳理了人工智能(AI)在药物研发全生命周期中的技术进展与实践案例。
当前各类AI相关新闻和文献众多,似乎其应用...
|