
|
国内药政每周导读:AI+ 药品监管,沟通交流修订,做...
2026.04.06
【CMC药学研究】
3.30,【NMPA】关于发布仿制药参比制剂目录(第一百零三批)的通告(2026年第8号)
【注册与变更】
3.30,【NMPA】部署完善药品附条件批准制度有关工作
3.30,【CDE】关于上线注册服务平台的通知
4.3,【CDE】关于修订发布《国家药品监督管理局药品审...
|

|
外行用 AI 治好了患癌宠物狗?制药界和科技界的“凉...
2026.04.06
一只患有皮肤癌的斯塔福郡斗牛梗犬Rosie,近期成为AI生物技术领域的讨论焦点。广为流行的叙事是,其主人Paul Conyngham利用ChatGPT、Grok等大语言模型(Large Language Models,LLM)为宠物Rosie开发定制信使核糖核酸(messenger RNA,mRNA)癌症疗法,疗效显著。
在这个故事席卷科...
|

|
【周末杂谈】AI 在 GMP 上的应用,在重蹈 Part11...
2026.04.05
让AI参与GMP控制,而不仅是单纯用于降本增效,会带来很多问题
Déjà vu,源自法语,意为“已见过”,表述的是一种强烈而短暂的错觉,让人感觉当前的情境仿佛早已经历过,尽管明知这是全新的体验(往往是不好的体验)。这是一位美国GMP领域资深人士,最近谈起如何监管AI在GMP上的应用时...
|

|
【识林社区】问答集锦:临床试验终止报告、IND中控数...
2026.04.04
识林社区是面向所有识林用户的互动交流平台。在这里,识林用户提出问题,同时也解答问题,并参与讨论。大家期待的答案,不是一句道听途说,也不仅是“经验之谈”,而且越重要越复杂的问题,往往并无拿来即用的答案。
好的答案,应兼具“依据”、“思考”和“建议”。读者不仅可以有所行...
|

|
GDUFA IV 谈判动态:审评时限延长,DMF 前置,仿制...
2026.04.03
FDA正与仿制药行业代表就第四期仿制药用户付费修正案(Generic Drug User Fee Amendments,GDUFA IV)展开多轮谈判。该修正案将覆盖2028至2032财年的仿制药注册审批,主要条款将在2026年底商定。近日公开的系列会议纪要显示谈判聚焦于多项操作性议题。
同期在谈判的还有处方药用...
|

|
FDA 局长:简化 IND,AI 立卷审查,“一天”突击检...
2026.04.03
FDA局长Marty Makary于2026年4月1日在其就任一周年的媒体电话会上公开谈及一系列旨在加速美国新药研发进程的监管改革设想。
识林此前曾报道Makary向媒体书面总结2025年工作并展望2026年,这次电话会里提到的举措更为具体,有望迅速落地。种种举措似乎都着落到一个“快”字。
简化I...
|

|
FDA 公布 Tavneos 相关死亡病例,此前公司拒绝撤市
2026.04.02
3月31日,FDA发布药品安全通讯,披露安进(Amgen)旗下罕见病药物Tavneos(avacopan,阿伐可泮)关联76例药物性肝损伤(drug-induced liver injury,DILI)病例,其中包含8例死亡病例。FDA指出,部分病例呈现“胆管消失综合征”(vanishing bile duct syndrome,VBDS)病理特征,...
|

|
欧盟就 PFAS 禁令征求意见,制药业恐致大量短缺
2026.04.02
欧盟针对全氟和多氟烷基物质(PFAS)的禁令计划进入公众意见征集阶段。
欧洲化学品管理局(ECHA)于2026年3月26日至5月25日期间,就其社会经济分析委员会(SEAC)关于在全欧盟范围内通过《化学品注册、评估、授权和限制法规》(REACH)限制PFAS的意见草案,面向利益相关方征集意见。ECH...
|

|
FDA 发布2025年度仿制药科研报告,分享大量研究成果
2026.04.01
3月25日,FDA发布《2025财年GDUFA科学与研究报告》,系统梳理了仿制药用户付费法案(GDUFA)科学与研究项目在2025财年的资助课题、技术进展与监管转化成果。
报告长达117页,分为9个领域,包括大量研究课题描述、进展和文献链接,为全球仿制药行业提供了详实的技术参考。篇幅所限,下...
|

|
欧洲药典13.1更新内容概要及13.2前瞻
2026.04.01
欧洲药典(Ph. Eur.)于3月初发布第13版第1期(13.1)更新内容,其中新增和修订的文本于2027年1月1日生效,须在此日期前实施。勘误文本不得迟于2026年5月31日前采纳。
3月中旬,欧洲药典委员会(EPC)召开第184届会议,会上通过的50个欧洲药典文本将在第13版第2期(13.2,2026年...
|

|
国际药政每周概要:EMA 定稿生物类似药临床简化,RWD...
2026.04.01
【非临床与临床研究】
3.25,【MHRA】MHRA 对采用非动物方法的药品的方针
3.27,【EMA】欧盟药品监管数据质量框架:应用于真实世界数据
3.27,【EMA】关于在生物类似药开发中采用定制的临床方法的思考性文件
【药学研究】
3.24,【EDQM】欧洲药典 13
【注册与变更】
...
|
|
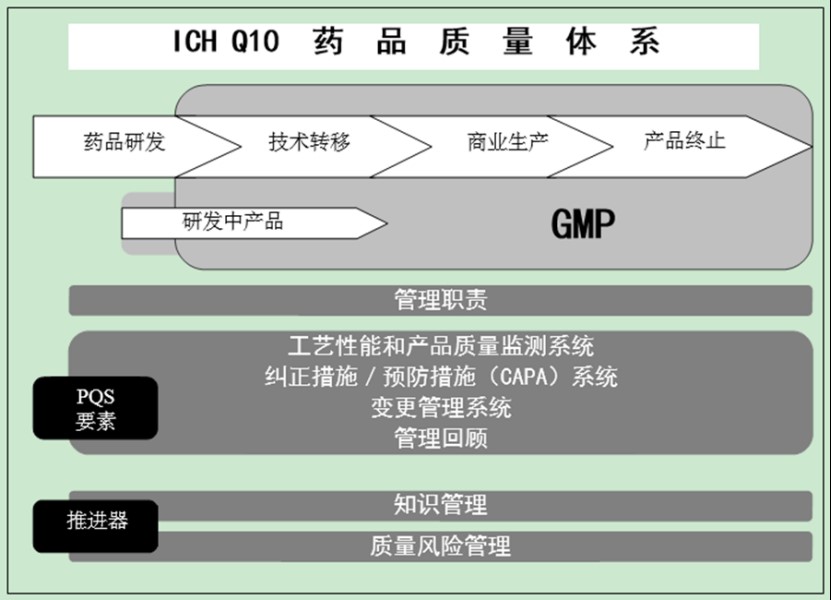
EMA 试点基于 PICS 指南检查变更管理,为 Q12应用...
2026.03.31
3月26日,EMA启动药品质量体系(Pharmaceutical Quality System,PQS)有效性试点项目。根据该项目,上市许可持有人(MAH)和生产企业可提名其生产场地,接受欧洲经济区(EEA)GMP检查员开展的PQS有效性现场评估。
试点旨在评估生产场地如何展示其PQS有效性,从而应用ICH《Q12:药...
|
|
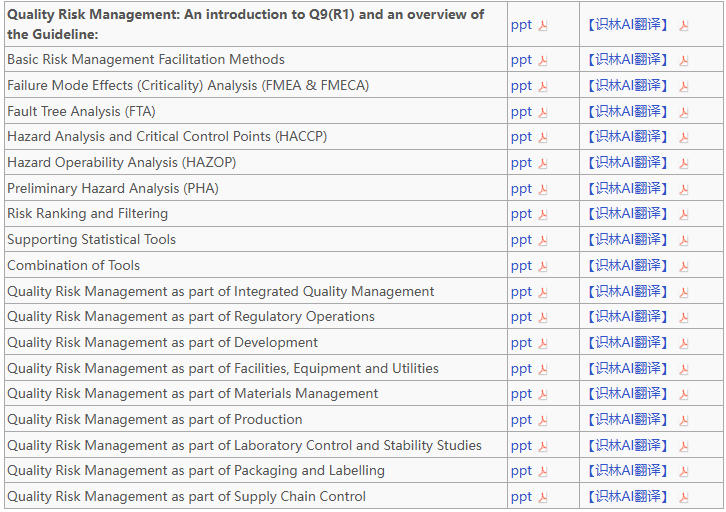
ICH 更新系列培训 PPT,适配 Q9(R1)全部工具和场...
2026.03.31
3月20日,ICH完成了对全套培训资源包(Briefing Pack)的更新,适配《Q9(R1):质量风险管理》。此次更新彻底取代了自 2006 年以来沿用多年的旧课件,为业界提供全面而权威的实操指导。
在一份纲领性PPT后,剩余18份PPT分为两大核心模块(完整目录见文末):
9个方法与工具涵盖Q...
|

|
国内药政每周导读:加速构建药品追溯体系,现代物流规...
2026.03.30
【注册与变更】
3.24,【NMPA】关于同意福建、河南省药监局开展优化药品补充申请审评审批程序改革试点的批复
【生产质量】
3.24,【NMPA】关于暂停进口、销售和使用 Vasudha Pharma Chem Limited 盐酸洛哌丁胺原料药和 Alchem International Private Limited 利血平、...
|

|
Makary 的 FDA 一周年,其2026目标是力保美国领先
2026.03.30
在FDA局长Martin Makary履新一周年之际,FDA拒绝了美国媒体PinkSheet对Makary进行就职周年专访的请求,称时间安排不可行。但Makary还是以书面形式回应了有关其第一年工作及第二年优先事项的提问(见文末)。
自2025年3月28日宣誓就任FDA局长以来,Makary推动了一系列药品审评与监管...
|

|
GAO 敦促 FDA 发指南管控 AC 会利益冲突
2026.03.30
3月24日,美国会政府问责局(Government Accountability Office,GAO)发布专题调查报告,并建议FDA提供时间表,制定针对其咨询委员会(Advisory Committee,AC)成员潜在经济利益冲突管理的指南文件。
GAO在调查中重点审查了FDA负责阿片类药物相关事务的两个AC会。调查结果显示,自2...
|

|
【周末杂谈】先进技术并未改进审批的质和量
2026.03.29
值得关注AI应用效果的人参考的、深知审批关键环节和企业实际需求的评论
无论是专业技术性应用,如基于问题的审评(QbR)、质量源于设计(QbD)、知识辅助评估和结构化申请(KASA),还是信息技术(IT)和知识工程(KE)应用,如eCTD、机器学习、大语言模型(后两者可用时髦的词AI来统称)...
|

|
【直播】26年3月全球法规月报划重点
2026.03.28
识林2026年3月报直播如期而至,并同步推出3月报。本次直播聚焦3月全球主要监管机构的重点法规,并挑选影响力较大的文件做重点简介。短短40分钟,轻量而轻松,旨在帮助大家回顾上个月的监管重点,加深理解或是查缺补漏。
月报获取渠道:
会员:关注直播当日(4月8日,周三)的【最近更...
|

|
【课程与会议】近期更新的重点课程和4-5月会议预告
2026.03.28
近期更新重点课程
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的1000+门课程7000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,及供应商技术介绍专业课程。除视频内搜索、收藏、评论功能外,...
|

|
EMA 将三项加速审评试点工具整合至 PRIME
2026.03.27
EMA于2026年3月18日发布声明,正式推出三项新监管工具,旨在优化“优先药品(PRIority Medicines,PRIME)”计划下未满足临床需求的药物研发效率。这三项工具此前已通过为期两年的试点验证,现作为永久性措施纳入PRIME计划。
三项新工具分别为:监管路线图与产品开发追踪器(regulatory...
|