|
EMA 首次认证动物试验虚拟对照组,分享审评报告和 SO...
2026.04.14
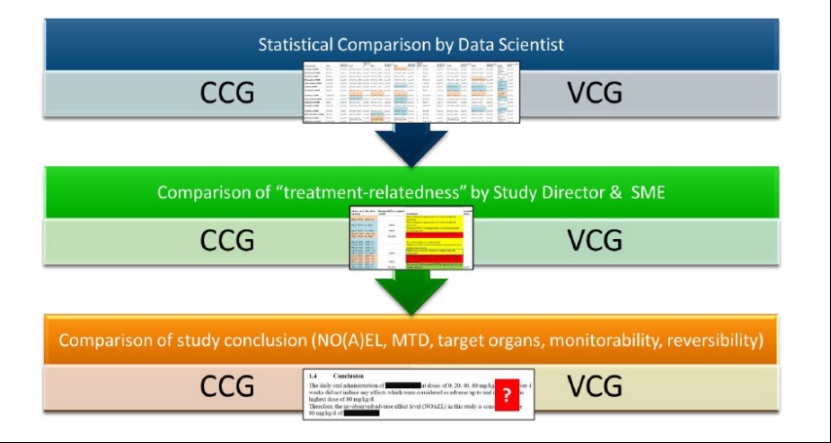
EMA于3月31日发布了一份认证意见草案,认定在大鼠剂量范围探索研究中使用虚拟对照组(virtual control group,VCG)的可行性,旨在减少或完全替代传统非临床研究中的动物使用。
正如2025年3月EMA认证了全球首个AI工具用于临床试验结果评价,这次EMA首次认证新方法学(NAM),对于动...
|

|
英国 MHRA 拟预先审评无动物非临床申报资料
2026.04.14
3月25日,MHRA发布对采用非动物方法的药品的方针,旨在进一步推进药物开发中动物试验的淘汰进程。该机构通过提供非动物数据的预先审评机制,并明确此类数据的评估标准,激励申办者基于非动物试验证据提交上市申请。
此举与英国政府减少药物开发中动物使用的长期战略相契合,也是继3月18...
|

|
国际药政每周概要:FDA 生物标志物验证指南,进一步...
2026.04.14
【非临床与临床研究】
4.10,【FDA】生物标志物的生物分析方法验证
4.10,【PMDA】关于“口服制剂食物影响评估的考虑要点(早期考虑)
【药学研究】
本周BE指南:
【注册与变更】
4.9,【FDA】SOPP 8216 快速通道开发计划-认定和管理
4.9,【FDA】SOPP 8212:...
|

|
FDA 可能放松监管,“灰色”多肽市场有望转正
2026.04.13
FDA正趋向于允许配药药房生产14种此前被禁止的多肽(peptides)。美国卫生部(HHS)小肯尼迪公开推动政策逆转,其在播客中表示个人使用这些产品治疗损伤“取得了非常好的效果”。他认为应解除限制,以便人们获得“良心厂家”(ethical suppliers)的产品。
若FDA最终解除限制,此前...
|

|
日本和越南拟设 FDA 海外办公室
2026.04.13
FDA计划在亚洲增设两个海外办公室,选址分别为日本(东京)和越南(河内)。FDA在其2027财政年度预算申请中提出增加250万美元预算及5名全职等效员工,以支持上述办公室的设立。
根据FDA提交给国会的预算说明文件,新办公室将执行食品和医疗产品(medical product)的现场检查任务,...
|

|
国内药政每周导读:国务院健全药价机制,IND 和 NDA...
2026.04.13
【非临床与临床研究】
4.8,【CDE】关于发布《药物临床试验申请临床评价技术指导原则》的通告(2026年第27号)
4.8,【CDE】关于发布《药物上市申请临床评价技术指导原则》的通告(2026年第26号)
【CMC药学研究】
4.10,【CDE】关于公开征求《化学药品创新药分段生产药学...
|

|
【周末杂谈】AI 创造新职业
2026.04.12
前线部署工程师(FDE),融合了开发、顾问和销售人员的角色
去年12月,英国《经济学人》杂志刊登了题为“就业末日?言之尚早。AI 正在创造全新的职业(Job apocalypse? Not yet. AI is creating brand new occupations)”的文章。下面是文中配图,以及两段内容的翻译、编辑...
|

|
【识林心得】几个可以长期收藏的页面
2026.04.11
在药品全生命周期中,ICH权威指南、审评思路、属地政策和国际GMP标准是企业最核心的信息需求,但这些官方文件往往分散、更新频繁,如何快速锁定“对的那一份材料”成为日常难题。
识林基于长期跟踪和系统整理,制作了多个专题索引页面,旨在将分散的信息集中呈现,降低检索成本。以下四个...
|

|
PDUFA VIII:“美国优先”达协议,本土 I 期临床药...
2026.04.10
最近释出的3月份《处方药用户付费法案》(PDUFA VIII)谈判会议纪要显示,FDA与行业代表已达成原则一致。将临床试验“锚定”(anchored)在美国本土开展I期研究的申办者,其药品上市申请的用户付费可减半。
按2026财年标准,需要提交临床数据的新药申请(NDA)或生物制品许可申请(BLA...
|

|
中国香港药监启动“第一层审批”,从化药补充申请开始
2026.04.10
中国香港药剂业及毒药管理局(PPBHK)于3月31日启动第一期第一层审批,从化药的“延伸应用”(补充申请)开始,并在同日发布《药品注册申请指南:新药注册申请》(版本1.0)及《药品注册申请指南:经第一层审批途径提交化学元素新药注册申请的特定要求》(版本1.0)。
PPBHK通过公...
|

|
新加坡 HSA 总结2025年药品 GMP 检查缺陷
2026.04.09
新加坡卫生科学局(HSA)近期公布了《2025年生产商 GMP 缺陷趋势》报告。本次报告覆盖了多元化的生产商群体,其中治疗类产品(TP)占比最高,达43%,其次为中成药(CPM,26%)、活性成分(即API,15%)及细胞、组织和基因治疗产品(CTGTP,13%)。
2025年的检查结果显示,尽管...
|

|
欧盟规划修订 GMP 指南章节附录,AI GMP 年底定稿
2026.04.09
3月23日,EMA发布《检查员工作组3年工作计划2026-2028》,阐述了GMP/GDP检查员工作组(GMDP IWG)在2026年至2028年期间的常规活动,包括5个重点行动和系列GMP文件的更新规划。
5个重点行动:改进检查规划,推广依赖检查与远程评估
在检查员培训方面,IWG将制定并维护GMDP IWG...
|

|
FDA 寻求72亿美元预算,披露更多政策手段
2026.04.08
美国白宫通过2027财年预算提案并提交国会,合计高达72亿美元,同时明确了FDA的一系列政策目标。尽管提案中只提“让美国再次健康”(MAHA),但有美媒称其核心诉求旨在支持美国生物技术产业与中国竞争。
药企缴费与财政拨款大致各半,但FDA越来越多依赖前者
FDA预算主要分为用户付...
|

|
PMDA 阐明如何利用“既定条件”预先设定变更级别
2026.04.08
3月24日,PMDA发布《关于预先设定被认定为既定条件的药品(化学品)生产工艺参数的变更分类的基本考虑要点(早期考虑)》,旨在澄清化学药生产过程中被判定为既定条件(Established Condition, EC)的工艺参数如何在初始申报时预设变更分级。
在EC的具体操作方面,FDA的《ICH Q12 ...
|

|
国际药政每周概要:FDA 推进 DHT 临床应用,EMA ...
2026.04.07
【非临床与临床研究】
3.31,【PMDA】关于“小样本量临床试验注意事项”(早期考虑)
3.31,【EMA】在临床前研究中实施虚拟对照组的标准操作规程
3.31,【EMA】关于肺动脉高压治疗药物临床研究指导原则的儿科附录
3.31,【EMA】关于修订肌萎缩侧索硬化(ALS)治疗药物临...
|

|
EMA 指导公共卫生突发状况下如何开展临床试验
2026.04.07
3月4日,EMA发布《公共卫生突发事件期间临床试验实施指南》征求意见稿。该指南针对公共卫生突发事件(Public Health Emergency,PHE)背景下临床试验的启动、变更及实施关键环节调整,提供了具体操作性框架。本指南充分吸收并整合了新冠肺炎(COVID-19)大流行期间的实践经验,旨在将...
|
|
真实世界数据质量如何评价?EMA 划定框架并提供示例
2026.04.07
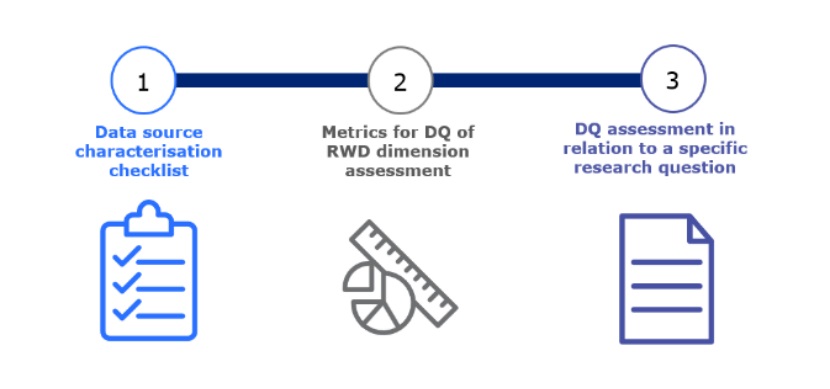
3月27日,EMA定稿工作文件《欧盟药品监管数据质量框架:应用于真实世界数据》,基于“欧洲药品监管网络数据质量框架”(EMRN DQF)以评估支撑真实世界证据(RWE)的真实世界数据(RWD)质量(即,RW-DQF),提供详细的可操作的技术建议,旨在促进高质量的RWE用于支持监管决策。
尽...
|

|
国内药政每周导读:AI+ 药品监管,沟通交流修订,做...
2026.04.06
【CMC药学研究】
3.30,【NMPA】关于发布仿制药参比制剂目录(第一百零三批)的通告(2026年第8号)
【注册与变更】
3.30,【NMPA】部署完善药品附条件批准制度有关工作
3.30,【CDE】关于上线注册服务平台的通知
4.3,【CDE】关于修订发布《国家药品监督管理局药品审...
|

|
外行用 AI 治好了患癌宠物狗?制药界和科技界的“凉...
2026.04.06
一只患有皮肤癌的斯塔福郡斗牛梗犬Rosie,近期成为AI生物技术领域的讨论焦点。广为流行的叙事是,其主人Paul Conyngham利用ChatGPT、Grok等大语言模型(Large Language Models,LLM)为宠物Rosie开发定制信使核糖核酸(messenger RNA,mRNA)癌症疗法,疗效显著。
在这个故事席卷科...
|

|
【周末杂谈】AI 在 GMP 上的应用,在重蹈 Part11...
2026.04.05
让AI参与GMP控制,而不仅是单纯用于降本增效,会带来很多问题
Déjà vu,源自法语,意为“已见过”,表述的是一种强烈而短暂的错觉,让人感觉当前的情境仿佛早已经历过,尽管明知这是全新的体验(往往是不好的体验)。这是一位美国GMP领域资深人士,最近谈起如何监管AI在GMP上的应用时...
|