
|
FDA 发布2025年度仿制药科研报告,分享大量研究成果
2026.04.01
3月25日,FDA发布《2025财年GDUFA科学与研究报告》,系统梳理了仿制药用户付费法案(GDUFA)科学与研究项目在2025财年的资助课题、技术进展与监管转化成果。
报告长达117页,分为9个领域,包括大量研究课题描述、进展和文献链接,为全球仿制药行业提供了详实的技术参考。篇幅所限,下...
|

|
欧洲药典13.1更新内容概要及13.2前瞻
2026.04.01
欧洲药典(Ph. Eur.)于3月初发布第13版第1期(13.1)更新内容,其中新增和修订的文本于2027年1月1日生效,须在此日期前实施。勘误文本不得迟于2026年5月31日前采纳。
3月中旬,欧洲药典委员会(EPC)召开第184届会议,会上通过的50个欧洲药典文本将在第13版第2期(13.2,2026年...
|

|
国际药政每周概要:EMA 定稿生物类似药临床简化,RWD...
2026.04.01
【非临床与临床研究】
3.25,【MHRA】MHRA 对采用非动物方法的药品的方针
3.27,【EMA】欧盟药品监管数据质量框架:应用于真实世界数据
3.27,【EMA】关于在生物类似药开发中采用定制的临床方法的思考性文件
【药学研究】
3.24,【EDQM】欧洲药典 13
【注册与变更】
...
|
|
EMA 试点基于 PICS 指南检查变更管理,为 Q12应用...
2026.03.31
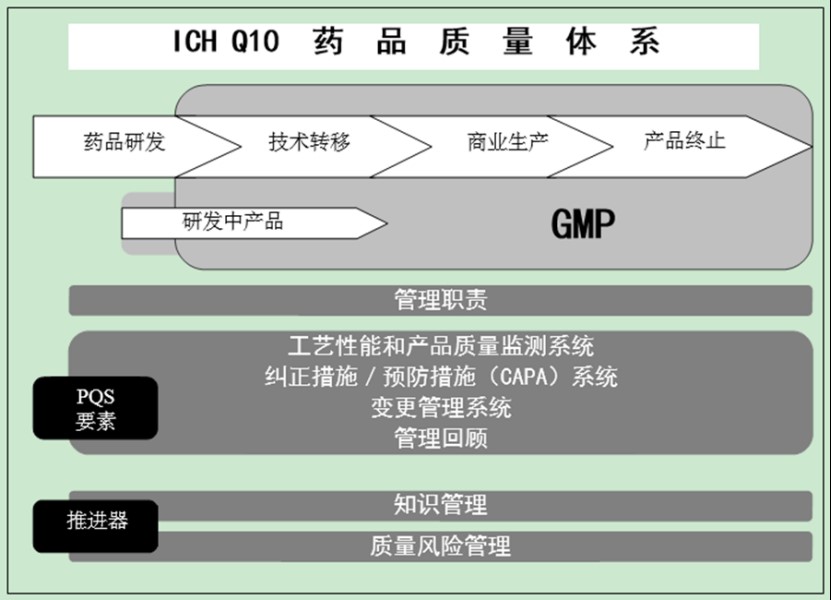
3月26日,EMA启动药品质量体系(Pharmaceutical Quality System,PQS)有效性试点项目。根据该项目,上市许可持有人(MAH)和生产企业可提名其生产场地,接受欧洲经济区(EEA)GMP检查员开展的PQS有效性现场评估。
试点旨在评估生产场地如何展示其PQS有效性,从而应用ICH《Q12:药...
|
|
ICH 更新系列培训 PPT,适配 Q9(R1)全部工具和场...
2026.03.31
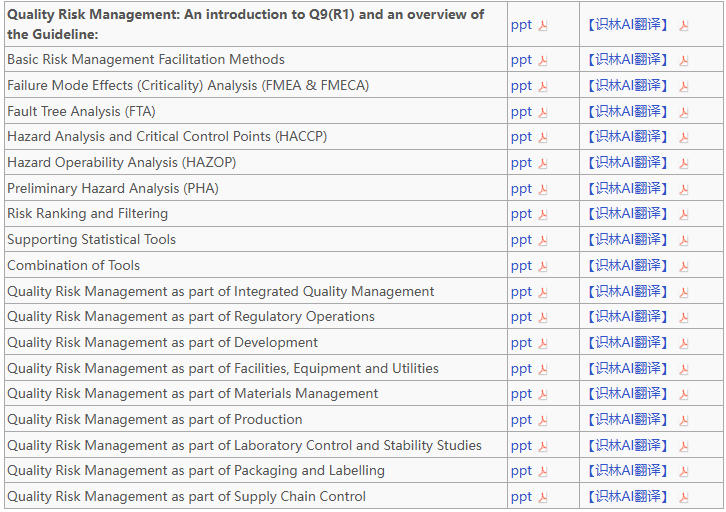
3月20日,ICH完成了对全套培训资源包(Briefing Pack)的更新,适配《Q9(R1):质量风险管理》。此次更新彻底取代了自 2006 年以来沿用多年的旧课件,为业界提供全面而权威的实操指导。
在一份纲领性PPT后,剩余18份PPT分为两大核心模块(完整目录见文末):
9个方法与工具涵盖Q...
|

|
国内药政每周导读:加速构建药品追溯体系,现代物流规...
2026.03.30
【注册与变更】
3.24,【NMPA】关于同意福建、河南省药监局开展优化药品补充申请审评审批程序改革试点的批复
【生产质量】
3.24,【NMPA】关于暂停进口、销售和使用 Vasudha Pharma Chem Limited 盐酸洛哌丁胺原料药和 Alchem International Private Limited 利血平、...
|

|
Makary 的 FDA 一周年,其2026目标是力保美国领先
2026.03.30
在FDA局长Martin Makary履新一周年之际,FDA拒绝了美国媒体PinkSheet对Makary进行就职周年专访的请求,称时间安排不可行。但Makary还是以书面形式回应了有关其第一年工作及第二年优先事项的提问(见文末)。
自2025年3月28日宣誓就任FDA局长以来,Makary推动了一系列药品审评与监管...
|

|
GAO 敦促 FDA 发指南管控 AC 会利益冲突
2026.03.30
3月24日,美国会政府问责局(Government Accountability Office,GAO)发布专题调查报告,并建议FDA提供时间表,制定针对其咨询委员会(Advisory Committee,AC)成员潜在经济利益冲突管理的指南文件。
GAO在调查中重点审查了FDA负责阿片类药物相关事务的两个AC会。调查结果显示,自2...
|

|
【周末杂谈】先进技术并未改进审批的质和量
2026.03.29
值得关注AI应用效果的人参考的、深知审批关键环节和企业实际需求的评论
无论是专业技术性应用,如基于问题的审评(QbR)、质量源于设计(QbD)、知识辅助评估和结构化申请(KASA),还是信息技术(IT)和知识工程(KE)应用,如eCTD、机器学习、大语言模型(后两者可用时髦的词AI来统称)...
|

|
【直播】26年3月全球法规月报划重点
2026.03.28
识林2026年3月报直播如期而至,并同步推出3月报。本次直播聚焦3月全球主要监管机构的重点法规,并挑选影响力较大的文件做重点简介。短短40分钟,轻量而轻松,旨在帮助大家回顾上个月的监管重点,加深理解或是查缺补漏。
月报获取渠道:
会员:关注直播当日(4月8日,周三)的【最近更...
|

|
【课程与会议】近期更新的重点课程和4-5月会议预告
2026.03.28
近期更新重点课程
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的1000+门课程7000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,及供应商技术介绍专业课程。除视频内搜索、收藏、评论功能外,...
|

|
EMA 将三项加速审评试点工具整合至 PRIME
2026.03.27
EMA于2026年3月18日发布声明,正式推出三项新监管工具,旨在优化“优先药品(PRIority Medicines,PRIME)”计划下未满足临床需求的药物研发效率。这三项工具此前已通过为期两年的试点验证,现作为永久性措施纳入PRIME计划。
三项新工具分别为:监管路线图与产品开发追踪器(regulatory...
|

|
ECA 呼吁重构 ATMP 质量标准,引入“以患者为中心...
2026.03.27
3月12日,欧洲合规学会(ECA)发布了一份关于先进治疗药品(Advanced Therapy Medicinal Products,ATMP)质量标准制定的思考性文件,探讨了在ATMP,特别是自体细胞治疗产品开发中,如何融入“以患者为中心”(patient-centricity)和“标准源于设计”(Specification by Design,S...
|
|
EMA 指导 3D 打印固体口服制剂 GMP 实践
2026.03.26
3月24日,EMA发布《口服固体制剂 3DP 技术(增材制造技术)实施问答》(Questions & Answers on the Implementation of 3DP Technology (Additive Manufacturing Technology) for Solid Oral Dosage Forms)。该文件针对3D打印(three-dimensional printing,3DP)...
|

|
ICH 规划先进制造指南,先从工艺建模和 AI 入手
2026.03.26
近日,ICH采纳并发布思考性文件《提议的ICH指导原则工作以促进先进药品制造的采用》,旨在制定全球范围内协调统一的监管指南,切实推动先进制造技术在药品研发与生产中的应用与规范。
ICH指出当前指南无法完全覆盖部分新兴制造领域,亟需制定新指南或对现有指南进行修订。这也是广大...
|

|
欧洲药监要求药企主动监测供应商的警告信
2026.03.25
近日,盛德律师事务所(Sidley Austin)的生命科学领域律师团队发表博客文章并接受媒体采访,主题是欧洲监管部门要求制药企业需建立系统以监测FDA向其关键供应商发出的警告信。
尽管律师称欧盟药监部门与英国MHRA不会因为FDA警告信而自动触发检查,但均倾向于药企自行主动监测供应商...
|

|
FDA 警告信罕见公开触目惊心的现场照片
2026.03.25
3月17日,FDA公布了一份3月12日向位于印度达曼的Patcos Cosmetics Pvt.Ltd.(以下简称 Patcos)发出的警告信。该信函披露了 FDA 检查员在2025年7月14日至18日的现场检查中发现的严重质量缺陷。
这封警告信的特别之处在于,FDA罕见地刊载了多张展示该工厂恶劣生产环境的照片,...
|

|
白宫发布 AI 政策总纲,灵活监管以保全球领先
2026.03.24
3月20日,美国白宫发布《国家人工智能政策框架》(National Policy Framework for Artificial Intelligence, NPFAI)立法建议文件,旨在确立统一的人工智能(Artificial Intelligence, AI)联邦政策框架,消除各州监管标准不一产生的碎片化现象,确立美国在 AI 领域的全球主导地...
|

|
美众议院听证会聚焦中国生物技术产业挑战
2026.03.24
3月18日,美国众议院中美竞争特设委员会举行主题为“从实验室到药柜:中国如何掌控我们的药物市场”(From the Science Lab to the Medicine Cabinet How China is Cornering the Market on Our Medicines)的听证会。本次听证会邀请四位行业及政策专家出庭作证,涵盖生...
|

|
国际药政每周概要:FDA 力推动物试验替代,白宫 AI...
2026.03.24
【非临床与临床研究】
3.17,【EMA】临床药理学和药代动力学问答:更新
3.16,【PMDA】在癫痫治疗中,针对暂时无法口服给药的患者的、与口服制剂具有相同有效成分的静脉注射制剂的临床开发考虑事项(早期考虑)
3.16,【PMDA】前列腺特异性膜抗原靶向正电子发射断层扫描(PSMA...
|