
|
国际药政每周概要:FDA批准强生BCMACD3双抗,欧盟启动...
2022.11.01
【注册、审评、审批】
10.25【FDA】FDA 批准 teclistamab-cqyv 治疗复发或难治性多发性骨髓瘤
【创新研发与临床】
10.25【EMA】原始数据概念验证行业试点信息
10.28【EMA】原始数据概念验证行业试点问答
10.27【MHRA】提高临床试验许可(CTA)申请的效率,减少后续...
|

|
FDA 启动 CMC 开发和准备试点计划,促进研究性新药...
2022.10.31
美国 FDA 于 10 月 31 日在联邦公告上发布通告,宣布启动化学、制造和控制(CMC)开发和准备试点(CDRP)计划,以基于患者更早获得产品的预期临床获益,在必要情况下促进在研究性新药(IND)申请下产品的加速 CMC 开发。
FDA 表示实施这一试点计划是为了帮助一些被监管产品做好...
|

|
国内药政每周导读:药品召回办法,临床方案审评规范,...
2022.10.31
【创新药与临床研究】
10.25,【CDE】关于公开征求《慢性乙型肝炎治疗药物临床试验技术指导原则》意见的通知
10.25,【CDE】关于公开征求《新药临床安全性评价技术指导原则》意见的通知
10.26,【CDE】关于公开征求《人乳头瘤病毒疫苗临床试验技术指导原则(征求意见稿)》...
|
|
【周末杂谈】鼻喷剂治心律不齐
2022.10.30
药的临床价值高,企业的市场估值低,竟有这等事?
10月17日,加拿大Milestone制药公司宣布,其在研的鼻腔喷雾药物Etripamil在刚完成的III期临床试验中,显示可有效治疗患有阵发性室上性心动过速(PSVT)的患者。该病的特征是突然开始和停止的快速心跳发作,虽不危及生命,但导致心悸、...
|

|
轻松一刻 - 以患者为中心?
2022.10.29
识林轻松一刻,意在以漫画形式,展现药企人酸甜苦辣,博得识林读者会心一笑之余,也希望带来些许回味与思索。
识林欢迎读者提供素材,可以是几段对话,也可以是一个故事。有合适的,识林会与您联系,一起优化完善,并由我们的设计师转化为漫画,在识林平台上分享给大家。
...
|

|
欧盟委员会表示初步调查显示 Teva 违反反垄断法
2022.10.28
欧盟委员会经过三年的初步调查认定 Teva 非法使用不同的策略来阻止竞争对手推出其最畅销的多发性硬化症治疗药 Copaxone(醋酸格拉替雷)的仿制产品。
另外,欧盟委员会还确定,Teva 针对医院和医生开展宣传活动,以制造对类似多发性硬化症药物的“错误认知”。
Copaxone 是一种...
|

|
赛诺菲将利用数字孪生技术优化未来疫苗工厂生产
2022.10.28
赛诺菲在法国和新加坡即将推出的“EVolutive”疫苗设施中增加了一层新技术,其正在利用达索系统(Dassault Systèmes)的模拟 3D 空间,通过数字孪生(digital twin)的力量优化生产。
赛诺菲此次合作的达索系统是一家法国软件公司,其在新闻稿中表示,达索的 3DEXPERIENCE ...
|

|
FDA 新发布四份局部仿制药指南草案,涉及体内BE、Q3...
2022.10.27
美国 FDA 最近发布了四份关于在简化新药申请(ANDA)下提交的局部仿制药产品的新指南草案,包括:局部皮肤用皮质类固醇体内生物等效性指南,ANDA 下提交的局部药品的物理化学和结构(Q3)表征、体外释放试验研究、体外渗透试验研究。
下面我们一一来看看这些指南:
局部皮肤...
|

|
2022 年 Biocon 马来西亚生物类似药工厂 483 解...
2022.10.27
美国FDA于 2022年8月11日至8月30日期间检查了印度Biocon生物在印度的两个工厂和马来西亚的一个工厂,此次检查是对生物类似药贝伐单抗、重组胰岛素和门冬胰岛素进行的预批准检查,并对生物类似药曲妥珠单抗进行产能扩展检查。
印度生物药巨头Biocon从2018年2月就开始积极推动马来西亚...
|
|
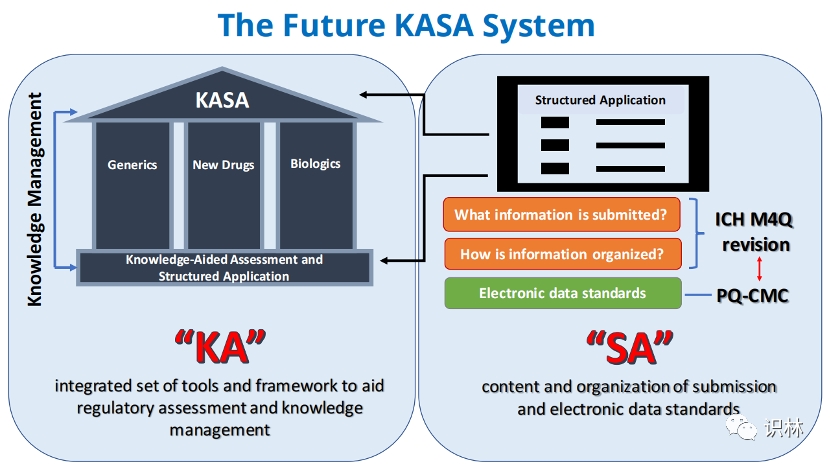
申报和审评数字化变革的回顾与展望:KASA,PQ CMC,Ac...
2022.10.26
美国FDA将在11月2-3日举行一场特殊的专家会,讨论质量成熟度和KASA。FDA 将在这场会上寻求业界和公众对KASA愿景的意见,并计划在未来5年内扩大KASA。另外,第6次2022年FDA/PQRI(Product Quality Research Institute,药品质量研究协会)联合会议预期将在年底举办。
在这两次重...
|

|
Catalent 比利时工厂再收 483,涉及数据、设备和 Q...
2022.10.26
Catalent 位于美国印第安纳州的工厂在收到来自 FDA 的 483 仅一个月后,其位于欧洲比利时的工厂同样收到了 483。
FDA 于今年 8 月份在 Catalent 位于比利时首都布鲁塞尔的生产场地进行检查后发布的 483 报告中列出了涉及无菌区空气过滤器问题、用于灌装的洁净间内 HVAC...
|

|
国际药政每周概要:FDA发布多篇局部药品相同性和生物...
2022.10.25
【CMC 与仿制药】
10.21【FDA】BE 指南 新增8篇,修订72篇
【注册、审评、审批】
【创新研发与临床】
10.20【FDA】指南定稿 临床研究中多个终点
【GxP 与检查】
【药典相关】
【监管综合】
10.17【EU】全球药品供应链的脆弱性 - 关于药品供应安全的结构性对...
|

|
FDA 神经退行性疾病的人类基因治疗定稿指南
2022.10.25
美国 FDA 于 10 月 21 日发布了“神经退行性疾病的人类基因治疗”定稿指南,为开发相关产品的生物制药公司提供化学、生产和控制(CMC)、临床前研究以及临床试验设计等方面的指导。
该定稿指南以 2021 年 1 月的指南草案为基础,同意了行业反馈的一些要求,包括修改指南中关...
|

|
国内药政每周导读:GLP认证征求意见,医保目录专家评...
2022.10.24
【创新研究】
10.21,国家药监局综合司公开征求《药物非临床研究质量管理规范认证管理办法(征求意见稿)》意见
【药学研究与仿制药】
10.20,【NMPA】关于发布仿制药参比制剂目录(第六十一批)的通告(2022年第52号)
【监管综合】
10.16,【国家医保局】关于2022年...
|

|
FDA就临床试验中多个终点的问题提供指导
2022.10.24
美国 FDA 于 10 月 20 日发布了“临床试验中多个终点”定稿指南,以最大限度减少对药物疗效做出错误结论的可能性。
FDA 表示,“在药物开发中进行的大多数临床试验都包含多个终点,以评估药物疗效并记录药物对一种或多种疾病特征产生有利影响的能力。当在一次试验中分析多个终点...
|

|
【周末杂谈】药品上市难,撤市也难
2022.10.23
药品撤市,不仅是科学、商业和公卫问题,还是社会问题
这周三,美国FDA召开公开听证会,讨论早产预防药Makena的撤市问题。会后专家表决141,支持FDA撤销对Makena的加速批准。这距离FDA提出撤销批准已2年,距离最初的加速批准近12年。虽然有了专家的表决,距离FDA最终做出撤销的决定,...
|

|
线上讲座:细胞治疗产品共线生产可行性策略分析与讨论
2022.10.22
共线生产模式,有着其经济性的价值,同时存在一定的质量风险。2021年11月12日NMPA审核查验中心发布了《药品共线生产质量管理指南(征求意见稿)》,旨在为指导和规范药品共线生产管理,识林曾邀本指南起草参与者之一的夏禄华老师,联合多位GMP检查员、行业专家于2022年5月25日进行分析...
|

|
【识林向导招新】2022年四季度,分享知识,畅游识林!
2022.10.22
很高兴认识您,亲爱的识林用户。
识林是制药业一站式法规技术学习平台,专注于药品全生命周期的系统性知识,为求知型人才、学习型企业、知识型产业提供知识驱动的工具和服务。
现在,识林诚邀大家成为“向导”,帮助更多识林求知者游历知识森林,一起成长,共同精进。
什么是向导...
|

|
仿制药商要求FDA修订ANDA增补指南以减少归类为主要缺...
2022.10.21
仿制药生产商最近敦促美国 FDA 修改其关于简化新药申请(ANDA)增补的指南,以将更少的缺陷归类为“主要”缺陷并避免扩大审评轮次。
FDA 建立了一个公开卷宗以征求公众对 2018 年 7 月行业指南“ANDA 申报 – GDUFA 下的增补指南”中附录 A 的意见。ANDA 增补指南定义了...
|

|
FDA 启动推进真实世界证据计划并更新复杂创新试验设...
2022.10.21
美国 FDA 于 10 月 19 日更新了有关根据处方药使用者付费修正案(PDUFA VII)协商的两个项目的最新进展,旨在让申办人有机会尽早与 FDA 沟通并刺激创新。这两个项目分别为:
旨在使用真实世界证据(RWE)来支持产品有效性或满足批准后研究要求的“推进真实世界证据计划”;
...
|