
|
接任 CDER 数周后,Pazdur 计划离职
2025.12.03
12月2日,多家外媒报道FDA药品审评与研究中心(CDER)新任主任Richard Pazdur在履新仅三周后决定退休。
此前11月11日,CDER前主任George Tidmarsh因面临内部审查压力而辞职后,Pazdur一开始拒绝,但数日后还是决定接手。
也许这一新闻并不如一些媒体所称的那么“意外”。《华盛...
|
|
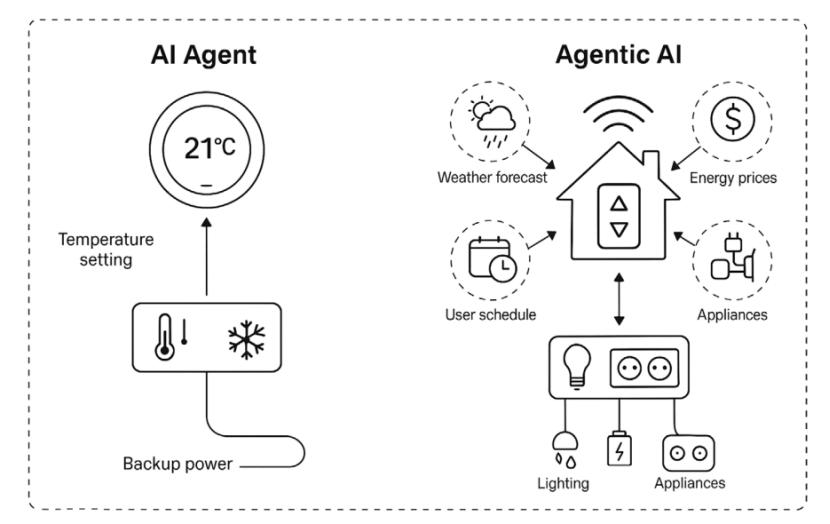
FDA 部署“智能体式 AI”能力平台,鼓励员工自建智...
2025.12.03
FDA于12月1日宣布,其已面向全体员工部署了智能体式人工智能(Agentic AI)能力平台。FDA将此次部署视为其机构内部AI应用战略迈出的关键一步,旨在通过构建更复杂的AI工作流来协助处理多步骤任务,从而提升药品及医疗器械等受监管产品全生命周期管理的效率与科学性。
不是新Elsa,可...
|

|
2025罕见病药物审评:FDA 临床审评的“松紧”把握
2025.12.02
近期,FDA在罕见病药物审批中展现出更为严格的监管姿态,但批准节奏并未放缓。
根据Pink Sheet的分析报告,过去12个月内,FDA针对罕见病适应症的药物发布了8份完全回应函(Complete Response Letter,CRL),均指出申请存在临床问题。另一方面,单一试验辅以确证性证据的策略仍常...
|
|
研究分析六个监管地区非肿瘤孤儿药审批,呼吁监管互认
2025.12.02
国际罕见病研究联盟(IRDiRC)在11月发表综述文章《全球非肿瘤孤儿药批准:所需证据类型与获批时间》,系统回顾了2021年至2022年间在六大监管区域包括美国FDA、欧盟EMA、日本MHLW/PMDA、加拿大HC、澳大利亚TGA及沙特SFDA首次获批的53种非肿瘤孤儿药,从证据要求与审批时间两个维度进行...
|

|
国际药政每周概要:FDA 更新医用气体 cGMP,ICH 发布...
2025.12.02
【早期开发与临床】
11.28,【ICH】E22 患者偏好研究的一般考虑
11.28,【ICH】E23关于使用真实世界证据(RWE)支持监管决策的考虑,重点关注药品有效性:概念性文件
11.28,【ICH】M18用于确定生物类似药开发项目中疗效比对研究效用的框架:概念性文件
【CMC 药学研究】...
|
|
ICH 拟制定 M18,协调全球药监豁免生物类似药临床
2025.12.01
11月28日,ICH发布概念性文件,启动一份全新的多学科指南《M18用于确定生物类似药开发项目中疗效比对研究效用的框架》(暂译)的制定,为生物类似药开发项目中疗效比对研究(CES)的必要性评估提供科学、一致的国际标准。
豁免CES的考量:区分力不足,分析技术进步,冗余成本
ICH...
|

|
ICH 新加坡大会:新成员和观察员,新指南启动
2025.12.01
2025年11月18日至19日,ICH在新加坡召开全体大会。本次会议与12个工作组会议同期举行,之前还举行了ICH管理委员会(Management Committee)与MedDRA管理委员会(MedDRA Steering Committee)的预备会议。
会议期间,ICH宣布接纳尼日利亚国家食品药品管理局(NAFDAC)与南非药品管理局(...
|

|
国内药政每周导读:疫苗电子化记录指南重要修订,临床...
2025.12.01
【早期开发与临床】
11.24,【CDE】关于公开征求《药物临床试验计算机化系统和电子数据指导原则(征求意见稿)》意见的通知
11.25,【CDE】关于公开征求《“三结合”中药注册审评证据体系下临床试验的一般原则(征求意见稿)》意见的通知
【生产质量】
11.28,【CFDI】公...
|

|
【周末杂谈】英国《经济学人》赞中国药监
2025.11.30
从文章的用词“agility, nimble和permissive”和未用词,看赞扬的实诚性
著名的英国《经济学人》杂志本期封面文章题目是“中国接下来将主导什么领域?”,并配有插图如下,显示我国在创新药和其它高科技领域举世瞩目的进展。值得注意的是,文章淡化政府经济手段的作用,重谈政府监管的...
|

|
【课程与会议】近期更新的重点课程和12月会议预告
2025.11.29
近期更新重点课程
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的800+门课程7000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,及供应商技术介绍专业课程。除视频内搜索、收藏、评论功能外,...
|

|
MRCT 如何把握多变的标准治疗?最新白皮书提供思考框...
2025.11.28
近日,识林收录了一份由癌症研究之友(Friends of Cancer Research)组织吉利德(Gilead)、安进(Amgen)、默克(Merck)等多家跨国药企和梅奥诊所(Mayo Clinic)等医疗机构专家共同起草的一份白皮书《多区域临床试验:应对标准治疗的差异白皮书(2025)》,专门针对这一业界关注...
|
|
PMDA 研究探讨亚洲 MRCT 合作与种族因素影响
2025.11.28
日本PMDA在今年9月参与发表综述文章《日本对通过亚洲多区域临床试验合作促进药物研发的看法:来自监管研究的启示》,系统总结了日本政府过去15年来资助的监管科学研究成果,探讨了种族因素对药物反应的影响以及亚洲多区域临床试验(MRCT)面临的挑战。
东亚人群药代动力学相似
研...
|

|
美国会智库呼吁重构生物技术科研体系以应对中国竞争
2025.11.27
近日,美国国家新兴生物技术安全委员会(National Security Commission on Emerging Biotechnology, NSCEB)向国会提交了题为《科学的未来》(The Future of Science)的政策建议报告。这份报告标志着美国在生物技术这一战略关键领域的政策导向,正从单纯的资金投入,转向对科...
|
|
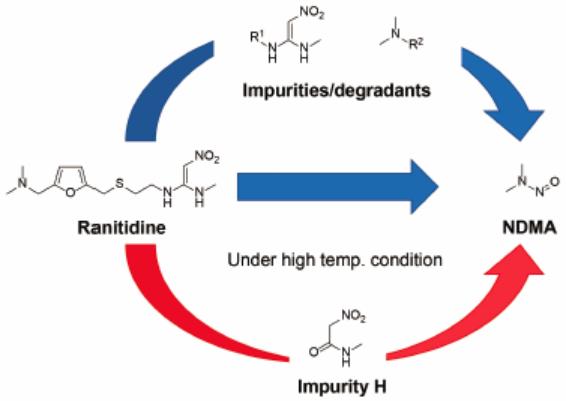
新处方解决亚硝胺问题,雷尼替丁重回美国市场
2025.11.27
11月24日,FDA发布公告,宣布批准经改良处方的雷尼替丁(ranitidine)片剂上市。FDA未明确其厂家,有报道称是印度仿制药企VKT Pharma,而非原研GSK。
此举标志着该重要抑酸药物在退出市场五年后重新回归。FDA称此次批准基于全面的安全性评估,新制剂通过生产工艺改进,解决了此前存在...
|

|
【直播】25年11月全球法规月报划重点
2025.11.27
识林月报直播如期而至,本次直播聚焦11月全球主要监管机构的重点法规,并挑选影响力较大的文件做重点简介。短短40分钟,轻量而轻松,旨在帮助大家回顾上个月的监管重点,加深理解或是查缺补漏。
直播信息速递:
直播时间:12月4日(周四)16点
直播时长:40分钟
直播平台:识林...
|

|
FDA 分析儿科药物开发失败原因,剂量选择首当其冲
2025.11.26
FDA CDER部门在10月份发表综述文章《2015-2022年提交FDA的未成功儿科药物研发项目试验回顾》,系统梳理分析了2015至2022年间申报未获批准的儿科药物研发项目。文章指出,自2002年《儿童最佳药品法案》(BPCA)与2003年《儿科研究公平法案》(PREA)实施以来,儿科药物研发取得显著进展...
|

|
EMA 更新临床非劣效性与等效性对比指南
2025.11.26
11月13日,EMA发布《临床试验中的非劣效性对比和等效性对比指南》草案,征求意见截至2026年5月31日。此前EMA曾于2024年2月发布概念性文件,现行非劣效指南还是早在2005年7月的《非劣效界值选择指南》和2000年7月的《优效性与非劣效性之间转换的考虑要点》。
指南适用范围包括旨在证明...
|

|
六个基因疗法技术有望获 FDA 平台技术认定
2025.11.25
继撤销Sarepta的认定后,FDA于10月授予Krystal平台技术认定,显示其平台技术认定项目在经历波折后重回正轨。
FDA于2024年5月发布平台技术认定项目的指南草案,定义平台技术为“被充分理解且可复制”的方法,对药品的结构或功能“至关重要”,且应适用于其他药物,实现“标准化生产或...
|

|
FDA 开发 OCMQ 系统来提升临床试验安全性分析能力
2025.11.25
FDA的CDER下属新药办公室(OND)研究人员在9月份发表文章《用于临床试验数据安全性分析的新药办公室定制医学查询的开发与使用》,OND开发了更具临床意义的用于上市前药品安全性评估的定制医学查询(OCMQ)系统,现包含104个定制化不良事件(AE)术语分组。该系统的开发基于对1960年至201...
|

|
国际药政每周概要:FDA 提供邮件沟通机会,更新 cGM...
2025.11.25
【早期开发与临床】
11.21,【PMDA】银屑病关节炎治疗药物临床开发需考虑的要点(早期考虑)
【CMC 药学研究】
11.21,【WHO】替代或取消生物制品质量控制动物试验的指南
【注册与变更】
11.19,【FDA】FDA 试点加快会议纪要澄清流程
【生产质量】
11.21,【FDA...
|