
|
【更新提示】识林一周回顾(20181014-1020)
2018.10.21
【CDE】中美两国CAR T细胞治疗临床试验的比较分析(10.19)
CAR T细胞治疗是近年来发展速度最快的癌症免疫疗法之一,中国和美国是世界上CAR T细胞临床试验开展最为活跃的国家,两国在临床试验登记网站“clinicaltrials.gov”上登记的临床试验数量占全球CAR T细胞临床试验的90%以上...
|

|
FDA 向 ICH 提议协调全球仿制药批准标准
2018.10.20
美国 FDA 于 10 月 18 日宣布正在向 ICH 提出一项建议更好地协调仿制药的科学和技术标准。该提议旨在允许仿制药研发商实施单一的全球药物研发计划以及提交申请的通用要素,以在多个市场同时批准。
FDA 局长 Scott Gottlieb 表示,“这将使原本只在一个地区寻求仿制药批准的...
|

|
2018 秋季统一议程:FDA 推进健康与安全的新监管工...
2018.10.19
(译自 FDA Voice https//www.fda.gov/NewsEvents/Newsroom/FDAVoices/ucm623619.htm “Fall 2018 Unified Agenda FDA's New Regulatory Work to Advance Health and Safety” 2018 年 10 月 17 日,作者:Scott Gottlieb,医学博士,美国 FDA 局长)
2018 年...
|

|
国际药品危机事件管理的法律、商务和技术考虑
2018.10.18
IPEM – 识林 专题课 (第二轮通知)
国际药品危机事件管理的法律、商务和技术考虑
2018年11月9-10日,北京
识林资讯 2018年9月30日,发布了专题课的首轮通知,及课程背景介绍。部分读者希望进一步了解课程细节,本篇资讯应此而生。
专题课将从商务、法律、公众和政...
|

|
FDA 官员总结 2018 年警告信趋势
2018.10.17
美国 FDA 药品审评与研究中心(CDER)生产质量办公室代理主任 Francis Godwin 在 9 月 25 日举行的 PDA/FDA 联合会议上讨论了一些推动警告信发布的最新趋势,并分享了最近警告信中的例子来说明检查员发现的一些缺陷。
Godwin 表示从今年 1 月到 8 月 31 日,FDA 生产...
|

|
FDA 2018 财年仿制药批准再创纪录
2018.10.16
美国 FDA 仿制药办公室(OGD)2018 财年批准了 781 件 ANDA,打破了 2017 财年 763 件批准的历史记录,同时还有 190 件暂时批准,共 971 件批准,也创下了新的批准记录。这是一个好迹象,表明随着 GDUFA II 期第一个财年的结束,仿制药批准工作正在朝着积极的方向发展。
FD...
|

|
FDA-DIA 复杂药械组合产品研讨会简报
2018.10.15
https//www.fda.gov/Drugs/NewsEvents/ucm617128.htm FDA/DIA 复杂药械组合产品研讨会于 10 月 9 -10 日在美国 Silver Spring 召开。会议第一天涉及这类产品仿制药提交的监管内容,并讨论了与复杂仿制药相关的临床内容,重点是吸入产品。
FDA 演讲者重点关注的话...
|

|
【更新提示】识林一周回顾(20181007-1013)
2018.10.14
【国务院】关于在全国推开“证照分离”改革的通知(10.11)
从2018年11月10日起,在全国范围内对第一批106项涉企行政审批事项,分别按照直接取消审批、审批改为备案、实行告知承诺、优化准入服务等四种方式,实施“证照分离”改革。
《通知》明确了改革的重点内容。一是明确改革...
|
|
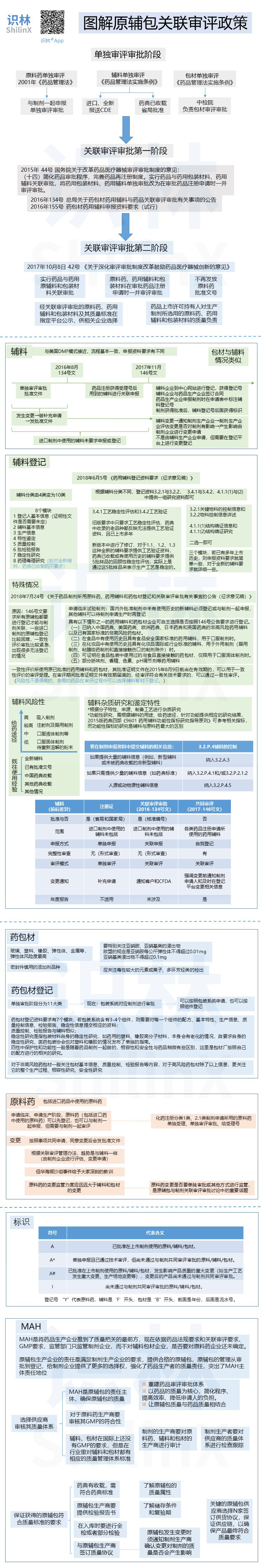
图解原辅包关联审评政策
2018.10.13
作者:识林-樟
识林®版权所有,未经许可不得转载。如需使用请联系 admin@shilinx.com 。
...
|

|
FDA 针对透皮仿制药发布系列指南
2018.10.12
美国 FDA 于 10 月 9 日发布了两篇有关透皮和外用递药系统(TDS)仿制药的指南,同时还发布了 25 篇针对外用和透皮产品的具体产品生物等效性(BE)指南,其中 2 篇新指南,23 篇修订指南。这些 BE 指南涉及具体产品所需的 BE 研究以及支持 BE 所必需的黏附性以及刺激性和致敏...
|

|
美国白宫发布“先进制造业美国领导力战略”报告
2018.10.11
美国白宫于 10 月 5 日发布了一份长达 40 页的《先进制造业美国领导力战略》报告1,继续其复兴美国制造业的努力。该报告由美国国家科学技术委员会先进制造业小组委员会编写。
该报告详细介绍了制造业中的各个方面,并概述了美国如何发挥领导作用。该战略基于三个具体目标:新制造...
|

|
FDA 受控函提交更方便,但能否真正解决问题?
2018.10.10
2018 年 10 月 1 日,美国 FDA 允许企业通过门户网站(CDER Direct NextGen Collaboration Portal)直接向 FDA 电子化提交受控函(CC,Controlled Correspondence ),并发布了包括如何注册使用门户网站的指导。这可能有助于加快向 FDA 提交受控函的速度,但是提交到 FD...
|

|
无进展生存期能否反映患者生存质量?
2018.10.09
尽管无进展生存期越来越多地用于癌症药品的临床试验,但一项新研究表明,这种方法并不一定能反映患者生存质量的改善。
一项研究1分析了 2000 年到 2016 年间涉及近 14000 名(患有 12 种不同形式癌症)患者 38 个随机临床试验的 52 篇文章,发现当疾病没有恶化时,健康相关...
|

|
国际药用气雾剂联盟点评 FDA 最新指南
2018.10.08
2018年9月13日-14日,由美国药学科学家协会中国讨论组(America Associate of Pharmaceutical Scientists China Discussion Group,AAPS CDG)和国际药用气雾剂联盟(International Pharmaceutical Aerosol Consortium on Regulation & Science, IPAC-RS)主办的“AAPS CD...
|

|
【更新提示】识林一周回顾(20180930-1006)
2018.10.07
【EMA】上市许可前指南更新(10.03)
新增问答5.1.13,对“如何更改正在进行中的上市许可申请?”作出了回答。
【中译】FDA定稿指南 ANDA递交-内容和格式(10.03)原文 花脸稿
该指南旨在帮助申请人根据“联邦食品、药品和化妆品法案”(FD&C法案)第505(j)条(21 U.S.C...
|

|
全球最权威医学杂志思考何去何从
2018.10.06
《新英格兰医学杂志》(NEJM)集团于上周四宣布,NEJM 总编 Jeffrey M. Drazen 博士将在明年退休。为了确保顺利过渡,Drazen 博士将继续领导期刊和 NEJM 集团,直到任命继任者为止。这一宣布,为世界上最负盛名的医学期刊带来新视角,创造了机会。
Drazen博士于 2000 年出任 N...
|

|
关键性临床试验成本可能并没有想象的那么高
2018.10.05
一项新研究表明,获得监管批准所需的关键性临床试验的中位数成本仅为 1900 万美元。换而言之,用于说服 FDA 批准新药的关键科学证据只占整体研发成本的一小部分,
根据发表在 JAMA Internal Medicine 上的研究1 显示,此类试验的最低成本从用于罕见代谢紊乱药物的四名患者试验的...
|

|
美墨加贸易协定为生物制品设定十年专营权
2018.10.04
新的美国-墨西哥-加拿大贸易协定规定,生物制品在产品“首次上市批准之日起至少 10 年内”拥有市场保护。
《美国生物制品价格竞争和创新法案》(BPCIA)规定,生物类似药申请必须在参照产品首次获得许可之日起 12 年之后才能获得批准。贸易协定不会改变这一规定,但会让将保护期缩...
|

|
FDA 发布公民请愿指南阻止品牌药商故意拖延仿制药批...
2018.10.03
美国 FDA 于 10 月 2 日发布《根据联邦食品、药品和化妆品法案第 505(q)节规定的公民请愿和停止诉讼请愿》修订指南草案,旨在为 505(q) 请愿提供更高效的路径,并使 FDA 能够将更多审评员资源集中在科学审评上。
这是 FDA 药品竞争行动计划(DCAP)增加处方药市场竞争...
|

|
复杂仿制药历史是由参与者书就的
2018.10.02
9 月 5 至 7 日,GRx+Biosims 会议在美国马里兰州巴尔的摩举行,会议的最后一天是 FDA 主持的关于复杂产品 GDUFA II 期 ANDA 前计划的内容。
仿制药办公室(OGD)研究与标准办公室监管事务副主任 Kris Andre 详细讨论了与复杂仿制药会议相关的组织工作和 FDA 的期望。...
|