
|
FDA 公告对一家药商伪造文件的惩处
2019.08.22
美国 FDA 于 8 月 20 日在其新闻公告中表示向一家中国非处方药(OTC)制药商发出了一封警告信,内容涉及包括数据可靠性在内的 CGMP 违规行为。这是 FDA 不太常见地通过新闻公告和邮件订阅的形式公布其向某家公司发出警告信,宣传力度之大或许与公司所生产的产品性质有关,FDA ...
|

|
FDA 标签或考虑通过 PKPD 建模分析增加剂量灵活性
2019.08.21
美国 FDA 药品审评与研究中心(CDER)临床科学中心副主任和新药办公室直属办公室高级顾问 Robert Temple 建议 FDA 考虑将药代动力学(PK)和药效学(PD)建模分析添加到药品标签中,以作为指导剂量个体化的一种方式。FDA一般不允许在药品标签中添加未经确证性研究的剂量,而通过 PK...
|

|
缬沙坦危机新进展:FDA 瞄准回收溶剂供应商
2019.08.20
美国 FDA 在沙坦类降压药含有潜在致癌物事件之后审查了几乎所有制药商,现在他们有了新目标。通过将目光瞄向溶剂回收商,FDA 表明了其打算将沙坦类产品致癌杂质的调查和药品 GMP 要求的执行范围扩展到所涉及的原料药和成品制剂之外的意图。
FDA 官员此前曾警告制药商不要使用重复...
|

|
FDA 仿制药批准再创纪录,但问题依旧
2019.08.19
美国 FDA 继续保持其仿制药批准大踏步前进,距财年结束还有两个月的时间,批准量已创历史新高。
FDA 在 7 月份公布了 61 件 ANDA 完全批准后,本财年前 10 个月的批准总数已达 814 件,首次突破 800 并打破了 2018 财年 781 件完全批准的记录。按照此速度,FDA 在本财年...
|

|
【更新提示】识林一周回顾(20190811-0817)
2019.08.18
【IPEM】9月份课程即将在北京开班(08.16)
IPEM 9月份IPEM课程即将在北京开班,课程安排如下:
9 月 5 - 6 日,陈建芳女士,课程:仿制药研发到申报前中后的项目管理 — 口服固体制剂大案例详解。针对美国申报的仿制药,将项目管理概述与案例研究相结合,旨在帮助学员了...
|

|
FDA 境外飞行检查摆上桌面,直指中国和印度
2019.08.17
美国参议院财政委员会主席共和党议员 Chuck Grassley 于 8 月 6 日在写给美国卫生部部长和 FDA 代理局长的一封信中表示,希望对于国外制药工厂,尤其是中国的工厂,FDA 不再提前通知检查安排而是开展不经提前通知的“飞行检查”。
Grassley 在信中写道,美国药品中使用的原料...
|

|
申报前会议可能给 EMA 审批过程带来偏见?
2019.08.16
经过两年的调查,欧洲监察使建议欧洲药品管理局(EMA)采取几项措施,以确保与制药商就上市申请进行的申报前会谈不会影响审批决定。
欧洲监察使 Emily O'Reilly 对于企业与监管机构之间申报前的会谈表示担忧并展开调查,她指出,这些会谈可能会产生偏见,或者企业可能会以某种方式...
|

|
FDA 最后通牒:企业需在一个月内更新药品登记信息
2019.08.15
有药品在美国 FDA 注册的企业请注意,请立即采取行动,确保场地信息、药品登记信息和生产场所正确无误,否则药品可能被禁止在美国销售。
FDA 于 8 月 13 日宣布将于一个月之后(9 月 12 日)清理其数据库,撤销那些没有按法规要求更新或认证的药品上市登记(drug listing)...
|

|
FDA生似药比对分析评价指南行业反馈摘选
2019.08.14
生物类似药申办人对于美国 FDA 放弃对一些比对分析评价要求统计等效性检验要求的决定普遍表示支持,但对于定量数据分析、参照标准品确认和国外参比品的使用持怀疑态度。
FDA 于今年五月份发布《治疗性蛋白质生物类似药的开发:比对分析评价和其它质量考量》指南草案(中文翻译),修...
|
|
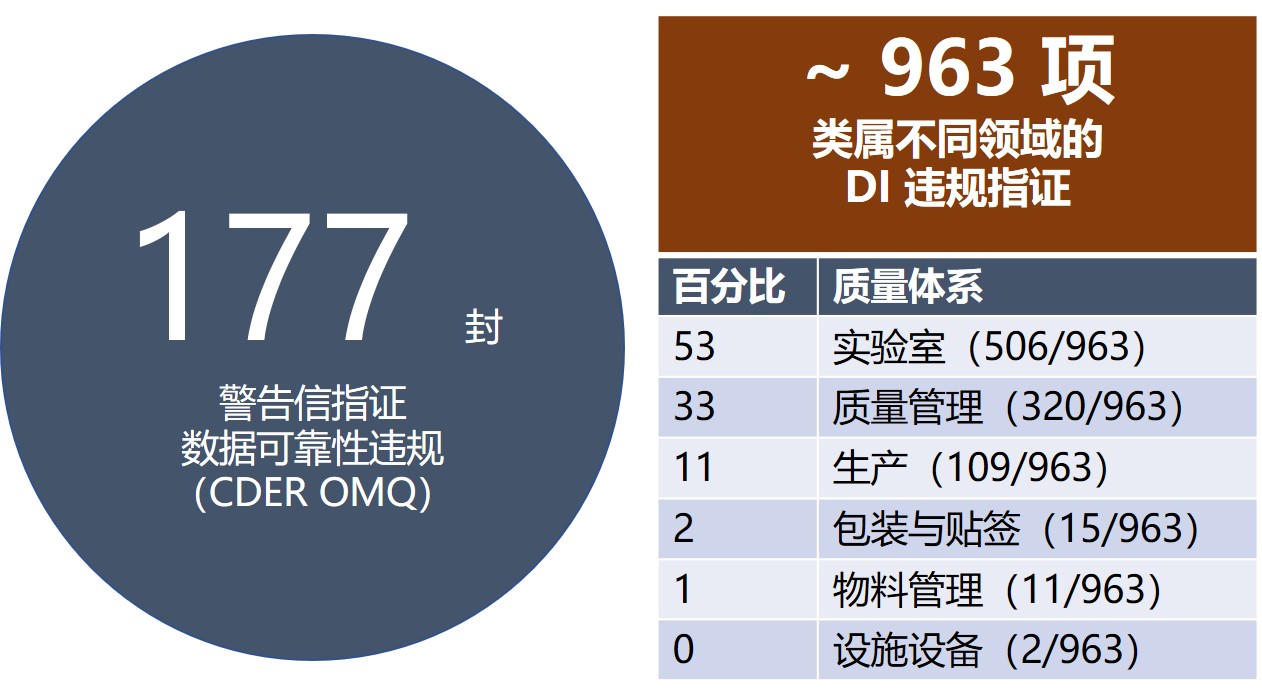
FDA 向国外发出的警告信四分之三涉数据可靠性
2019.08.13
昨天的资讯介绍了企业如何换个角度从监管视角审查自身问题,在监管检查之前发现隐藏的数据可靠性缺陷。今天我们从一些警告信观察项数据以及资深专业人士的建议来继续看看如何及早、高效的发现数据可靠性问题。
前 FDA 检查员、Parexel 咨询公司副总裁 Ron Tetzlaff 于 2019 年...
|

|
企业应从监管视角审查自身数据可靠性
2019.08.12
数据可靠性(data integrity, DI)监管合规专家观察到,行业内部和第三方审计人员通常不会发现数据可靠性失败,因为他们没有像 FDA 检查员那样查看系统和流程。即使在公司已经针对即将到来的检查执行了多次审计的情况下,监管机构也能识别出公司尚未发现或者尚未进行风险评估的 DI ...
|

|
【更新提示】识林一周回顾(20190804-0810)
2019.08.11
【IPEM】2019年IPEM课程教育8月份课程即将在北京开班(08.07)
【IPEM】注射剂的处方设计、工艺开发与生产管理;注射剂的一致性评价与参比制剂的选择;欧盟和WHO无菌指南、常见GMP缺陷分析、数据可靠性;欧美现场检查、交流沟通方式方法、483 和警告信处理(08.05)
IPEM 8月份...
|

|
请小公司代报新药避缴 PDUFA 费,机关算尽反误卿
2019.08.10
一药企因付费请两家小公司分别向美国 FDA 提交两个氯化钾口服溶液的新药上市申请(NDA)被罚款 400 万美元。而这家药企这样做的目的原本是为了节省 220 万美元的处方药使用者付费法案(PDUFA)下的申请费。
Lehigh Valley 技术公司,现称为 Genus 生命科学公司,被指控向两...
|

|
识林“会议日历”上线了
2019.08.09
找专家解决技术难题,如何找到合适的专家,怎么判断专家的水平?
部门要做培训计划,有哪些行业会议应该去,值得去?
总是错过有价值的研讨会,工作繁忙之中,如何安排学习日程?
国外好会路途遥远,语言不通,如何足不出户,双语学习?
识林“会议日历”是整合识林资料和万名用户分...
|

|
透彻理解,有效控制 — 记口服固体缓控释制剂青岛专...
2019.08.08
2019年8月3-4日,由北京大学药物信息与工程研究中心主办、青岛百洋制药有限公司承办的“口服固体缓控释制剂专题会”在美丽的海滨城市青岛成功举办,近200名来自中美药品监管机构、药品研发机构、制药企业、医疗机构和大学院校等单位的专家和业内人士参会,参会者中还有十多名IPEM的学员...
|

|
诺华基因治疗药陷数据可靠性泥淖,知情迟报或加重问题...
2019.08.08
美国 FDA 严肃声明,诺华及其子公司 AveXis 公司可能会面临民事或刑事诉讼,不仅是因为操纵用于 Zolgensma 基因治疗药物批准的数据,更是因为公司在产品批准前就知道了这个问题但并没有向 FDA 披露。
FDA 生物制品审评与研究(CBER)主任 Peter Marks 在 8 月 6日的一份声...
|

|
MHRA 对临床试验电子健康记录问题的GCP缺陷示例和建...
2019.08.07
本文是英国 MHRA 资深 GCP 检查员撰写的一篇有关用于临床试验目的的电子健康记录(EHR)的问题和建议,文中详细列举了在检查中发现的各类问题,并给出了一些改进原则和注意事项。无论对于临床机构还是申办人,都非常有帮助。
英国有一项国家医疗服务(NHS)计划,用电子健康记录(E...
|

|
从教训开始学习 – 看看回复483有哪些常犯的错
2019.08.06
是不是检查结果不好就会收到警告信呢?根据识林483数据库(即将上线,数据库收录了美国FDA 过去十年近50000条检查信息和6000多封483报告原文,还可提供检查员信息等迎检定制服务),官方行动指示(OAI)最终转化为警告信的比例近似为20%(考虑到检查结果的升级和降级,这个比例是假设FDA...
|
|
患者收到的一封药品召回信
2019.08.05
这是我在美国首次收到一封来自经销商(不是生产商)的药品召回电子信,其中明确说明了召回原因,召回药品对患者的安全影响,给患者的补救方式,以及具体的召回批次等。邮件为患者着想,简明扼要。特与大家分享。
Dear Patients,
亲爱的患者:
Natural Ophthalmics Eye Drops ha...
|

|
ICH Q12 在日本和加拿大的进展情况一瞥
2019.08.05
加州分离科学学会(CaSSS)每年夏天都会在美国华盛顿特区举行一个为期两天的互动论坛,即 CMC 战略论坛。今年论坛的题目是“批准后变更的未来即将来临 — 你准备好迎接 ICH Q12 了吗?”这是一次非常及时的会议,因为预计 Q12 指南将于今年 11 月份在下一次 ICH 大会上进展到第...
|