
|
欧盟更新 MAH 和 GMP 法规体系思考性文件
2021.07.31
欧洲药品管理局(EMA)于 7 月 27 日发布了 GMP 和 MAH 思考性文件“Reflection paper on Good Manufacturing Practice and Marketing Authorisation Holders”,规定了根据欧盟委员会(EC)GMP 指南和其它欧盟立法,上市许可持有人(MAH)负有的 GMP 责任,系统梳理了欧...
|

|
PICS 将纳入欧盟 GMP 附录 16 质量受权人认证和...
2021.06.22
6 月 15 日,国际药品认证合作组织(PIC/S)宣布了其将欧盟 GMP 附录16 关于药品质量受权人(QP)认证和批次放行的内容纳入 PIC/S 指南的计划。目的是让非欧盟/欧洲经济区(EEA)成员将附录 16 纳入其监管体系。
欧盟附录 16 涵盖了 QP 的认证,QP 可以为在欧盟的上...
|

|
礼来内部调查报告称没有向 FDA 做出虚假陈述
2021.06.15
据路透社上周报道,根据 5 月 20 日礼来公司 Branchburg 工厂负责人发给员工的一份内部备忘录称,礼来的独立外部法律顾问调查得出结论,“礼来向 FDA 做出虚假陈述的指控没有得到证实。”
备忘录的结论与礼来 Branchburg 工厂工人最初提出的指控不同。根据此前爆出的一份内部...
|

|
CMO混淆污染致千万剂疫苗报废:FDA 要求报废 6000 ...
2021.06.14
美国 Emergent Biosolutions 巴尔的摩工厂的制造问题持续升级。
根据《纽约时报》于 6 月 11 日的报道,援引知情人士消息,FDA 在花费数周时间对工厂进行检查后,已要求新冠疫苗制造商强生公司及其生产合作伙伴 Emergent 报废 6000 万剂疫苗。另外,FDA 允许大约 1000 ...
|

|
美国司法部介入调查礼来新冠抗体工厂质量控制和文件造...
2021.05.28
礼来公司位于新泽西州 Branchburg 生产新冠治疗性抗体的工厂因质量控制问题和涉嫌篡改文件而备受关注。现在美国司法部(DOJ)已介入调查。
礼来于 5 月 27 日公布提交给美国证券交易委员会的 8-K 披露表显示,美国司法部已向礼来发出传票,要求提供与 Branchburg 工厂有关的...
|

|
礼来爆出内部员工投诉高管造假、FDA 最新检查缺陷等...
2021.05.11
根据路透社 5 月 5 日报道,礼来公司内部的一份投诉显示,其员工控告新泽西州 Branchburg 礼来工厂(该厂主要生产新冠治疗性抗体)的一名高管修改 FDA 要求的文件以试图淡化严重的质量控制问题。
这份未签字的投诉报告于 4 月 8 日在礼来保密的员工投诉系统中提交。投诉称,该高...
|
|
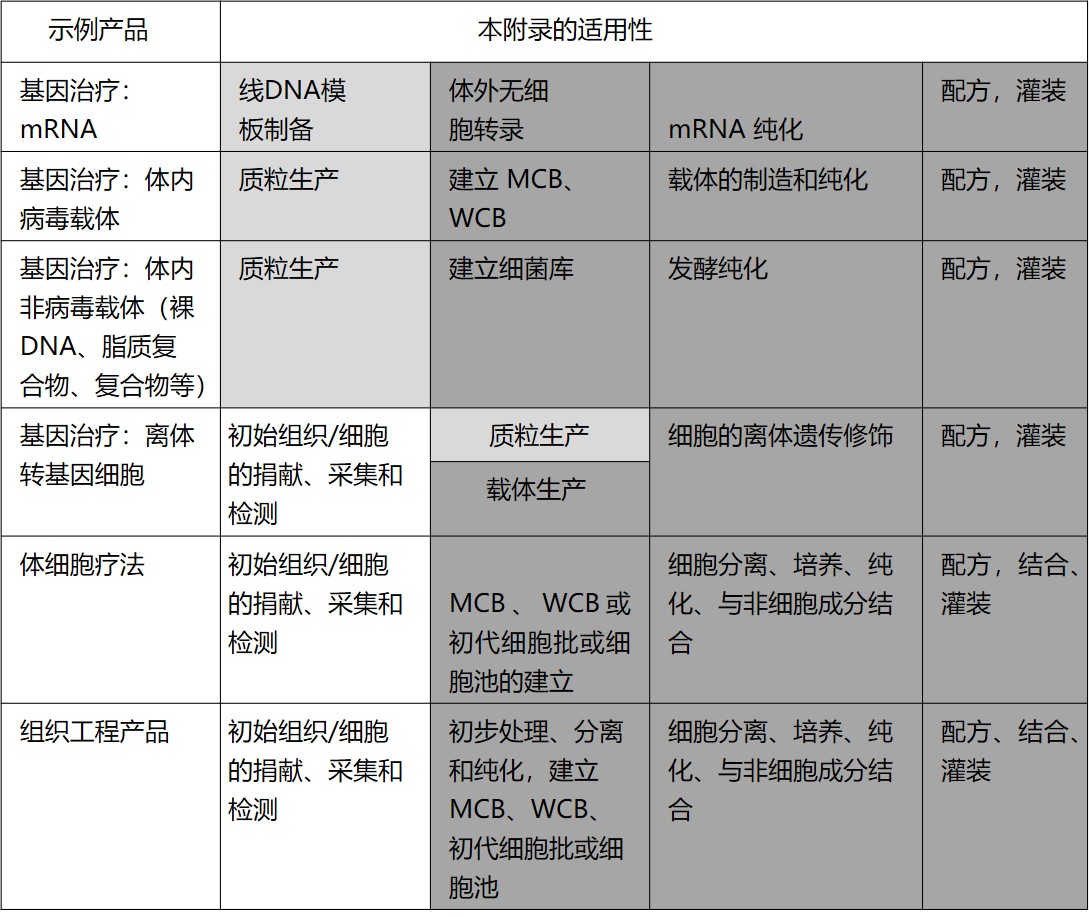
PICS 最新 GMP 指南增加附录 2A 先进治疗药品的...
2021.04.28
国际药品认证合作组织(PIC/S)于 4 月 26 日重新发布了其 GMP 指南,主要修订为将原 GMP 指南的附录 2 《人用生物原料药与药品的生产》稍作修订变为附录 2B,新增附录 2A《人用先进治疗医药产品的生产》。此次修订版本将于 2021 年 5 月 1 日生效。
在生产先进治疗医药产品(Adva...
|

|
FDA飞速检查新冠疫苗CMO并发布长达12页的483
2021.04.22
美国 FDA 于 4 月 21 日(周三)公布了其对 Emergent Bio Solution 巴尔的摩工厂的检查 483,总共 12 页,9 大观察项。
此次 FDA 行动速度之迅速,自上个月底 Emergent 被曝出在生产强生和阿斯利康的新冠疫苗可能存在交叉污染问题,强生将此情况报告给了 FDA。【CMO混淆...
|

|
CMO混淆污染致1500万剂新冠疫苗报废:FDA 关停工厂,...
2021.04.21
美国 FDA 要求 Emergent BioSolution 的巴尔的摩工厂停止生产新冠疫苗原液,并隔离所有剩余产品。
之前,该工厂由于同时生产强生和阿斯利康的新冠疫苗可能存在交叉污染而不得不废弃 1500 万剂强生疫苗原液。之后强生公司将事故报告给 FDA,FDA 对工厂生产线展开调查,同时强生...
|
|
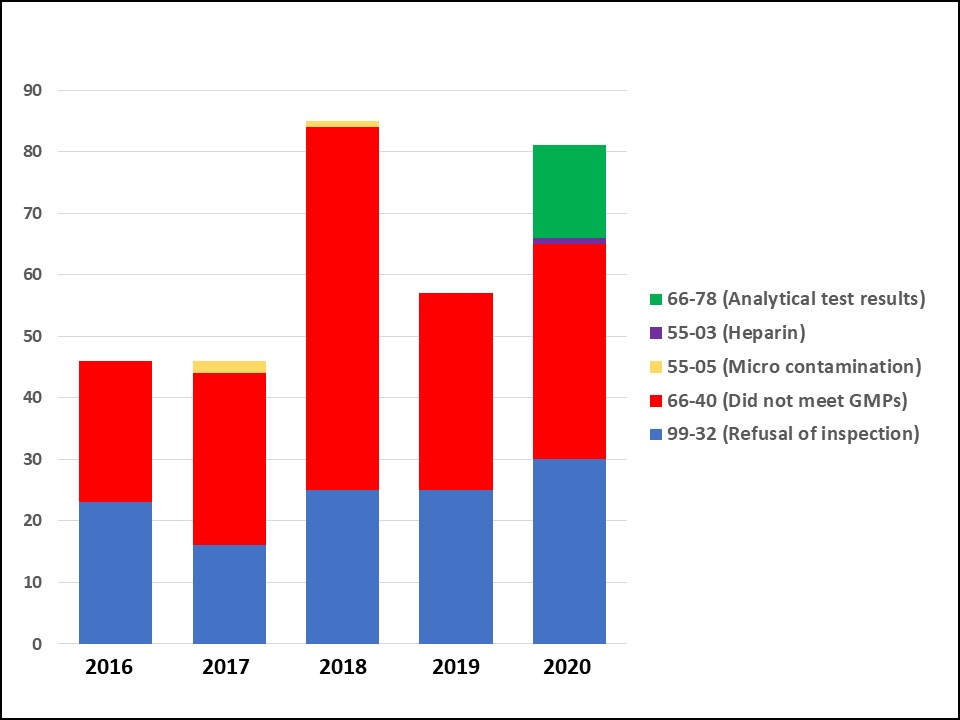
FDA 合规办公室 2020 年报:检查减少,警告信增多
2021.04.05
根据美国 FDA 近期发布的《2020 年合规办公室年度报告》,FDA 药品审评与研究中心(CDER)合规办公室(OC)在 2020 年,由于新冠疫情,检查工作减少,但警告信却有所增多,进口禁令数量也有所增加。
报告还重点介绍了 2020 下半年在办公室活动中占主导地位的新冠应对,包括:保...
|
|
欧盟无菌 GMP 附录修订进展与业界疑虑
2021.03.24
制药行业目前仍对欧盟委员会关于无菌 GMP 附录(Annex 1)的修订有所担忧。行业和监管人员在 3 月 16 日召开的 ISPE 年度无菌会议上介绍了欧盟无菌附录的最新进展,谈到了仍然产生混乱的一些方面并讨论了将受到无菌附录影响的一些领域。
目前讨论的附录修订版于 2020 年 2 月...
|

|
WHO 和国际原子能机构联合发布研究用放射性药品 GMP...
2021.03.10
世界卫生组织(WHO)和国际原子能机构(IAEA)于 3 月 3 日发布了关于研究用放射性药品的 GMP 指南。该指南是对现行研究用产品的 GMP 指南进行修订的首个工作草案,征求意见截止日期为 4 月 30 日,预计将在 2021 年 7 月之前完成修订后的文件并再次公开咨询意见。
指...
|
|
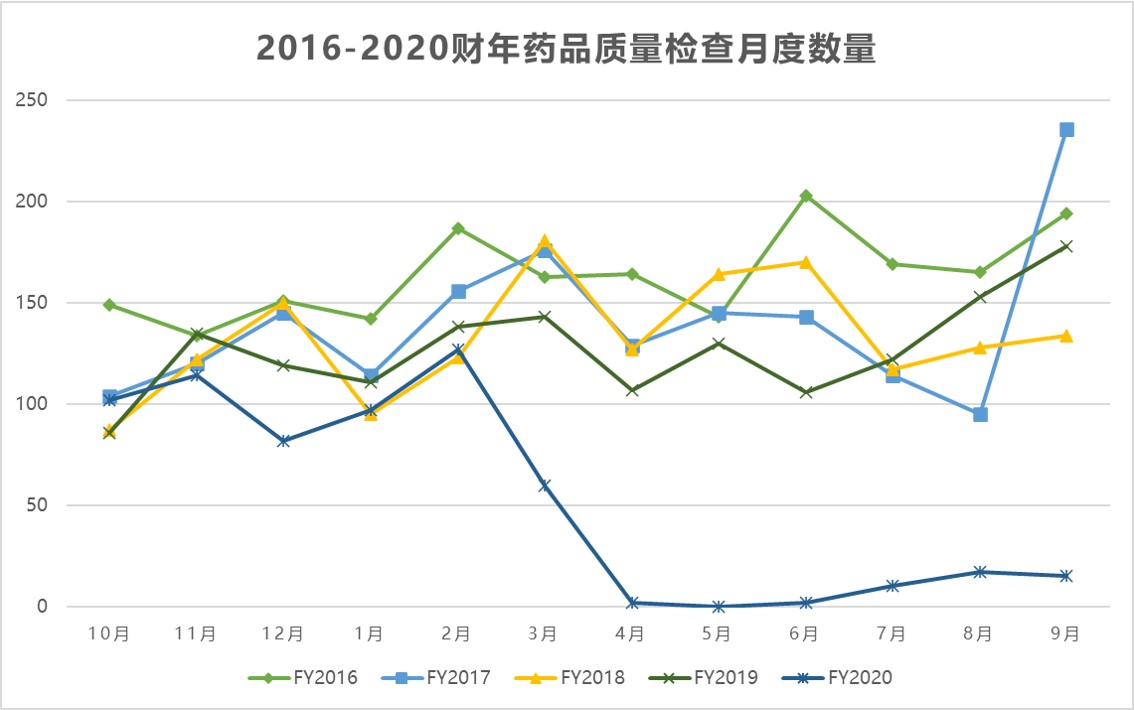
美国 FDA 检查分类情况回顾,做好准备迎接未来的检...
2021.02.12
识林祝大家过年好!牛年第一天我们来回顾一下 FDA 2020 财年的检查分类情况,以及通过这些数据,企业可以提前为未来的检查做哪些准备。
去年,疫情严重影响了美国 FDA 的执法计划,这一影响将在今年持续,并可能波及未来几年。上周识林集中报道了有关 FDA 首封基于远程记录审查的警...
|

|
欧盟检查员分享远程 GMP 检查经验,或将成永久性措...
2021.02.03
在正在进行的试点取得早期积极成果之后,欧洲药品质量管理局(EDQM)计划将“实时远程检查”作为其 GMP 检查计划的一项永久性措施。
这项试点是由于与 COVID-19 相关的旅行限制导致的现场检查的推迟而启动的。到目前为止,EDQM 的检查员已经从他们在欧洲的办公桌旁对印度两家制药...
|

|
FDA 2020 财年药品检查观察项和趋势
2020.11.28
美国 FDA 于 11 月 24 日最新发布了 2020 财年检查观察项汇总数据,本文重点查看药品制剂方面的 483 相关缺陷数据。
今年由于新冠(COVID-19)大流行的影响,FDA 自 3 月份宣布推迟所有境内和境外场地的常规监督检查,并在可能的情况下采用其它工具和方法进行批准前检查。【...
|

|
WHO 发布药品研发期间的 GMP 指南草案
2020.11.16
世界卫生组织(WHO)于 11 月 11 日发布《研究和开发设施的良好实践》指南草案,为在研究和开发设施中进行的开发批、中试批和稳定性批次的生产提供 GMP 方面的建议,并指出,GMP 严格性随着开发过程的不断进展而不断增加。
鉴于最近对于治疗新冠治疗药快速开发的迫切需求,WHO ...
|

|
礼来新冠治疗性抗体获紧急授权,GMP 合规要求为授权...
2020.11.12
美国 FDA 于 11 月 9 日发布了针对礼来 COVID-19 治疗性单克隆抗体 bamlanivimab 的紧急使用授权(EUA)。该 EUA 独特之处是将 GMP 合规要求列为授权条件之一。授权书解答了 FDA 是如何解决对礼来新冠治疗性抗体的迫切需要与在生产设施检查中发现严重 GMP 问题之间的冲突。
Ba...
|

|
欧洲众协会对欧盟无菌 GMP 附录修订提出更多改进
2020.11.12
欧洲 12 个行业协会组织代表联合致信欧盟委员会,要求对欧盟无菌 GMP 附录进行改进,制定一套统一的“高级别”建议。信中还建议取消示例,并更好地区分无菌药物生产中的某些技术类型。关于取消示例的原因,主要是无菌 GMP 附录不仅会在欧盟使用,还会在全球范围内使用,这些例子可能...
|

|
WHO 发布试验用药品 GMP 指南修订草案
2020.11.10
世界卫生组织(WHO)于 11 月 5 日发布了《试验用药品的 GMP》指南草案征求意见稿。
该指南是对 1996 年相同主题 GMP 附录7 的修订,几乎相当于重写。由于原先的指南发布日期较旧且最近对 COVID-19 药物进行检查产生的新的指导原则,WHO 第55次药物制剂专家委员会(ECSPP...
|

|
美国、英国和俄罗斯前十大检查观察项对比
2020.10.22
前日我们分析了英国药品与医疗保健产品监管机构(MHRA) 2019 年的 GMP 检查缺陷趋势【英国 MHRA 2019 年 GMP 检查缺陷趋势分析 2020/10/20】,本文我们来看看美国 FDA、俄罗斯卫生部、英国 MHRA 三国在 2019 财年前十大制药企业检查观察项,有哪些相似和差异之处。
今年三月份的 ...
|