
|
对于细胞和基因治疗产品,与临床研究阶段相适应的GMP...
2022.07.01
细胞和基因治疗产品产业持续发展,从发现研究阶段逐步进入临床开发并过渡到中后期和及商业化生产阶段,产品的质量、合规以及适当的标准成为需要考虑的必要要素,到了是否准备好开始GMP生产的决策点。
在着手考虑这些要素的组织或机构,包括成熟的大/中型生物药企业、初创公司、以及学...
|

|
【线上讲座问答集锦】GMP附录-临床试验用药品实施策...
2022.06.30
5月27日国家局发布药品GMP附录-《临床试验用药品(试行)》(以下简称:本附录),并确定自2022年7月1日起施行。为帮助大家更好的理解并执行本附录,6月18日识林特邀请本附录起草参与者之一的夏禄华老师,就本附录起草过程中的相关讨论及落地实施策略进行了分享。
现将交流过程的精彩...
|

|
线上讲座:GMP附录-《临床试验用药品(试行)》实施...
2022.06.13
5月27日国家局发布《临床试验用药品(试行)》附录,作为《药品生产质量管理规范(2010年修订)》配套文件,自2022年7月1日起施行。同时发布的还有核查中心编写的《药品生产质量管理规范》临床试验用药品附录相关问答。更好的为临床试验用药品的生产、质量管理提供合规依据。(参见识...
|

|
【线上讲座问答集锦】《药品共线生产质量管理指南(征...
2022.06.08
5月25日,识林特邀《药品共线生产质量管理指南》起草参与者之一的夏禄华老师,联合行业专家:付秋雁老师、何林旺老师、季铁军老师、赵振坤老师、刘倩老师、赵成刚老师,就《指南(征求意见稿)》进行在线讨论,分享指南的起草背景、愿景,分析行业中存在的问题、解决的思路,为企业在实践...
|

|
临床试验用药品 GMP 附录,识林向导这么读
2022.05.30
临床试验用药品的管理,对于药企,无论从哪个角度,都颇为棘手:
从药品质量出发,回顾2010 GMP 的总原则“企业应当建立符合药品质量管理要求的质量目标,将药品注册的有关安全、有效和质量可控的所有要求,系统地贯彻到药品生产、控制及产品放行、贮存、发运的全过程中,确保所...
|

|
【周末杂谈】雅培总裁的道歉信
2022.05.29
看全球著名企业,在遭遇重大公众危机事件时的公关
美国雅培公司总裁一周前在华盛顿邮报上,就其婴儿配方奶粉停产而引起的大范围婴儿配方奶粉短缺(详见识林资讯【周末杂谈:FDA饱受诟病的又一周】)发表的道歉信,为我们了解大企业如何应对重大公众危机,为我国企业进军欧美市场未...
|

|
【识林社区】优质问答集锦4
2022.05.28
以下是识林社区中的部分优质问答:
1. 与注册现场核查合并检查时,有什么注意事项?
社区用户@bvyc:
来自实操:
1、由于GMP符合性检查归属于省局负责,故与省局负责核查的检查中心对接、沟通尤为重要,收到核查通知后,第一时间沟通,包括核查时间,成员,查看工序(对api...
|

|
【问答回顾】疫苗CMC和GMP专题课精彩问答摘录
2022.05.26
5月21-22日,IPEM 邀请WHO的Ian Thrussell 先生和 Wacharotayankun 博士远程讲授疫苗专题的系列课程,并和来自PATH的高光博士一起在线答疑。
Wacharotayankun博士是疫苗CMC审评专家,参与了多项国外和国内疫苗产品的CMC审评,Ian Thrussell和高光博士最近两年在多家中国疫苗...
|

|
线上交流会:《药品共线生产质量管理指南(征求意见稿...
2022.05.19
2021年11月12日,为指导和规范药品共线生产,NMPA 核查中心组织研究起草并发布了《药品共线生产质量管理指南(征求意见稿)》。旨在为药品全生命周期内共线生产策略的设计、实施及改进提供分析和指导,重点介绍了药品研发阶段、技术转移阶段以及药品生产阶段对共线生产策略的考量,帮助相...
|

|
IPEM 课程 疫苗CMC和GMP:WHO专家讲解及在中国企业...
2022.05.16
以下文章来源于IPEM ,作者IPEM
新冠大流行带来了疫苗产业的热潮。4月初,WHO因GMP检查中发现缺陷,暂停采购印度Bharat Biotech生产的新冠疫苗Covaxin。Bharat Biotech也主动提出,因预期疫苗的需求减少,将减少Covaxin的生产。现在WHO已授权了超过10种新冠疫苗的紧急使用,接种率在...
|

|
【周末杂谈】国会对疫苗合同生产商 GMP 违规的调查...
2022.05.15
企业内部、及与合作方和咨询师的往来邮件和文件,都可被传证并公开
这周二,美国国会公布了对位于美国马里兰州巴尔的摩市的新冠疫苗委托生产商 Emergent BioSolutions GMP 违规的《调查报告》。虽然报告本身不乏美国国内党派争斗的色彩,但有一些值得我国企业注意的地方。有关 Emergen...
|

|
【公开课回顾】GMP迎检工作分析及注意事项
2022.05.05
4月28日识林邀请深资行业专家张新老师就“GMP 迎检工作分析及注意事项”进行在线公开课讲座【详见相关资讯】。讲座内容包括:中国/美国/欧盟的 GMP 检查概述、GMP 现场检查的常规过程、实施远程 GMP 检查及其准备工作、检查结论/检查缺陷及缺陷回复等内容,本次讲座内容详实,脉...
|

|
检查、指南、互认,EMA发布GMP 和 GDP 检查工作组20...
2022.04.27
4月20日,欧盟EMA发布 GMP/GDP 检查员工作组 (GMP/GDP IWG) 2021年度报告。
该检查工作组于 1996 年成立,由于英国退出欧盟的影响,EMA 业务连续性计划 (BCP) 中断,导致没有 2018 年至 2020 年的年度报告。GMDP IWG 目前通过远程会议平台进行会议。
GMP/GDP ...
|

|
【公开课回顾】中药质量问题解析与药品安全风险防控
2022.04.22
3月23日识林邀请原国家药监局药品GMP/中药GAP组长级资深检查员操复川老师,就中药质量问题解析与药品安全风险防控,进行了在线公开课讲座。讲座从中药常见质量问题与监督检查要点、中药饮片生产关键环节控制要点、中药制剂生产关键环节控制要点、中药均一化规定要求与生产质量控制、数据...
|

|
识林公开课:GMP迎检工作分析及注意事项
2022.04.20
随着我国新《药品管理法》、《疫苗管理法》及配套法规颁布和实施及加入ICH、并申请加入PIC/s等国际组织,强化事前审批和事中事后监管的新模式的同时,着力推动监管法治化、制度化、智慧化、国际化。对上市许可持有人依法开展药品全生命周期的监管,夯实主体责任,确保药品安全。
同...
|

|
PICS 修订 GMP 指南反映新的欧盟临床试验法规
2022.02.04
国际药品认证合作组织(PIC/S)于 2022 年 2 月初修订了其 GMP 指南(PE 009-16),以反映新的欧盟临床试验法规(CTR),该法规经过多年延迟后于 2022 年 1 月 31 日生效。
具体来说,PIC/S GMP 指南的附录 13 与研究性医药产品的生产有关,被新的欧盟附录 13 所取代...
|
|
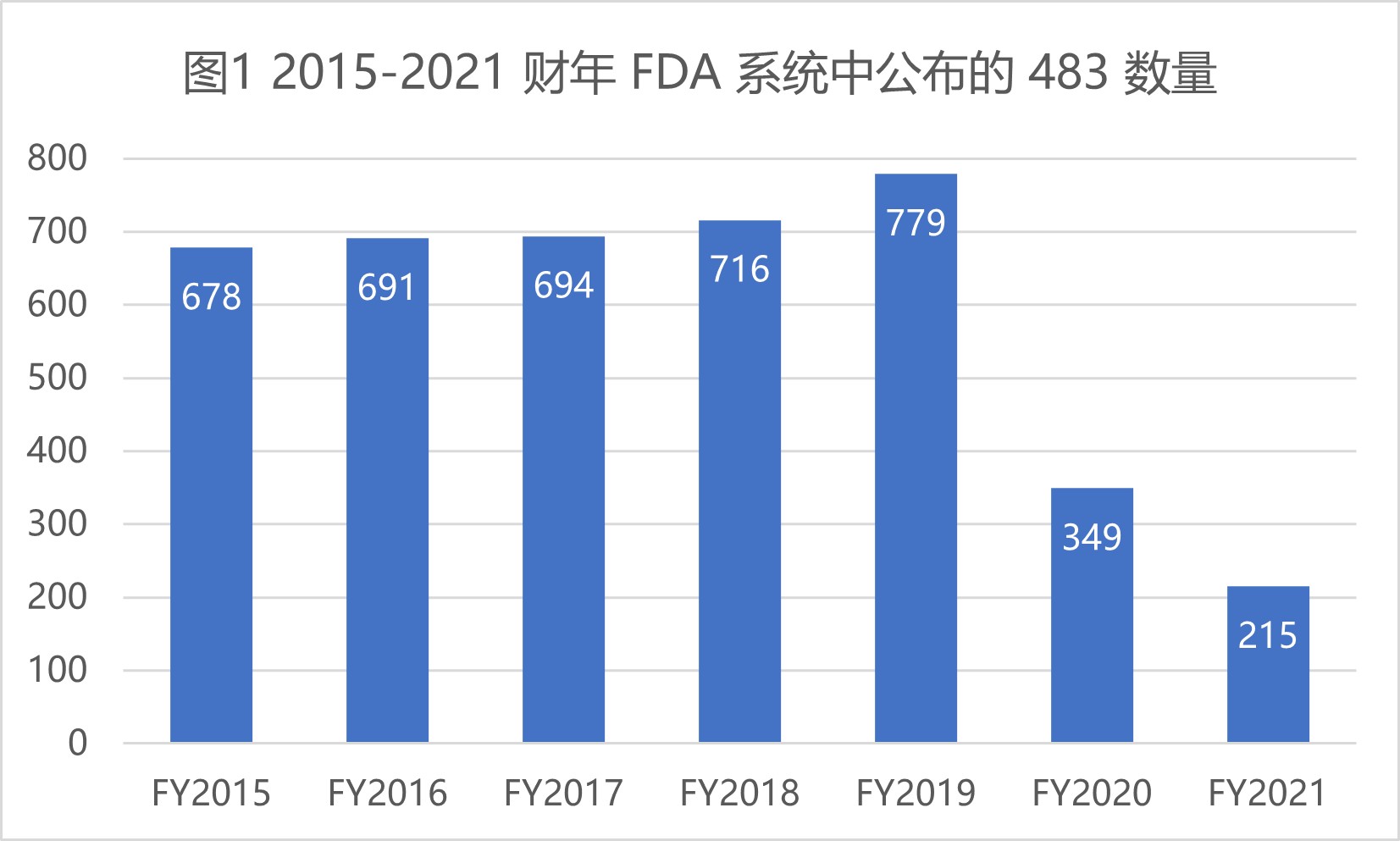
FDA 2021 财年药品检查观察项和趋势
2021.10.21
美国 FDA 于 2021 年 10 月 18 日最新发布了 2021 财年检查观察项汇总数据,本文重点查看药品制剂方面的 483 相关缺陷数据。
由于新冠疫情继续在世界绝大多数国家和地区肆虐,2021 财年 FDA 执行的检查数量仍然有限,而且执行的检查大多也是针对关键任务,涵盖面有限。所以...
|

|
欧盟因新冠疫情继续延长 GMP 和 GDP 证书有效期
2021.10.04
由于新冠疫情继续给 GMP 和 GDP 现场检查带来困难并且为了最大程度减少因新冠疫情对药品生产和供应造成的干扰,欧盟监管机构已将现有证书和限时许可的有效期延长至 2022 年底。这是欧盟自疫情以来第二次延长 GMP/GDP 证书有效期。【欧盟和英国在疫情期间放宽部分 GMP 要求 2020/04...
|
|
ISPE 会上关于数据可靠性、欧盟无菌附录以及常见 GM...
2021.09.29
国际制药工程协会(ISPE)9 月 24 日举办的生物技术会议和研讨会的一个小组讨论会上,澳大利亚监管机构检查负责人分享了有关数据可靠性、欧盟 GMP 附录 1,以及影响受监管制药行业的其它问题的看法。
数据可靠性问题
在小组讨论上,监管机构被要求评论虚拟审计如何影响他们在...
|

|
FDA 发布蛋白原液生产企业监督检查指南手册
2021.08.31
美国 FDA 于 8 月 27 日发布了新修订的合规项目指南手册《CPGM 7356.002M 蛋白原液生产企业监督检查》,该修订版 CPGM 将于 2021 年 10 月 1 日实施,届时将取代 2015 年相同编号的《许可生物治疗药品的检查》指南手册。
CPGM 是 FDA 指导检查员的工作手册,其中包...
|