
|
【识林解读与案例】细胞GMP,9-10月欧美批准,483综...
2022.12.03
在官方发布的法律法规、指导原则之外,识林原创、汇编、搜集了大量对比、解读、案例、解析等内容,作为识林用户学习法规指南的辅助,提供更多视角,且与岗位实务联系更为紧密。
这类资料,全部收录在刚刚开发的【对比解读案例解析】数据库内(点击查看使用介绍),通过“业务标签”和“...
|

|
IPEM 课程 工艺验证,变更管理,质量量化统计
2022.08.08
老师简介
李晓明博士,PQS+公司创始人,曾就职于美国默克制药、美国礼来制药和浙江海正药业。在近30年制药生涯中,创立了一套完整的固体口服制剂理论和制剂药物研发、生产、工艺优化的技术和方法,在领导力培养、质量组织框架搭建、质量管理体系高效率系统化设计、跨北美...
|

|
【周末杂谈】影响FDA监管权限的法院裁定
2022.07.03
未经法律的明确授权,监管当局不得制定具有广泛经济和政治影响的规章政策。
这周四,美国最高法院做出了一项限制美国环保局权限的裁定。表面上看,法院认定《环保法》未授权环保局(EPA)将各州的煤电厂作为整体来监管碳排放,尽管它授权EPA监管各家煤电厂的碳排放。深入地看,法院认...
|

|
【质量对话】质量量度与仿制药
2022.06.26
质量量度计划的主要对象,对FDA的做法提出了尖锐的意见
刺槐:6月7日截止的FDA征求行业对其质量量度报告计划的意见,共收到31份,其中两份值得特殊关注:一份来自辉瑞,一份来自普享药协会(曾用名是仿制药协会)。
编辑:一个是创新药企的领头,一个是仿制药业的代表,覆盖了药业的...
|

|
【质量对话】质量量度与供应保障
2022.06.19
为提高供应链稳健性,质量量度应关注但却未关注的一些因素
刺槐:今年3月9日,FDA在美国联邦公报上发表了修订的质量量度报告计划,并征求行业意见。到提交截至日期6月7日止,共收到31份意见(FDA网站上列出33份,但有重复计数)。
编辑:对此,识林资讯在3月9日和4月6日,报道过两次...
|

|
FDA质量管理成熟度线上研讨会内容梳理
2022.06.09
近日,FDA举办了为期两天的质量管理成熟度(QMM)线上研讨会。本次研讨会主要介绍了质量管理成熟度计划的基本概念、评估方法、实施现状、经验教训和业界反馈等,本文对研讨会的主要内容进行了归纳梳理。
一、质量管理成熟度的未来
定义和主要构成
FDA应领导开发一个框架,以衡量...
|

|
质量管理成熟度:迈向 21 世纪药品质量的必要步骤
2022.04.11
几天前,CDER 药品质量办公室(OPQ) 发布了一份关于质量管理成熟度 (QMM) 的白皮书 。
白皮书表示,CDER 朝着实现 21 世纪药品质量的愿景又迈出了一步:一个最大限度高效、敏捷、灵活的生产部门,在没有广泛监管监督的情况下可靠地生产高质量的药品。贸易协会、学者和监管机...
|

|
【质量对话】令人失望的 FDA 质量量度计划
2022.03.13
制药行业生产科学的状态需要改进,过度监管阻碍了创新
编辑:这周二,FDA公告了其在“质量量度计划”方面的最新思考并征求业界的意见。知道您一直关注质量量度,所以想听听您对此有何想法。
刺槐:FDA作为药品科学监管火车头,……
编辑:这话听上去怎么不对味呀,有话您就直说吧...
|

|
FDA 重提质量量度,就量度报告计划征求意见
2022.03.09
美国 FDA 于 2022 年 3 月 8 日发布了质量量度计划的最新更新,强调更多数据可以帮助 FDA和供应链,这些数据需要更好地理解哪些生产商超出了基线水平。FDA 表示,现行 GMP 合规“并不一定表明”制药商是否正在投资改进并努力对生产性能和质量进行一致的控制。
FDA 自 2013...
|

|
批次合格率和无效OOS率可能不是好指标,FDA 报告两质...
2021.03.25
美国 FDA 药品质量办公室质量监督办公室代理主任 Jennifer Maguire 表示,根据 FDA 两个质量量度项目参与企业的反馈,FDA 被敦促采用场地级别的报告而非产品级别的报告,不要使用批次合格率和无效 OOS(超标)率,可以使用其它指标,例如一次成功率、过程能力以及对前置时间(lead ...
|

|
FDA 全球质量基准研究初步分析结果
2020.12.01
一项由美国 FDA 资助的质量基准研究(Quality Benchmarking Study)计划从全球 52 个国家 2000 多家制药厂收集质量数据,帮助研究参与者基准化自己的质量绩效并学习如何改善。
该项目于今年 5 月启动,已从 1000 多家工厂收集到数据。研究由邓白氏公司(Dun & Bradstreet)和瑞...
|

|
FDA 宣布两项质量管理成熟度试点计划
2020.10.16
美国 FDA 药品审评与研究中心(CDER)今日宣布了两项新的试点计划,以从对制药商质量管理体系的第三方评价中获得洞察,从而为 FDA 表征质量管理成熟度(QMM)评级系统的未来发展提供参考。
成品制剂质量管理成熟度试点计划(QMM FDF 试点计划)适用于处方药和非处方药(OTC)药品...
|

|
FDA 质量基准研究向全球召集参与企业
2020.08.07
企业匿名参与,研究结束后可获得一份只有自己能够看到的定制报告
美国FDA一直都在寻找如何能继续推进和落实质量量度计划,而且试图从业界和学术界的试点和研究中获得更多知识,以期找到可行之路。
奖励质量(或者可以说“优质优价”),是 FDA 一直想做的事,2013 年FDA 就提出单靠...
|

|
FDA 药品质量评分系统久不落地,药房开发自己的优质...
2020.05.28
最近一篇论文中,一群学者和药剂师认为,基于监管行动和化学分析的评分系统可以刺激制药商生产更多优质药品并减少短缺,同时改善公共卫生。这篇发表在 medRxiv 的预印版论文1中表示,该想法“对于在美国药品供应链中增加急需的透明度,并使医疗系统购买方和药品支付方避免劣质药至关重要...
|

|
FDA 寻求制药商参与质量基准研究
2020.05.20
美国 FDA 一直以来都没有放弃探索如何评价和实施质量量度计划,而且试图从业界和学术界的试点和研究中获得更多知识,以期找到可行之路。今日,FDA 发布公告,就其资助的药品质量管理体系当前状态的研究,寻求制药商的参与。
FDA 表示,制药商可以通过标准化的质量基准研究(Quality B...
|

|
FDA 现场警示报告预测性分析试点,机器学习助力质量...
2020.04.15
美国 FDA 药品质量办公室(OPQ)下的质量监视办公室最近开展了一项预测性分析(Predictive Analytics)试点,使用现场警示报告(Field Alert Report, FAR)中的信息来衡量药品质量。给那些调查时间短并且能够发现不合格的根本原因的公司打高分,而给那些调查时间长并且无法找到不合...
|

|
医院和药房检测药品质量是可持续的方法吗?
2020.04.09
前段时间我们曾介绍过美国医疗机构对于公开质量评级持普遍支持态度,远比药业积极得多。但医院对于当前市场上药品的质量状态非常担心,虽然 FDA 一再保证仿制药的质量与品牌药一样。【公开质量评级,医院比药业更支持 2020/02/29】。医疗机构对处方的仿制药无效、仿制药被召回或售罄...
|

|
公开质量评级,医院比药业更支持
2020.02.29
美国 FDA 与医疗机构最近在华盛顿举行的杜克大学 Margolis 卫生政策中心研讨会上达成一致,认为公开药品质量评级将使患者和消费者受益,但 FDA 与医疗机构之间对于当前的质量状态有着巨大分歧。
FDA 集中精力于如何确保公众能够接受品牌药和仿制药的质量,而医疗机构则担心 FDA...
|

|
质量量度升级版呼之欲出?
2019.12.17
12月5日在FDA总部边上举办的ISPE全球制药监管峰会上,质量量度再次成为业界关注的议题。FDA向业界表示质量量度项目是FDA当前高优先级的项目,FDA正在着力推出整合了过去几年FDA、工业界和学术界研究和试点经验教训的改造版质量量度。
自FDA于2015年7月发布质量量度指南草案以来已经过去...
|
|
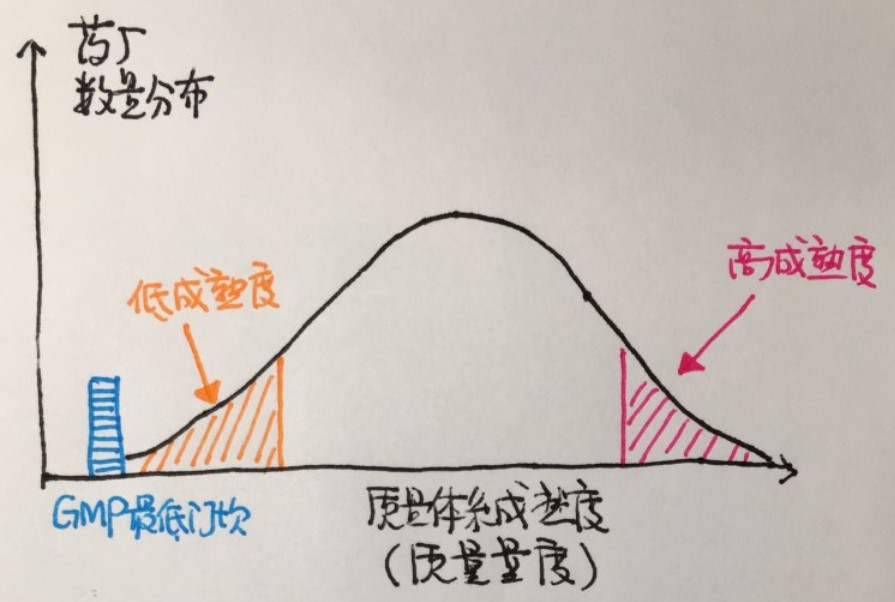
【周末杂谈】FDA再谈“优质优价”
2019.11.03
众所周知,FDA 的使命是保护和促进公众健康,方法是确保产品的安全、有效和质量可靠。但也许不那么众所周知的是,FDA 完成使命的手段是干预跨洲商贸,也就是说采用的是商业手段1,通过建立、维护并改善合理的市场秩序,来促使企业研制和生产有助于公众健康的产品。本文的讨论只限于仿...
|