
|
国内药政每周导读:2022.02.21-02.27
2022.02.28
【医疗器械】
2.18,NMPA发布《中国医疗器械标准管理年报(2021年度)》,随后中检院公开1851项《医疗器械标准目录汇编(2022版)》
【注册,审评,审批】
2.22,CDE公开征求《药审中心加快创新药上市申请审评工作程序(试行)》意见
【上市后监管】
2.25,NMPA修订质...
|

|
【周末杂谈】信达 PD1 审批与缺乏尊重和信任
2022.02.27
做强我国药监局,是促进我国药业创新、赢得国际尊重和信任的好办法?
锣鼓听声,说话听音。2月10日的“信达”PD1审批专家会上,也许最值得注意的是会议的调子和气氛,尤其是关键人物、FDA肿瘤中心主任Pazdur医师说的话,包括他会前发表在“柳叶刀”和“新英格兰杂志”文章中的话。翻译...
|

|
线上答疑:技术和合规专家联合解答 FDA 可见异物指...
2022.02.26
2022年1月27日,识林联合IPEM邀请盛德律所的合规和监管专家解读了FDA去年底发布的《注射剂产品中可见异物的检查》的行业指南(会议回放视频请登录识林查看),会上收到了近百个问题,因此识林联合盛德律所,邀请到IPEM项目的两位资深教师 — 尹放东博士和 Ian Thrussell 先生,在3月1日...
|

|
【纪要】美国律师谈 FDA 关于仅中国试验策略、数据...
2022.02.25
识林联合IPEM教育项目和美国盛德(Sidley Austin)律所于2月22日举行线上讲座,解读 FDA 近期关于仅中国试验策略、数据可靠性和监管参与必要性的挑战。现就讲座要点整理如下:
基于外国数据获得美国批准的监管要求
两个法律依据 21 C.F.R. 312.120(a)(1) 和 21 C.F.R....
|

|
【问答】美国律师谈 FDA 关于仅中国试验策略、数据...
2022.02.25
识林联合IPEM教育项目和美国盛德(Sidley Austin)律所于2月22日举行线上讲座,解读 FDA 近期关于仅中国试验策略、数据可靠性和监管参与必要性的挑战。现就讲座现场问答整理如下:
1:FDA如何认定研究员有足够的经验与资质?
FDA会通过考量研究人员之前是否参与过FDA对于临床试验...
|

|
只能买$10000的原研却买不到$450的仿制?美国联邦政...
2022.02.24
在美国,当社会把矛头朝向高药价时,药企总是“甩锅”给药房福利管理(pharmacy benefit managers,PBM),痛陈这些“邪恶”的中间人如何操纵药品市场。
近日,旨在阻止可能给消费者带来危害的行为的美国联邦贸易委员会(Federal Trade Commission,FTC)召开听证会,结果颇具争议。F...
|

|
【识林主题词】新增:外消旋体,Meta分析,质量文化,...
2022.02.24
什么是识林主题词?
— 主题词是识林产出的知识,源于对大量法规、文献、案例、问答的综合分析,并从概述/概述、法规指南、实施指导、视频、问答、案例、参考资料等多维度呈现。
— 区别于散点化的法规和技术资料,主题词是精炼沉淀的知识,目的是帮助识林用户系统学习,全面了...
|

|
ICH 考虑开辟途径吸收临床医生和患者代表意见
2022.02.23
ICH 正在寻求增加医务人员和患者群体参与其指南制定过程的方法,尤其是在涉及临床试验时。
ICH 去年 11 月在一次关于 E8(R1)《临床研究的一般考虑因素》指南的公开会议上讨论了一些不同寻常的内容,建议临床医生和患者代表应与监管机构和行业团体一样在 ICH 中占有一席之地。
自 ...
|

|
欧盟监管机构 2025 工作计划重点:提高药品供应
2022.02.23
欧盟成员国人用药互认和分散程序协调小组(CMDh)最新发布的到 2025 年的多年度工作计划中的关键优先事项之一是改善欧盟基本药物的供应。
工作计划概述了 CMDh 为解决优先领域而打算采取的几项短期和长期行动。提高药品供应,尤其是基本药品的供应是首要任务。CMDh 在工作计划中指...
|

|
国际药政每周概要:2022.02.14-02.20
2022.02.22
02.14 【FDA】2021年仿制药办公室年度报告
美国 FDA 仿制药办公室(OGD)发布了第 7 份年度报告。去年,仿制药项目批准了数百件简化新药申请(ANDA)和数千份补充申请。OGD 优先审评为新冠患者提供潜在治疗和支持性治疗的仿制药申报,批准了超过 75 件的原始 ANDA。另外,OGD ...
|

|
业界呼吁 FDA 可见异物分类和检查与 USP 保持一致
2022.02.22
制药商和行业团体最近在对美国 FDA 《注射剂产品中可见异物的检查》指南草案的反馈意见中,敦促 FDA 将其可见异物分类类别与美国药典(USP)通则 保持一致。
FDA 于 2021 年 12 月 21 日发布《注射剂产品中可见异物的检查》指南草案并公开征询意见,旨在帮助制药商建立检...
|

|
国内药政每周导读:2022.02.14-02.20
2022.02.21
【注册、审评、审批】
2.18,CDE公开征求《药品注册受理审查指南(试行)》意见
2.18,广东省局、卫健委发布第二批粤港澳大湾区内地临床急需进口港澳药品医疗器械目录
2.16,CDE新增药品审评报告和说明书:注射用左亚叶酸钠
【临床】
2.18,CDE正式发布《新型冠状...
|

|
FDA 新任局长工作重点:反击错误信息,加固科学基础
2022.02.21
新上任的美国 FDA 局长 Robert Califf 在 2022 年 2 月 17 日与 FDA 工作人员和公众的首份备忘录中承诺,打击有关科学和 FDA 的错误信息和应对持续的新冠(COVID-19)大流行是其重新掌舵 FDA 后的首要任务。
Califf 于 2 月 15 日以 5046 票的微弱优势得以再次出任...
|

|
【周末杂谈】信达PD1审批与“知己知彼”
2022.02.20
从厂家和客户关系的角度,分析企业与FDA的交流
药品是商品。商品有客户。商品的设计和研发应围绕客户需求。
药品是特殊商品。药品的首客户是药监局。药监局不满意,何谈其他(医生、患者、医保)?
2月10日的“信达”PD1审批专家会上(严格讲,这不是关注疗效的传统意义上的新药...
|

|
讲座:美国律师谈 FDA 关于仅中国试验策略、数据可...
2022.02.18
美国 FDA 官员最近发表了几项声明,重点关注仅在中国进行的成功临床试验可能不足以获得美国批准,更倾向于进行国际多中心临床试验(MRCT)。他们还关注到数据可靠性的重要性,当中国申办人设计旨在获得美国批准的临床试验时来自 FDA 的具体产品建议可能会有帮助,以及在没有事先咨询 F...
|

|
FDA 发布 42 篇 BE 指南,新增诺西那生钠指南
2022.02.18
美国 FDA 于 2022 年 2 月 17 日发布了新一批 42 篇具体产品指南(PSG),为仿制药的开发和生成支持简化新药申请(ANDA)批准所需的证据提供建议,从而帮助简化企业仿制药开发和 FDA 的 ANDA 审评。
这一批 42 篇具体产品指南包括:29 篇新增和 13 篇修订。34 篇(其...
|

|
英国 MHRA 总结新冠疫情期间临床试验经验
2022.02.17
英国药品与医疗保健产品监管机构(MHRA)在其官方博客中回顾了在新冠大流行期间对于临床试验所学到的经验教训以及如何利用这些经验构建英国临床试验生态系统并最终使患者获益。
在大流行开始时,MHRA 指派了专门的新冠审评员,并制定了预评估试验文件的流程,因此在方案和支持文件最终...
|
|
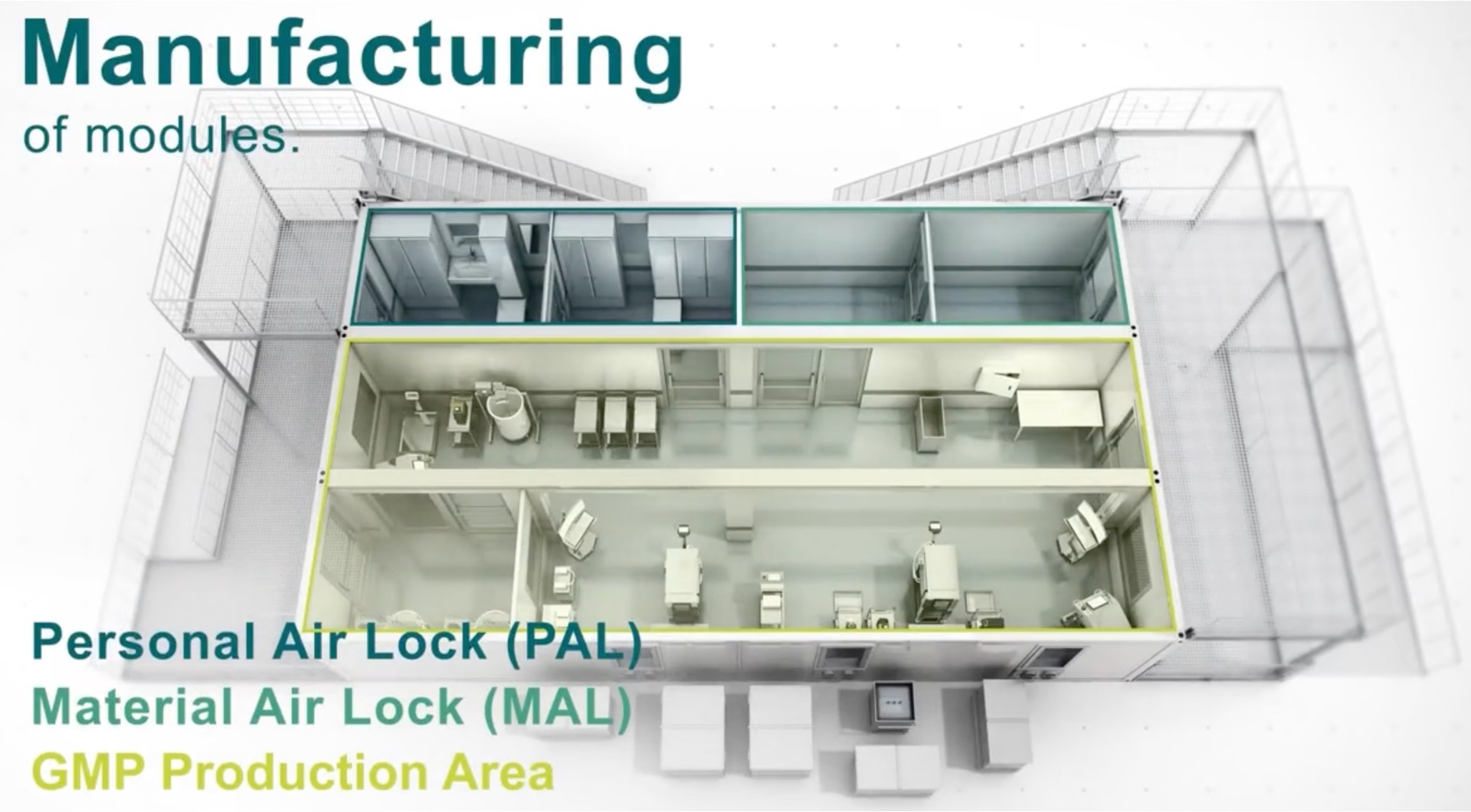
BioNTech 推出可全球生产 mRNA 疫苗的廉价可运输模...
2022.02.17
德国 BioNTech 公司于 2022 年 2 月 16 日在一次会议上公布了其在塞内加尔、卢旺达和“可能在南非”的首个“模块化”mRNA 生产设施。
塞内加尔和卢旺达将于 2022 年年中开始建造第一批设施。这些设施是由堆叠的集装箱制成的即用型场地,公司将其命名为“BioNTainer”。该设...
|

|
Robert Califf艰难获FDA局长提名确认,Woodcock将出...
2022.02.16
2022 年 2 月 15 日,美国参议院以 50 比 46 票的微弱优势,正式确认 Robert Califf 为美国 FDA 局长。
这一投票终于结束了 FDA 历史上最旷日持久且最具争议的确认程序。FDA 局长候选人从未有人以如此接近的票差勉强通过确认程序。不过 FDA 总算结束了近 400 天没...
|

|
【识林会议日历】20220215-0228 预告
2022.02.15
识林会议日历
会议是医药产业学习的关键途径之一。会议数量太多,质量参差不齐,没有实时更新提醒的平台,经常会错过一个好会、或在一个不好的会耽误时间,并无处吐槽。
识林会议日历,专门搜集国内外有专业声誉和影响力的会议日程,梳理详细信息和原始链接,并提供评分和评价功能...
|