
|
法律专家回答国内企业关注的 FDA 疫情期间检查的问...
2020.07.30
美国参议院最近召开了题为“COVID-19及后续:对FDA海外制药检查程序的监督”的听证会,要求FDA对海外企业的监管更加严格。在这样的大环境下是否坚持国际化路线,应该如何坚持并应对新局势?
识林联合IPEM教育项目和美国霍金路伟(Hogan Lovells)律所,于7月25日举办了link=13px 线上...
|

|
Moderna 疫苗III期入组标准惹争议,FDA 将开展实时...
2020.07.29
美国 Moderna 公司于 7 月 27 日宣布启动针对其 COVID-19 候选疫苗的关键性 III 期试验,入组标准将排除已知新冠感染史者,引发专家疑问。当天 FDA 局长 Stephen Hahn 表示,FDA 将对 Moderna 公司的候选疫苗执行实时评价机制,实时审评从开始 III 期试验的当天开始...
|

|
美国开始生产供仿制药用的原料药和中间体
2020.07.29
一小时前,北京时间今晨 5 点 20 分,美国总统特朗普在白宫宣布了伊士曼柯达公司(Eastman Kodak Co)在美国生产 API 的 7.65 亿美元的合同,用于为美国仿制药生产 API 和中间体。
柯达公司获得的这笔合同是根据美国《国防生产法案》的首个针对 API 生产的政府贷款合同...
|

|
生物制药公司为共享新冠单克隆抗体制造信息扫清监管障...
2020.07.28
美国司法部同意几家大型生物制药公司的申请,对于共享与治疗 COVID-19 的单克隆抗体(mAb)药物相关的某些详细制造信息,不实施任何反托拉斯限制。
正在开发中的用于治疗 COVID-19 的单克隆抗体包括可以直接靶向冠状病毒的中和抗体,以及可以解决急性呼吸窘迫综合症的抗体。中和...
|
|
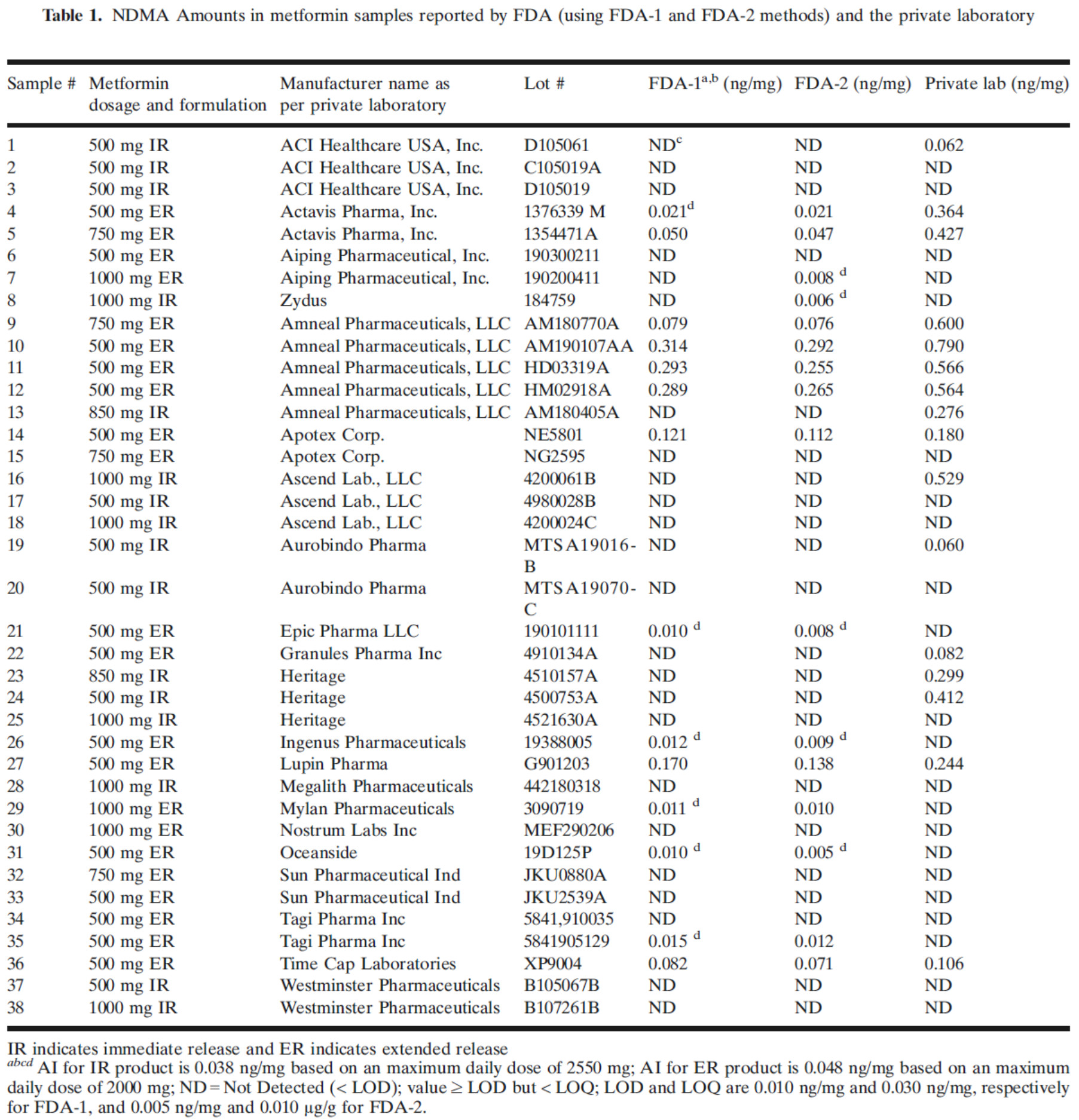
FDA 发论文为亚硝胺检测方法辩护,USP 推出检测亚硝...
2020.07.28
美国 FDA 认为其对二甲双胍中 N-亚硝基二甲胺(NDMA)的检测结果比私营实验室 Valisure 的结果更准确。7 月份发表在美国药物科学家协会(AAPS)上的一篇论文为 FDA 的检测方法做了辩护。FDA 表示,私营实验室的方法“不适用于对二甲双胍药品中的 NDMA 进行定量分析,原因是存...
|

|
【一周回顾】2020.07.20-07.26
2020.07.27
识林推出“中国、欧盟附条件批准程序对比”以及带注释版《药品生产监督管理办法》。药审中心发布药物临床数据递交以及相关指南。卫健委发布抗菌药临床应用及儿童抗菌药应用指南。WHO 发布扎那米韦及吸入粉雾列入国际药典的提案草案。EMA 发布制药用水质量定稿指南。FDA 两大审评收费...
|

|
FDA 处方药收费新一轮谈判可以期待些什么?
2020.07.27
细胞与基因疗法成为关注重点,真实世界证据仍将加码
继仿制药使用者付费(GUDFA III)重新授权首次公开会议之后【GDUFA III 谈判拉开帷幕,业界提出多条改进建议 2020/07/23】,FDA 处方药使用者付费(PDUFA) VII 重新授权首次公开会议也于 7 月 23 日召开,会上 FDA、...
|

|
【周末杂谈】从立法看科学和理性监管
2020.07.26
仿制药标签修订法案中,多数条款是约束FDA而不是企业行为的。
非资源性日用消费品市场,市场经济应是最有效的。药品市场是例外,原因之一是有药监局的存在。对药监局而言,保护和促进公众健康是使命,干预市场是手段,依法定规、行规及释规是功能。因此,要想科学理性监管,首先药品法...
|

|
真实世界证据对随机对照试验的复制能力与支持监管决策...
2020.07.25
随机对照试验(RCT)一般被认为是评价药物安全性和有效性的金标准,并为药物临床研究普遍采用。然而,传统RCT所需的长时间和高成本以及日常诊疗电子健康数据的激增,使人们越来越关注真实世界数据(RWD)能否开发为支持监管决策的真实世界证据(RWE)。RWE已对批准后药物安全性监管决策做...
|

|
美国政府与辉瑞达成疫苗最大订单,为新冠疫苗价格定下...
2020.07.24
7 月 22 日,美国政府与辉瑞公司和 BioNTech 美国公司签订了 19.5 亿美元的疫苗购买合同,这是迄今为止美国政府宣布的最高疫苗合同金额。
根据宣布的协议,美国卫生部(HHS)的生物医学高级研究与发展局(BARDA)和国防部将在辉瑞成功制造并获得批准或紧急使用授权(EUA)后,以 ...
|

|
COVID-19 和中美新形势下,中国药企在美风险和应对
2020.07.24
7月23日,FDA举办了题为“面向全球利益攸关方的药品质量(Pharmaceutical Quality for Global Stakeholders)”的大型网络研讨会,会议有超过1700人报名(据说大半来自印度药企,而非中国),尽管这个报名人数远逊于一门普普通通的国内网课(平均3000人,参考识林资讯【网课时代大数据...
|

|
COVID-19 疫苗公众教育与研发同样重要
2020.07.23
【编者按】在全球疫苗研发人员争分夺秒开发 COVID-19 疫苗之时,我们不能忘记另外一个重要的人群:疫苗所服务的普通大众。研发者开发出安全有效的疫苗,制造商接过接力棒生产出高质量的产品,所有这些努力最后还有临门一脚 — 人们愿不愿意伸出手臂让小瓶中的液体注入自己体内。而...
|

|
GDUFA III 谈判拉开帷幕,业界提出多条改进建议
2020.07.23
7 月 21 日,美国 FDA 举行了仿制药使用者付费修正案第三次重新授权(GDUFA III)公开会议,以从联邦机构、医疗机构、行业协会和其他利益相关者那里获得有关 GDUFA III 期重新授权准备工作的初步意见。
FDA 局长 Stephen Hahn 医学博士做了介绍性发言,仿制药办公室(OGD)主任 S...
|

|
赛默飞世尔工厂接受 EMA 远程检查的经验分享
2020.07.22
尽管 COVID-19 大流行造成了国际旅行限制,但最近欧洲药品管理局(EMA)对位于美国佛罗里达州一家工厂的虚拟监管检查给业界带来了一些希望:全球制药生产部门和监管机构能够以某种看似正常的方式维持下去。
赛默飞世尔法规事务经理 Monica Commerford 在最近 ISPE 召开的生物制...
|

|
仿制药标签修订新篇章:新法案将以合理方式提供变更路...
2020.07.22
7 月 15 日,美国众议院能源和商业委员会投票通过了H.R. 5668
《2020 年对新标签客观药物证据修订法案》(2020 MODERN 标签法案),该立法概述了当参照上市药品不再销售时进行仿制药标签变更的方法。
关注识林的读者对于仿制药标签变更方面的重要性和问题可能已经不陌生,我...
|
|
糖尿病药上市前安全性争论不停,FDA 新指南草案受质...
2020.07.21
美国 FDA 于 3 月份发布《2 型糖尿病:评估新药的安全性以改善血糖控制》指南草案向公众征询意见,指南中关于糖尿病药物 III 期安全性数据库的规模和组成引发了业界的担忧。企业认为,指南对 III 期试验安全性的建议过于严苛,并且规模不必要的大,且缺乏正当性。
利益相关者...
|

|
FDA 监管思路转变:从律师至上到技术驱动?
2020.07.21
【编者按】从目前看,FDA 讲数据、深度挖掘、人工智能重要性的人还多数是做数据的人,而不是做临床审评的人。大数据和数据大不是一回事。人工智能与智能也不是一回事。重视数据不错,但能否对审评质量和效率有实质改进,还有待观察。
美国 FDA 升级信息技术基础设施的努力可能会为...
|

|
【一周回顾】2020.07.13-07.19
2020.07.20
识林推出“国内外审评期间资料补充对比”。WHO 发布口服固体制剂溶出度测试指南,并发布在 WHO 基本药物清单中确定进行溶解度测定的 API 优先次序,COVID-19 候选治疗药地塞米松和羟氯喹在列。药审中心发布新冠肺炎疫情期间药物临床试验管理指导原则,并发布抗肿瘤药联合治疗临床...
|

|
欧盟人用药中亚硝胺杂质评估报告要点
2020.07.20
欧盟药品管理局(EMA)于 7 月 9 日发布《人用药中的亚硝胺杂质评估报告》,详细解释了有关亚硝胺杂质根本原因调查、科学讨论以及专家组意见,并为制药公司提供了有关如何避免人用药中亚硝胺杂质存在的建议。
除了 EMA 已经要求对含化学合成 API 的药品申办人对其产品中可能存...
|

|
【周末杂谈】质量管理可以职业化吗?
2020.07.19
职业化使得行医成为受人尊敬、高薪酬的职业,药业可否效仿?
上世纪初,美国在经济上跃居世界之首的时刻,痛改医学院教学多小散乱差的局面,旗帜鲜明地树立以科学为纲的教学和行医准则,统一全国的医学院教程,关闭一半的医学院,减少医生数量、提高医生质量,使得行医成为受人尊敬、高...
|