
|
制药商因同款药获批将FDA告上法庭 - 从免费到37万...
2019.06.25
故事的发展变得越来越有意思了。大家是否还记得我们之前曾报道过一个年价 37 万美元的孤儿药?Catalyst 公司的 Firdapse,FDA 于去年 11 月批准的首个用于治疗Lambert-Eaton肌无力综合征(LEMS)的药物。FDA 的批准引发了一场风暴,在那之前,患者可以通过同情使用计划从一家小型家...
|

|
美国生物药是否真的需要 12 年市场专营权?
2019.06.24
人们普遍认为生物药由于其复杂性,开发过程耗时且昂贵。因此《生物制品价格竞争与创新法案》规定生物药的专营权期限为 12 年。相比之下,Hatch-Waxman 法案规定新分子实体专营权为五年。但 6 月 18 日发表在《自然 – 生物技术》(Nature Biotechnology)上的一项研究通过分析...
|

|
【更新提示】识林一周回顾(20190616-0622)
2019.06.23
【IPEM】7月课程通知
IPEM 7月份IPEM课程即将在北京开班,课程安排如下:
7 月 4-5 日,Garth Boehm博士,课程:根据预BE结果调整口服固体制剂处方工艺。
7 月 6 日,张哲峰博士,课程:口服固体制剂的一致性评价与参比制剂的选择。
7 月 7 - 8 日,何公欣博士...
|

|
FDA 公开表示 USP 生物制品标准阻碍创新
2019.06.22
美国 FDA 的主要官员公开发文表示 FDA 对于美国药典(USP)生物制品药典标准的立场并做出解释,认为 USP 生物制品药典标准对于确保安全和质量并不会提供额外保证,并且可能会给审评人员和行业增加负担,减少竞争,限制创新。
美国药典会正在反对一项参议院拟议法案,该法案规...
|

|
2018 年指证数据可靠性问题的 FDA 警告信情况
2019.06.21
2018年FDA警告信中指证的数据可靠性缺陷
2018年FDA警告信中指证的数据可靠性失败中最为常见的违反法规的情况
过去11年中,指证存在数据可靠性缺陷的FDA警告信数量变化情况
过去11年中FDA警告信中指证的数据可靠性问题及趋势
企业可采取的防范、确定和改正问题的措施:高级管理层有责...
|

|
美国阿片类药物危机战火波及 WHO
2019.06.21
06/21 更新:WHO 于本周在一份声明中表示,“WHO 正在根据自指南发布以来出现的新科学证据而撤销这些指南。这也将解决所提到的有关专家利益冲突问题。”
----
两名美国国会议员敦促世界卫生组织(WHO)撤销近十年前发布的治疗疼痛的指南,因为这些指南中含有“危险的误导”...
|

|
FDA 第IV段专利声明清单包含新数据以促进仿制药竞争
2019.06.20
美国 FDA 于 6 月 18 日表示,在决定是否提交仿制药申请时,仿制药申请人将从 FDA 获得更多信息,这可能会增加早期批准的可能性。
过去,清单仅包括药品名称、剂型、规格、参照上市药品(RLD)/新药申请(NDA)号,以及向 FDA 提交包含第 IV 段声明的首份实质完整的仿制药...
|

|
拖延仿制药批准、公民请愿与监管透明度
2019.06.19
为拖延仿制药(ANDA,505(j))、改良药(505(b)(2))和生似药(351(k))的注册审批,原研药公司可以向美国FDA提交公民请愿(citizen petition),引证如生物等效或其它安全性问题,提出FDA应拒绝批准某注册申请。收到请愿后,FDA有150天时间决定是否接受该请愿。若是请愿在FDA即...
|

|
MHRA 检查员强调对 QA 的重视并分享实验室关键检查...
2019.06.18
我们在昨天的资讯中介绍了英国药品与医疗保健产品监管机构(MHRA)GCP 和 GLP 资深检查员 Jason Wakelin-Smith 在今年 3 月举办的 MHRA 实验室研讨会上关于实验室数据可靠性实践问题的一些看法。【英国 MHRA 检查员关于实验室数据可靠性实践问题的评论 2019/06/17】今天我...
|

|
英国 MHRA 检查员关于实验室数据可靠性实践问题的评...
2019.06.17
英国药品与医疗保健产品监管机构(MHRA)资深检查员极力鼓励把数据工艺映射(data process mapping)作为规划、建立和维护数据可靠性(DI)所必需的控制措施的第一步。另外还就数据可靠性实践中的一些常见问题从检查员的视角给出了切实的答案。
虽然 DI 的概念并不新鲜,但现代可互...
|

|
【更新提示】识林一周回顾(20190609-0615)
2019.06.16
【WHO】TRS 1016 世界卫生组织药生物制品标准专家委员会第69次技术报告(06.15)
WHO的TRS 1016文件阐述了专家委员会在2018年10月的专家会议上作出的决定和建议,包括疫苗和生物治疗药物,血液制品和体外诊断标准化,与生物制品的生产,质量控制和评估有关的国际建议和准则;抗生素,...
|

|
FDA 配药监管移至合规办公室,预示将加大执法力度?
2019.06.15
美国 FDA 宣布计划将监督配药和外包机构的办公室从药品审评与研究中心(CDER)主任办公室,转移至合规办公室。该举措意味着配药监管计划的“制度化”,配药监管计划自建立以来已经发展成为一个更成熟的项目。
CDER 主任 Janet Woodcock 于 6 月 10 日发送给员工的备忘录中宣...
|

|
FDA 连续制造质量考量指南草案引发制药商担忧
2019.06.14
针对FDA公布的《连续制造质量考量》指南草案的评议显示,品牌药制造商关注指南所涉范围是否包含原料药,以及术语定义方面的问题,而仿制药制造商则对连续制造有可能导致制药成本高企和缺乏效益,对连续制造有可能阻碍仿制药新入局者表示担忧。有制药商与行业组织提出FDA的指南将如何与即将...
|

|
英国 MHRA 就分析质量源于设计公开征询意见
2019.06.13
英国药品与医疗保健产品监管机构(MHRA)于 6 月 4 日宣布计划将分析质量源于设计(AQbD)原则应用于药典标准,并向利益攸关方征询反馈意见pdf 。MHRA 认为采用 AQbD 原则能够提供“明显的附加获益”并且能够使英国药典中的分析方法框架“比目前更加健全和清晰”。
MHRA 发布...
|

|
口服固体缓控释制剂专题青岛会议(首轮通知)
2019.06.12
高端制剂暑期论坛
口服固体缓控释制剂专题青岛会议
第一轮通知
2019年8月3 - 4日
青岛海泉湾皇冠假日度假酒店
主办单位:北京大学药物信息与工程研究中心
承办单位:青岛百洋医药股份有限公司
支持单位:上海安必生制药技术有限公司;北京宽见科技有限公司...
|

|
探讨在制药质量管理中运用 AI 工具
2019.06.12
药品投诉通常属于滞后指标,一旦发生问题,就展开响应式调查。借助于人工智能工具,将来的场景或许变为以积极主动的方式查看所有数据和系统,能够主动预测并做出决策。对于习惯于事后开展响应式调查的业界人士来讲,这样的场景或许有些科幻和遥远,对于AI术语,刚接触时也会感到晦涩、难...
|

|
连续制造发展趋势
2019.06.11
不到四年前,只有一款美国 FDA 批准的产品是通过连续制造生产的。现在有四家公司的五种获批产品通过连续制造生产。另外还有 20 家公司(包括品牌药和仿制药)已经在与 FDA 联系,努力开发和实施连续制造流程。据研究预测,2016 年价值 17.4 亿美元的全球医药连续制造技术市场到 2...
|
|
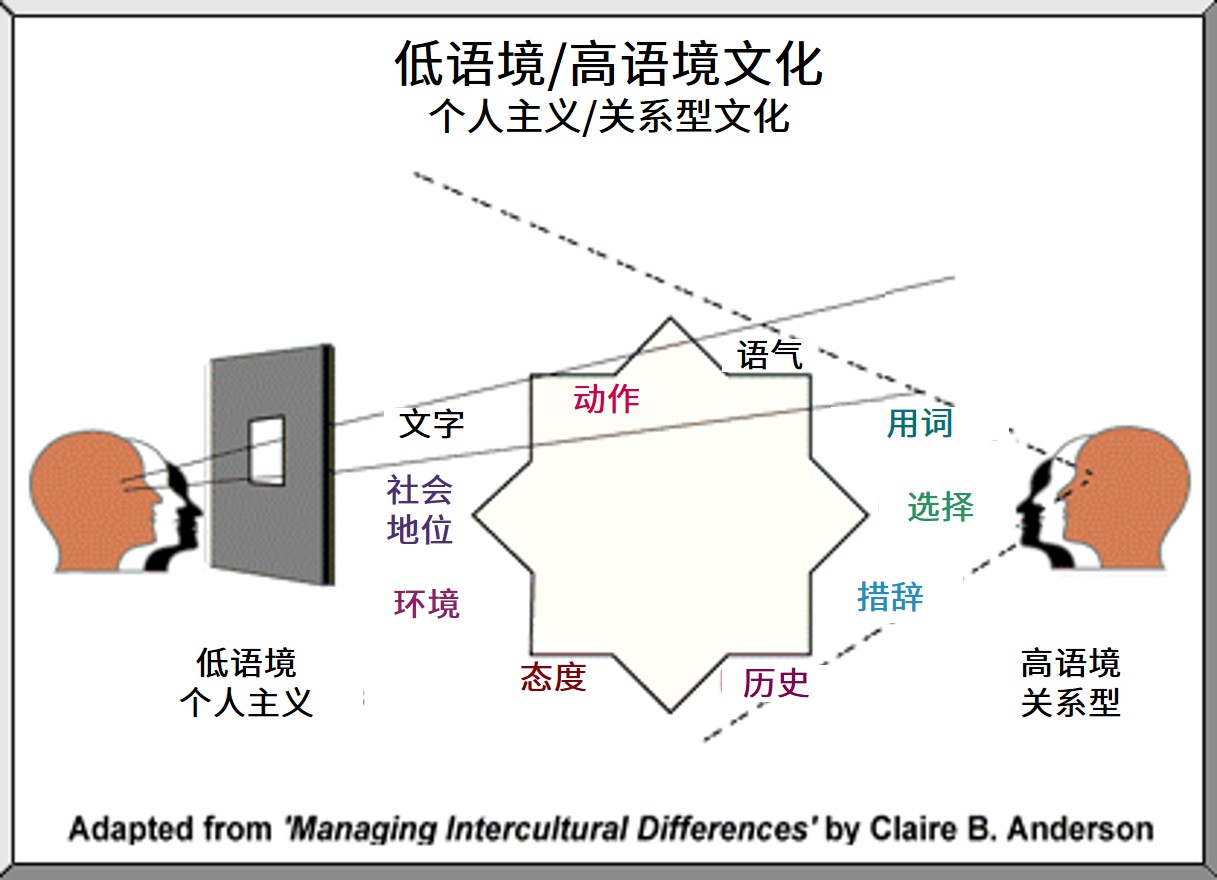
语境沟通造成的人为错误对数据可靠性的影响
2019.06.10
尽管直接负责数据可靠性的人员尽最大努力改善,但人为错误仍然无时不在。公司领导层必须始终考虑人为因素将如何影响组织的数据可靠性,因为即使是拥有最先进的数据可靠性实践的最成熟组织也可能经历人员流动或招聘新员工,这些新进人员必须接受教育并融入到组织的文化和运营之中。
人为...
|

|
【更新提示】识林一周回顾(20190602-0608)
2019.06.09
识林用一周回顾包成一颗资讯的粽子送给大家,祝各位端午安康!
【FDA】指南草案 增强临床试验人群的多样性 - 资格标准,入组实践和试验设计(06.07)
针对参与临床试验的挑战,该指南建议临床试验申办方支持新药申请或生物制品许可申请可以采取的方法,在科学和临床上适合时扩大...
|

|
FDA 使用机器学习建模预测 ANDA 申报
2019.06.08
美国 FDA 研究人员 4 月 22 日在线发表在《临床药理学和治疗学杂志》上的一篇文章指出,利用药品、监管和药物经济学信息可以准确地预测新化学实体的首个简化新药申请(ANDA)申报的时间。这种建模方法可以帮助 FDA 优化其在仿制药使用者付费(GDUFA)计划下的资源分配和工作量,并...
|