
|
欧盟和英国兴起的远程分散式临床试验
2023.01.05
远程分散式临床试验正在欧盟和英国兴起。关于此类临床试验,欧盟曾出台相关指引。2022 年 12 月,欧盟发布了关于如何开展此类临床试验的新指引,对现有指引进行了补充。为此,盛德主办律师 Zina Chatzidimitriadou、资深主办律师 Lauren Cuyvers和实习律师 Bronwyn Tonelli 探讨...
|

|
研究显示制药商从吸入装置二级专利中获利匪浅
2023.01.05
2023 年 1 月 3 日发表在美国医学会杂志(JAMA)上的一篇研究文章1表明,即使主要专利已过期,制药商正在通过二级专利从避免仿制药竞争中“实质性”获益。
研究的主要作者、波士顿布莱根妇女医院副医师的 William Feldman 医学博士表示,自己在肺部和重症监护室实习时注意到有...
|

|
美国众议院调查报告建议 FDA 修订申办人互动和阿尔...
2023.01.04
上周我们报道了美国众议院两委员会联合对渤健阿尔茨海默药 Aduhelm 审批和定价过程的调查报告,揭示了 FDA 存在的一些不恰当行为以及企业的贪婪。报告中的发现引起了人们对 FDA 在程序方案方面的失误以及渤健在 Aduhelm 批准过程中无视疗效和可及性的严重关切。这些发现也证明了专...
|

|
美国众议院关于阿尔茨海默新药的调查报告中未回答的问...
2023.01.04
上周发布的美国众议院两委员会联合对渤健阿尔茨海默药 Aduhelm 审批和定价过程的调查报告,揭示了 FDA 存在的一些不恰当行为以及企业的贪婪,同时也给出了一些建议。但对于 FDA、渤健以及阿尔茨海默病治疗药的未来,一些资深专家指出报告未在几个重要方面给出答案。
1. FDA 有...
|

|
国际药政每周概要:FDA有关在短消息等情形中的处方药...
2023.01.03
【注册、审评、审批】
12.28【FDA】FDA D.I.S.C.O. 突发版:FDA 批准菊欧文氏菌(重组)天冬酰胺酶的新给药方案
【创新研发与临床】
【GxP 与检查】
12.27【FDA】警告信 美国 MD Pharmaceutical Supply, LLC
【监管综合】
12.27【FDA】在线字符空间限...
|

|
FDA 向原料药再包装商发布警告信,投诉调查不充分未...
2023.01.03
美国 FDA 于 12 月 27 日公布了一封 11 月发送给位于宾夕法尼亚州 Hanover 的一家原料药再包装商 MD Pharmaceutical Supply 的警告信。FDA 列出了在 2022 年 4 月到 5 月间对其工厂进行检查后发现的一些问题。
FDA 在警告信中指出的主要缺陷项包括,企业没有充分调...
|

|
国内药政每周导读:MAH责任管理落地,2021年监管统计...
2023.01.02
【CMC药学开发与仿制药】
12.27,【CDE】关于发布《同名同方药研究技术指导原则(试行)》的通告(2022年第48号)
12.28,【NMPA】关于发布仿制药参比制剂目录(第六十二批)的通告(2022年第62号)
12.29,【中检院】国家药品抽检探索性研究情况(第十期)
【注册、审评、审...
|

|
识林年度回顾:2022 年热点资讯
2023.01.02
2022 年已经过去,2023 年正在展开。新年之际,我们一起来回顾一下识林读者在过去一年中关注的热点话题。
1. 信达 PD-1 出海之路
FDA 对信达 PD-1 的审批过程显示我国药业的国际化已进入了新发展阶段。如何调整战略战术,无论是对企业还是政府,可能都要从长计议。知己知...
|
|
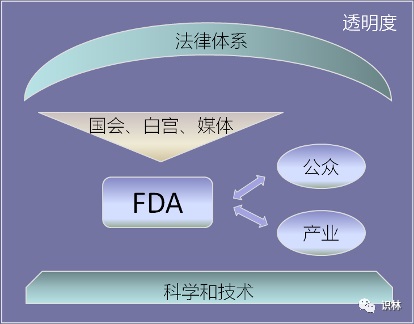
【周末杂谈】广义的监管体系
2023.01.01
FDA的服务和监管对象,监督方,科技基础,法律体系和透明度
瑞士有以罗氏和诺华为代表的强大制药产业,但只有8百余万人,很小的药品市场。印尼有2.7亿人,但药业平平。前者的药主要供国际市场。由于在哪卖药,就受哪的药监局管,所以瑞士药监局对其药业的影响还不如美国FDA的大。印尼...
|

|
轻松一刻 - 制药人的苦辣酸甜
2022.12.31
年复一年,总有苦辣酸甜;不变的是保持学习,为了心中的愿望,撸起袖子加油干!
识林祝大家 2023 新年快乐!
识林轻松一刻,意在以漫画形式,展现药企人酸甜苦辣,博得识林读者会心一笑之余,也希望带来些许回味与思索。
识林欢迎读者提供素材,可以是...
|

|
WHO 发布药品研发期间的 GMP 定稿指南
2022.12.30
WHO 于 12 月 22 日发布了第 56 届药物制剂规范专家委员会(ECSPP)技术报告 1044(TRS 1044),定稿了大批指南和标准,其中包括《研究和开发设施的良好实践》指南。
指南为在成员国上市销售申请和 WHO 预认证中提交数据的研发批次、中试批次和稳定性检验的良好规范提供了指...
|

|
美国众议院委员会发布对渤健阿尔茨海默药 Aduhelm ...
2022.12.30
美国众议院监督和改革委员会和能源与商业委员会在对 FDA 关于渤健(Biogen)的阿尔茨海默药 Aduhelm 的监管审评和批准程序以及渤健对 Aduhelm 的定价进行了为期 18 个月的调查,整理了超过 50 万页来自 FDA 和渤健的文件后发布了一份46 页的工作人员报告。随报告一同发布的还有...
|

|
WHO 发布研究用药品 GMP 定稿指南
2022.12.29
WHO 于 12 月 22 日发布了第 56 届药物制剂规范专家委员会(ECSPP)技术报告 1044(TRS 1044),定稿了大批指南和标准,其中包括《研究用药品 GMP》指南。
该指南是对 1996 年相同主题 GMP 附录 7 的修订,几乎相当于重写。由于原先的指南发布日期较旧且最近对 COVID-...
|

|
ICER 公布渤健和卫材以及礼来两款最新阿尔茨海默药成...
2022.12.29
美国临床与经济评价研究所(ICER)于上周发布的一份分析草案指出,卫材和渤健(Biogen)公司最新的阿尔茨海默病治疗药 lecanemab 每年需要低于 2 万美元才能具有成本效益。
ICER 深入研究了 lecanemab 的证据并得出结论认为,根据该药已证明的获益 — 适度但具有统计学意义的...
|

|
FDA 就数据可靠性问题向巴西原料药生产商发布警告信
2022.12.28
美国 FDA 于 12 月 20 日公布了一封 12 月初发送给位于巴西里约热内卢的一家原料药生产商 Nortec Quimica 的警告信。FDA 列出了在 8 月份对其生产工厂进行检查后发现的一些数据问题。
FDA 表示,Nortec Quimica 对其电子数据和软件系统没有“系统安全性和访问控制”,...
|
|
首例加州雷尼替丁致癌诉讼案,辉瑞和赛诺菲与原告达成...
2022.12.28
据彭博社报道,继本月初联邦法官对雷尼替丁(品牌名为 Zantac,善胃得)产品责任跨地区诉讼案作出裁决之后,赛诺菲和辉瑞同意就一起将在美国加利福尼亚州开庭审理的案件达成和解。
该诉讼由加州 Alameda 县高等法院提起。据彭博社称,善胃得产品企业与 James Goetz 达成和解,Goet...
|

|
国际药政每周概要:WHO TRS1044,ICH M13A速释固体...
2022.12.27
【注册、审评、审批】
【创新研发与临床】
【GxP 与检查】
【CMC与仿制药】
12.21【FDA】指南草案 仿制药研发相关的受控函
12.21【ICH】M13A 速释固体口服剂型的生物等效性
【药典相关】
12.19【EDQM】欧洲药典增补11.1修订胶塞密封组件通则
【监管综合】
12...
|

|
ICH 发布 M13A 速释固体口服剂型的生物等效性指南...
2022.12.27
ICH 于 12 月 20 日发布了M13A《速释固体口服剂型的生物等效性》第 2b 阶段指南草案,旨在为设计用于递送药物至体循环的速释(IR)固体口服剂型(例如片剂,胶囊剂和口服混悬剂的颗粒剂/粉剂)的研发和批准后阶段进行生物等效性(BE)研究提供建议。
具有全身作用的速释固体口服...
|

|
国内药政每周导读:中药品种保护时隔30年大修,药典25...
2022.12.26
【创新与临床研究】
12.21,【CDE】关于公开征求《罕见疾病药物开发中疾病自然史研究指导原则》意见的通知
12.21,【CDE】关于发布《中药新药用于慢性胃炎的临床疗效评价技术指导原则(试行)》《中药新药用于胃食管反流病的临床疗效评价技术指导原则(试行)》的通告(2022年第47...
|

|
WHO 发布药品生产技术转移定稿指南
2022.12.26
WHO 于 12 月 22 日发布了第 56 届药物制剂规范专家委员会(ECSPP)技术报告 1044(TRS 1044),定稿了大批指南和标准,其中包括《药品生产技术转移》指南。
技术转移是产品生命周期管理的一个组成部分,受到监管期望的约束。技术转移需要一种有计划、基于风险的方法。新修订...
|