|
FDA 批准首个呼吸道合胞病毒疫苗,开启 RSV 重磅疫...
2023.05.05
美国 FDA 于 5 月 3 日批准了首个呼吸道合胞病毒(RSV)疫苗 —— GSK 的 Arexvy,用于 60 岁及以上成年人。
GSK 高级副总裁兼疫苗研发全球负责人 Phil Dormitzer 表示,“经过这么多年,终于有了针对 RSV 的好选择,这令人非常兴奋。这也是基础科学的胜利,一项非常...
|

|
FDA 发布分散式临床试验指南草案
2023.05.05
美国 FDA 于 5 月 2 日发布分散式临床试验(DCT)指南草案,旨在为药品、生物制品和器械临床试验的申办人提供建议。
该指南草案的制定是为了满足《食品和药品综合改革法案》(FDORA)中有关发布或修订指南草案的要求,澄清和推进分散式临床研究的使用,以支持药物和器械开发。
F...
|

|
IPEM课程 GMP指南(第2版)研讨课
2023.05.04
2021年8月,国家药品监督管理局食品药品审核查验中心委托北京大学知识工程与监管科学实验室组织开展“药品GMP指南”修订工作。
来自130多家国内外药品监督管理机构、生产企业和研究机构的500余位专家积极参与再版修订工作,经过多轮审稿,历经18个月,完成了约4500页、500多万字的稿件...
|

|
礼来阿尔茨海默新药三期研究显示患者认知能力下降速度...
2023.05.04
礼来公司于 5 月 3 日表示,其开发的阿尔茨海默病新药 donanemab 在一项 III 期试验中,与安慰剂相比,可使患者的认知和功能下降速度降低 35%,这为向美国 FDA 提交申请铺平了道路。
但 donanemab 研究的积极结果也许会因两名患者(可能还有第三名患者)因该药引起脑肿胀...
|

|
欧盟公布专利改革提案,关注强制许可和补充保护证书
2023.05.03
欧盟委员会于 4 月 27 日发布了一揽子法规,建立欧盟范围内的强制许可计划,允许其它公司在紧急情况下不经专利持有人同意即可生产药品。法规还将建立欧盟区域范围的补充保护证书(SPC),对专利药品的期限最多可再延长五年。目前,SPC 仅在国家层面授权。
委员会表示,这些提案“...
|

|
数据可靠性凛冬之后,爱克龙迎来倒闭结局,召回 70 ...
2023.05.02
继爱克龙(Akorn)在两个月前宣布破产并关闭所有生产场地后,公司正在召回 70 多种产品。
爱克龙是一家美国仿制药生产企业,专注于生产眼科用药,注射剂,口服液,滴耳液,局部药,吸入剂和鼻腔喷雾剂等。它的研究和生产设施曾分布在美国、印度及瑞士。
爱克龙于上周三自愿召...
|

|
国际药政每周概要:欧盟药品立法廿年大修,GMP-GDP检...
2023.05.02
【监管综合】
04.26【EU】欧洲卫生联盟:欧盟委员会提议进行药品改革,目标是更易获得、负担得起和创新的药品
04.26【EU】常见问题解答:药品立法的修订
【注册、审评、审批】
04.26【FDA】批准首个口服粪便微生物产品用于预防艰难梭菌感染的复发
04.25【FDA】FDA 批准...
|

|
国内药政每周导读:Q12实施过渡期2年,放射性药品审评...
2023.05.01
【创新与临床研究】
4.24,【NMPA】关于适用《E19:在特定的上市前后期或上市后临床试验中选择性收集安全性数据》国际人用药品注册技术协调会指导原则的公告(2023年第56号)
4.26,【CDE】关于发布《肿瘤主动免疫治疗产品临床试验技术指导原则(试行)》的通告(2023年第32号)
...
|

|
FDA 基因治疗产品审评团队负责人谈生产变更等 CMC ...
2023.05.01
美国 FDA 生物制品审评与研究中心(CBER)治疗产品办公室(OTP)官员敦促基因治疗产品的开发者避免在后期关键性研究期间实施生产工艺变更,以免以后出现问题,例如产品超标(OOS)。
在 4 月 25 日的网络研讨会上,OTP 基因治疗 1 处的团队负责人 Graeme Price 回答了利益...
|

|
【周末杂谈】渔夫与商人的故事
2023.04.30
渔夫钓鱼是迫于养家糊口,有财富的人钓鱼是自己的选择
大家可能都知道“渔夫与商人的故事”:渔夫躺在海滩上,享受着阳光的温暖和钓鱼的乐趣。路过的商人纳闷,为何渔夫不去捕鱼、努力工作来养家糊口。
【商人】“躺在这里钓不到多少鱼,你应去捕鱼”。
【渔夫头也不抬】“这样做...
|

|
【识林新课程】FDA 2023仿制药论坛,CDE 药品注册沟...
2023.04.29
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的500+门课程3000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,及供应商技术介绍专业课程。除视频内搜索,收藏,评论功能外,部分原声视频实现双语...
|

|
【识林会议日历】5月重点:IPEM新版GMP指南研讨,FDA...
2023.04.29
会议是医药产业学习的关键途径之一。会议数量太多,质量参差不齐,没有实时更新提醒的平台,经常会错过一个好会,或者在一个缺乏知识内容的会耽误时间,无处吐槽。
识林会议日历,专门搜集国内外有专业声誉和影响力的会议日程,梳理详细信息和原始链接,并提供评分和评价功能,可分享...
|

|
欧盟公布药品立法改革提案,二十年来首次大修
2023.04.28
欧盟委员会于 4 月 26 日公布了欧洲药品立法修订提案,这是二十年来欧盟制药政策的首次重大更新。提案包括缩短药品专营期,鼓励制药企业在所有欧盟成员国迅速推出新药。
改革包括两项立法提案:一项新指令和一项新法规,构成了欧盟所有药品(包括罕见病药品和儿科药品)的监管框架...
|

|
FDA 批准首个粪便微生物群口服新药,预防艰难梭菌感...
2023.04.28
美国 FDA 于 4 月 26 日批准了 Seres 药业的 Vowst,用于 18 岁及以上成人患者在复发性艰难梭菌感染(CDI)治疗后预防 CDI 复发,这是 FDA 批准的首款口服粪便微生物群产品。
艰难梭菌会释放出对消化系统造成严重破坏的毒素,在某些情况下,例如服用抗生素治疗感染,可...
|

|
药品GMP指南(第2版)厂房设施设备分册的变化:编委访...
2023.04.27
历经18个月,来自超过130家单位的500余位监管和产业专家完成了4500余页,近500万字的药品GMP指南(第2版)。受指南起草牵头单位--北京大学知识工程与监管科学实验室委托,我们对指南编写小组的专家开展了系列访谈,第四篇请到厂房设施设备分册组长尹放东、副组长郑金旺和编委介绍该分...
|
|
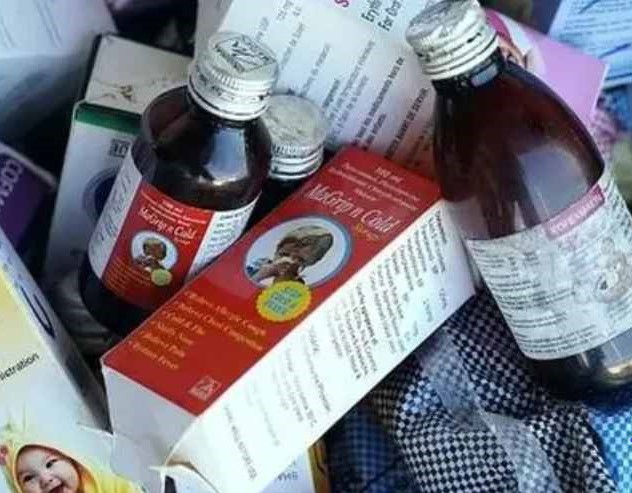
WHO 第四次就印度产受污染止咳糖浆发布产品警示报告
2023.04.27
世界卫生组织(WHO)于 4 月 25 日发布产品警报,报告了另一家印度企业生产的止咳糖浆被发现受到污染。这已是 WHO 自去年 10 月份以来针对受污染止咳糖浆产品发布的第四次警示。
被污染的糖浆为愈创甘油醚糖浆 TG 糖浆,是一种用于缓解胸闷和咳嗽症状的祛痰剂。根据 WHO 的...
|

|
FDA 2023 仿制药论坛上报告的 GDUFA III 相关要...
2023.04.26
美国 FDA 于 4 月 12 日 - 13 日举办了年度仿制药论坛,今年的主题是庆祝仿制药论坛 10 周年。FDA 仿制药领域相关工作人员在会上从 FDA 仿制药审评计划的各个方面作了详细报告。论坛的目的是提供实用建议和说明简化新药申请(ANDA)审评过程,为仿制药申请人提供信息。完整...
|

|
FDA 加速批准渤健肌萎缩侧索硬化症(ALS)新药,基于...
2023.04.26
美国 FDA 于 4 月 25 日通过加速审批路径批准了渤健(Biogen)公司治疗罕见遗传性肌萎缩侧索硬化症(ALS)的新药 Qalsody。这是 FDA 首次基于初步证据在加速审批路径下批准用于治疗 ALS 的药物,这些证据也可能加速未来治疗这种致命的神经退行性疾病药物的开发。
Qalsody ...
|

|
国际药政每周概要:FDA定量构效关系模型建模预测血脑...
2023.04.25
【监管综合】
04.17【FDA】新药办公室着力扩大监管科学研究
【注册、审评、审批】
【创新研发与临床】
04.19【FDA】监管 QSAR 建模的新进展:预测血脑屏障通透性的新 QSAR 模型
04.22【EMA】基于在上市许可中递交的作为关键证据的单臂试验建立有效性思考性文件
【...
|

|
FDA 外部对照试验指南草案解读,仍有问题需要解答
2023.04.25
美国 FDA 药品审评与研究中心(CDER)、生物制品审评与研究中心(CBER)和肿瘤卓越中心(OCE)在今年 2 月份联合发布了一份题为“药品和生物制品外部对照试验设计和实施的考虑因素”的指南草案,为那些考虑使用外部对照临床试验来提供药品安全性和有效性证据的申办人提供建议。
指...
|