|
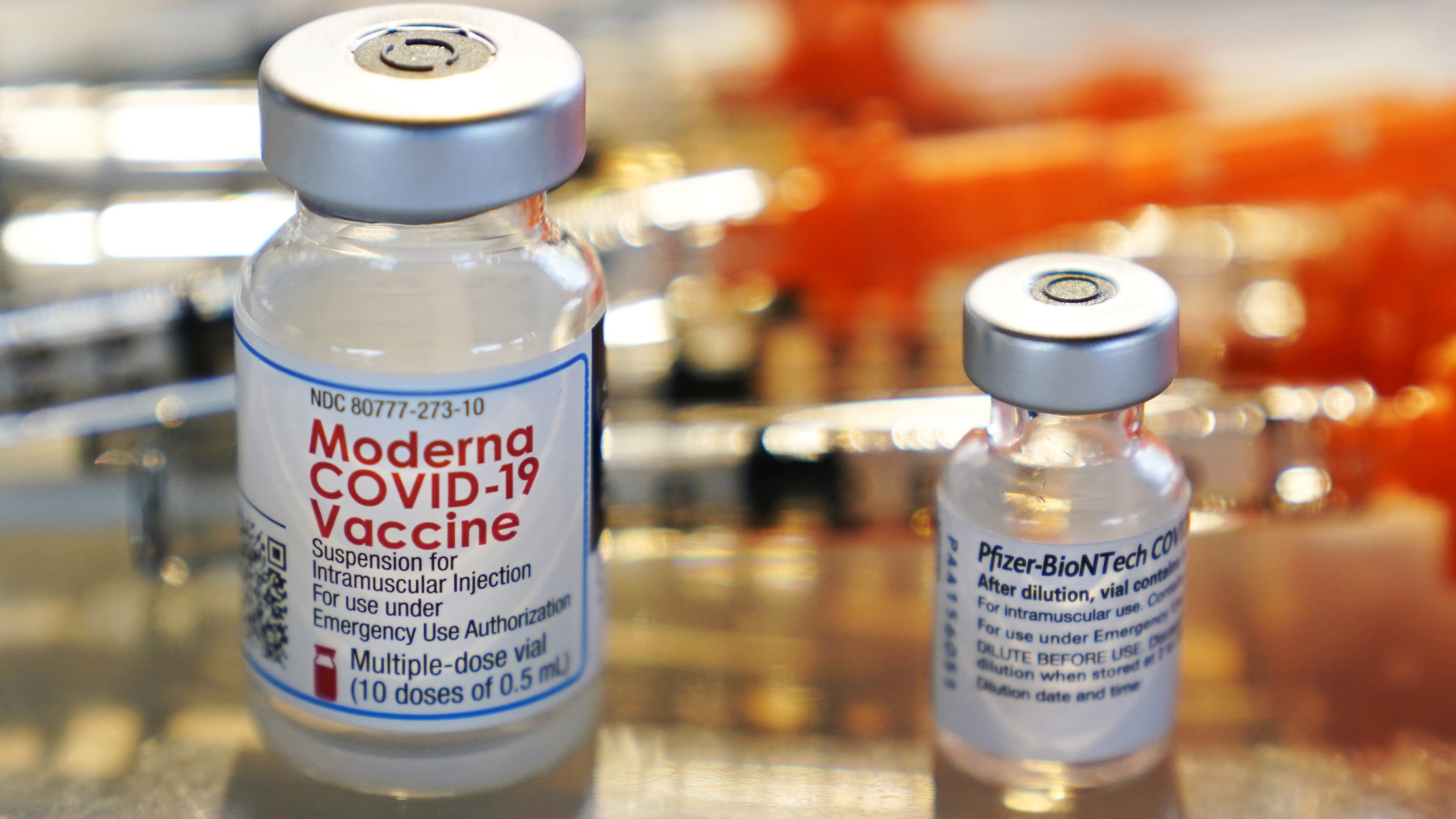
FDA 宣布推迟下周针对辉瑞幼儿新冠疫苗的专家会
2022.02.12
美国 FDA 于 2022 年 2 月 11 日下午表示,取消原定于下周召开的讨论辉瑞幼儿新冠疫苗的专家委员会,以“给 FDA 时间考虑更多数据。”
FDA 生物制品审评与研究中心(CBER)主任 Peter Marks 和 FDA 代理局长 Janet Woodcock 在一份声明中表示,“基于 FDA 的初步...
|

|
罕见之举:FDA 主动要求辉瑞提交幼儿新冠疫苗 EUA ...
2022.02.03
美国 FDA 于 2 月 1 日下午罕见地要求辉瑞公司提交滚动申请,修订其新冠疫苗紧急使用授权(EUA)以包括 6 个月至 4 岁年龄段的儿童。
而与之相对,上个月,辉瑞宣布其疫苗(适用于最年幼人群的 3 µg 剂量)与已证明高有效性的 16 至 25 岁人群相比,对 6 至 24 ...
|
|
辉瑞和 BioNTech 对奥密克戎新冠疫苗开展临床试验,...
2022.01.26
辉瑞和 BioNTech 公司于 2022 年 1 月 25 日在一份声明中表示,他们已经开始一项研究将基于奥密克戎的新冠疫苗与原始疫苗进行比较。辉瑞表示,预计该研究的初步结果将在 2022 年上半年出来,这项研究预期招募 1420 名志愿者。
如果监管机构等待此类研究的数据,这可能意味...
|
|
谁发明了新冠 mRNA 疫苗?Moderna 和美国政府各执...
2021.11.11
根据 2021 年 11 月 9 日下午《纽约时报》公布的一份最新报道显示,Moderna 声称三名美国国立卫生研究院(NIH)科学家并没有参与发明新冠疫苗的关键成分。该声称来自Moderna 于今年 7 月份向美国专利商标局提交的文件。
在提交的文件中,Moderna 表示,已经“达成信实的决定”...
|
|
美国政府审查报告证实新冠疫苗生产场地在获得授权之前...
2021.11.03
一直关注识林的读者可能还记得,去年 12 月份我们就曾讨论过 FDA 授权新冠疫苗之前并没有做批准前检查。现在美国政府的官方报告数据出来了,没做批准前检查是确定的,而其中的一些原液和重要辅料工厂甚至从未接受过 FDA 的检查。
美国政府问责办公室(GAO)在一份最新的报告中表...
|
|
FDA 发布关于 Moderna 和杨森新冠疫苗加强针的专家...
2021.10.14
美国 FDA 将于 10 月 14 - 15 日两天召开专家会讨论并投票表决是否应授权 Moderna 和杨森新冠疫苗的加强针 EUA。FDA 已公布了部分会前资料,文件列出了授权两款加强针的理由,但也指出,数据到目前为止还不清楚是否需要第三针。
FDA 科学家在 Moderna 疫苗的简报文件中...
|
|
FDA 授权辉瑞新冠加强疫苗,虽有限制适用人群仍然广...
2021.09.24
美国 FDA 于 9 月 22 日发布了针对辉瑞和 BioNTech 的新冠(COVID-19)疫苗加强针的紧急使用授权。FDA 表示,加强针的使用应仅限于 65 岁以上人群,18 至 64 岁严重新冠疾病高危人群以及因为工作而面临更高感染风险的人群,例如医护人员和教师等。
FDA 代理局长 Janet Woo...
|

|
【快讯】FDA 新冠疫苗加强针专家会:16-2 反对全员...
2021.09.18
北京时间 9 月 18 日 4 点 40,美国 FDA 就辉瑞新冠 mRNA 疫苗 COMIRNATY 的加强针申请召开的专家会结束。在经历了一整天对新冠疫苗加强针的讨论后,起初专家组投票反对批准辉瑞新冠疫苗的加强针,之后 FDA 修改了问题获得了专家组的一致通过。虽然讨论专门针对辉瑞新冠疫...
|

|
FDA 发布辉瑞新冠疫苗加强接种专家会会前资料,对加...
2021.09.16
根据美国 FDA 9 月 15 日公布的专家会会前资料,FDA 科学家对是否需要为所有接种过辉瑞新冠疫苗的人提供加强夹中表示怀疑。FDA 将于 9 月 17 日召开专家会议就哪些人群需要额外的加强接种以及何时需要加强接种进行辩论。
在文件中,FDA 自己的科学家似乎对广泛使用加强接种...
|

|
即将离任的 FDA 疫苗办公室正副主任柳叶刀发文称目...
2021.09.14
美国 FDA 疫苗研究与审评办公室(OVRR)主任和副主任在 9 月 13 日《柳叶刀》发布的一篇文章上表示,即使针对德尔塔变体,疫苗对严重新冠疾病的有效性仍然很高,从而在疫情现阶段对普通人群进行加强接种是不合适的。
这两名领导人 Marion Gruber(OVRR 主任)和 Phil Krause(O...
|
|
FDA 在两周后对辉瑞新冠疫苗加强针召开专家会,存在...
2021.09.03
美国 FDA 正在加快审评辉瑞/BioNTech 新冠疫苗 Comirnaty 的加强针补充申请。FDA 宣布将于 9 月 17 日召开专家咨询委员会会议,以审查补充生物制品许可申请(sBLA),即使当前手头的数据是否足以支持加强针的许可仍受到质疑。
疫苗和相关生物制品专家咨询委员会(VRBPAC)的召...
|
|
FDA 疫苗办公室主任和副主任将相继离任,不满疫苗决...
2021.09.01
美国 FDA 两位最资深的疫苗领导人将于今年秋天离任,他们在 FDA 工作了数十年,并且在美国新冠疫苗审评和授权行动中发挥了关键作用。
FDA 疫苗研究与审评办公室(OVRR)主任,在 FDA 工作了 32 年的资深官员 Marion Gruber 将于 10 月底离职,而担任 FDA OVRR 副主近 11 年的 ...
|
|
日本新冠疫苗微粒污染:针头错误插入小瓶导致污染,两...
2021.09.01
新冠疫苗的安全性问题一直处在人们关心的风口浪尖。前有强生和阿斯利康疫苗混淆污染导致千万剂疫苗报废的前车之鉴,现在,在日本有两人在接种受污染的 Moderna 疫苗死亡后,Moderna 也面临着对其疫苗的严重质疑。
根据上周六日本政府的报告,有两人在接种 Moderna 疫苗后死亡。Moder...
|

|
Moderna 新冠疫苗日本批次发现金属颗粒污染
2021.08.31
美国 Moderna 公司于 8 月 25 日表示正在调查一批发往日本的 mRNA 疫苗,该批疫苗可能受到污染。
Maderna 公司表示收到了“几起关于疫苗小瓶中的颗粒物的投诉。”投诉来自在日本销售的“一批产品”。日本共同社报道称,Moderna 在日本的疫苗合作伙伴武田(Takeda)已暂停使用发...
|

|
辉瑞新冠疫苗获 FDA 正式批准用于 16 岁以上人群
2021.08.24
美国 FDA 于本周一(8 月 23 日)宣布正式批准辉瑞和 BioNTech 的 mRNA 新冠(COVID-19)疫苗用于 16 岁及以上的个人,成为首个获得完全批准的新冠疫苗。
该疫苗之前于 2020 年 12 月 10 日获得 FDA 针对 16 岁以上人群的紧急使用授权(EUA)【辉瑞新冠疫苗专家会意...
|

|
FDA 开发新免疫分析和动物模型以评估疫苗对新发疾病...
2021.07.28
行业和学术研究人员正在开发针对各种病毒的新疫苗,包括禽流感病毒株(H5N1、H7N7、H7N9、H9N9)、呼吸道合胞病毒(RSV)、埃博拉、寨卡病毒和现在的新冠(SARS-CoV-2)病毒。新型“通用流感疫苗”也在开发中。许多这些疫苗正在与新型佐剂(刺激或增加对疫苗的免疫反应的试剂)一起开发...
|

|
欧盟、WHO 和各监管机构关注如何确定第二代新冠疫苗...
2021.07.20
欧洲药品管理局(EMA)正在与制药企业对话,以解释在安慰剂对照试验越来越难以进行的情况下,如何确定下一代新冠疫苗的保护效力。EMA 表示,将要求企业执行免疫桥接研究,直到为新冠疾病确定可接受的保护“免疫标志物”,该标志物可用作有效性的替代终点。
EMA 生物健康威胁和疫苗战...
|

|
WHO 用于预防传染病的 mRNA 疫苗质量、安全性和有...
2021.07.14
世界卫生组织(WHO)表示,由于新冠候选疫苗的临床试验、紧急使用批准或授权以及随后的广泛使用进展迅速,迫切需要对 mRNA 疫苗的评估提供指导。WHO 正在邀请利益相关者就一份文件草案提供反馈,文件概述了评估用于预防传染病的 mRNA 疫苗的质量、安全性和有效性的监管考虑因素。
...
|

|
CMO 混淆污染致千万剂疫苗报废:公司面临投资者反抗...
2021.07.07
美国 Emergent BioSolutions 公司自从今年 3 月份被爆出混淆了强生和阿斯利康的两种新冠疫苗原液以来,面临的麻烦不断升级。【CMO混淆污染致1500万剂新冠疫苗报废:冰冻三尺非一日之寒 2021/04/12】除监管机构要求停产整顿【CMO混淆污染致1500万剂新冠疫苗报废:FDA 关停工厂,隔离...
|

|
FDA 关于在 Emergent 生产的强生新冠疫苗原液的处...
2021.06.15
昨日,我们在【CMO混淆污染致千万剂疫苗报废:FDA 要求报废 6000 万剂,放行 1000 万剂】一文中报道了 FDA 对于 Emergent 工厂生产问题影响的疫苗原液批次的处理决定。今天我们来看看,FDA 生物制品审评与研究中心(CBER)主任 Peter Marks 医学博士撰写的关于这些批次处置决...
|