
|
FDA 发布一系列疫苗、诊断试剂和治疗指南应对新冠病...
2021.02.23
美国 FDA 于 2 月 22 日发布了一系列四篇指南以应对已出现以及未来可能出现的新冠(COVID-19)病毒变体,指南分别涉及疫苗、诊断试剂和治疗产品。
FDA 代理局长 Janet Woodcock 表示,“FDA 致力于寻找有效的方法来改良正在开发管线中的或已获紧急使用授权的医疗产品,以...
|

|
【一周回顾】2021.02.15-02.21
2021.02.22
药审中心发布生物类似药相似性评价和适应症外推技术指导原则。WHO 发布首个从纸质到数字化途径的 SMART 指南,推出新工具帮助各国建立儿童癌症计划。欧盟发布应对新冠病毒变体的计划。识林发布 FDA 药品质量办公室 2020 年度报告全文翻译。FDA 发布针对上海中华药业南通公司和印度 Shi...
|

|
协调表征细胞因子释放综合征促进 CAR-T 细胞疗法的...
2021.02.22
根据美国癌症研究之友最新发表的一份白皮书1,表征细胞因子释放综合征(CRS)将是确保免疫肿瘤学领域更广泛的接受先进细胞和基因疗法的关键。细胞因子释放综合征通常出现在新型免疫疗法中,例如,T 细胞抗体桥和 CAR-T 细胞。
美国 FDA 生物制品审评和研究中心(CBER)负责人 Peter ...
|

|
【周末杂谈】科学诚信与监管科学
2021.02.21
看FDA是如何提供促进和保护监管科学和科学家发展的制度环境
这周四《识林》报道了一家消费者公众组织质疑FDA在审评Biogen公司的阿尔茨海默药时的职业操守,以及FDA代理局长Janet Woodcock医学博士对此的回复【FDA 回复对阿尔茨海默药审评程序的批评,拒绝在申报前和申报后人员之间建...
|

|
瑞士药品管理局新指南详述抗癌药多国同步审批 Orbis...
2021.02.20
瑞士药品管理局(Swissmedic)已决定https//www.swissmedic.ch/swissmedic/en/home/news/mitteilungen/swissmedic-beteiligt-permanent-projekt-orbis.html 长久参与 Orbis 计划(Project Orbis),这是一项全球计划,允许参与机构同时审评新的癌症药物。Swissmedic 最近...
|
|
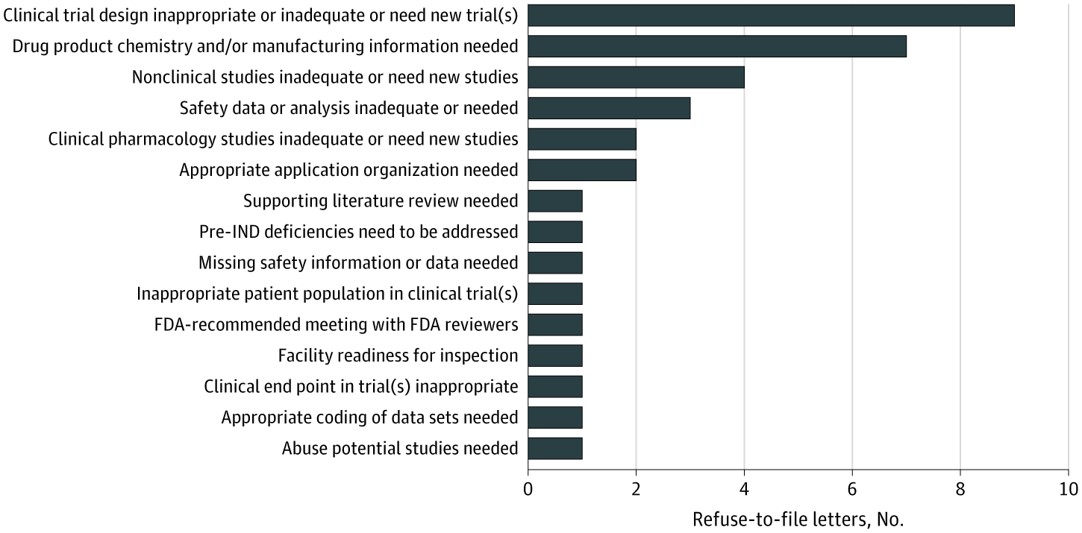
FDA 立卷审查拒收原因和公开披露情况分析
2021.02.19
日前发表在《美国医学会杂志》内科医学研究上的一项研究1发现,美国 FDA 通常会针对“实质性”缺陷发出立卷审查拒收(refuse-to-,RTF)函,这些缺陷包括缺少产品质量、安全性和有效性所需的信息。
这项研究的主要作者是 FDA 局长办公室公共卫生策略和分析人员 Harinder Singh Ch...
|

|
欧盟宣布应对新冠病毒变体的新计划
2021.02.19
欧盟于 2 月 17 日宣布了一项应对新冠(COVID-19)病毒变体的计划:将建立一个新的称为“HERA 孵化器“的生物防御准备计划,与欧盟和全球研究者、生物技术公司、制药商和公共机构合作,检测和评估新变体,为开发新型和调整疫苗提供激励措施,加快这些疫苗的批准程序,并确保扩大生产能...
|

|
FDA 回复对阿尔茨海默药审评程序的批评,拒绝在申报...
2021.02.18
美国 FDA 长期以来在可批准的申请方面一直采取协作方式与制药商合作,以将新药推向市场。但当一个药充满争议时,监管者和企业之间的这种关系就容易受到指责。
12 月,消费者倡导组织公共公民(Public Citizen)就 FDA 对 Biogen(渤健)有争议的阿尔茨海默药 aducanumab 上市...
|
|
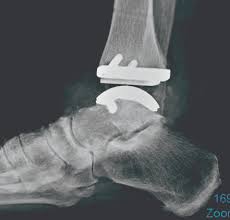
FDA 批准世界首个 3D 打印距骨植入物用于罕见骨病
2021.02.18
美国 FDA 于 2 月 17 日宣布批准了 Additive Orthopaedics 公司的患者特制距骨垫片(Patient Specific Talus Spacer)3D 打印距骨植入物用于人道主义用途。患者特制距骨垫片是世界上首个,也是同类首个用于替代距骨(连接腿和脚的踝关节中的骨骼)的植入物,用来治疗踝关节缺血...
|

|
使用 ICH Q12 方案简化分析方法的批准后变更,道阻...
2021.02.17
“人们普遍认为,PACMP 不会真正减少批准后的变更活动”
ICH Q12 指南实施工作组成员在 2 月 4 日的美国药典(USP)会议上表示,制药行业应利用 Q12 指南中有关批准后变更管理方案(PACMP)的规定促进分析方法的变更。
工作组成员、辉瑞工艺知识高级主管 Graham Cook 表...
|

|
FDA 肿瘤卓越中心 2020 年报,关注疫情下的癌症患...
2021.02.17
美国 FDA 肿瘤卓越中心(OCE)于 2 月 4 日发布了其 2020 年年报。OCE 主任 Richard Pazdur 在主任寄语中表示,“在COVID-19大流行期间,我们没有忘记癌症患者。我们的注意力一直集中在癌症患者身上,以确保这些患者在大流行期间不会被遗忘。”
Pazdur 表示,“在这一剧...
|
|
FDA 对非酒精性脂肪性肝炎(NASH)药物开发问题的解...
2021.02.16
在最近美国 FDA 举行的非酒精性脂肪性肝炎(NASH)的新药开发网络研讨会上,与会者提出了众多问题,显示了这一药物研发领域的热度。申办人们关心的问题涵盖从生物标志物的使用到试验时长。
在 1 月 29 日的研讨会上,FDA 药品审评与研究中心(CDER)免疫与炎症办公室肝病与营养...
|

|
【一周回顾】2021.02.08-02.14
2021.02.15
药审中心发布一批试行指南文件,国务院发布关于加快中医药特色发展的若干政策。欧盟开始滚动审评 CureVac 的新冠疫苗。FDA 发布 2020 年药品质量办公室年报和仿制药办公室年报,分别向中国上饶市春宇和美国 Allay 公司发布两封警告信。
上周热点资讯:
世界首套在药品生产线中...
|

|
【全文翻译】FDA 药品质量办公室 2020 年度报告
2021.02.15
美国 FDA 药品质量办公室(OPQ)于 2 月 11 日发布 2020 年年度报告,这是自 OPQ 成立以来发布的第四份年报(前三年的年报全文翻译点击相应年份阅览:2019 年;2018 年;2017 年)。今年的年报版式上与过去两年类似,但增加了多媒体链接,一些重要事项直接加入了相关视频链接...
|

|
【周末杂谈】热爱雪道
2021.02.14
当老师成为过时和多余,学生可以进入下一阶段学习时,教育才算成功
今天是大年初三,想必大家都沉浸在喜庆的过年气氛中。《周末杂谈》也凑个热闹,分享一篇关于孩子教育和成长的文章。原文刊载于今年一月的美联航Hemispheres旅游和购物杂志,用意恐怕是介绍美国怀俄明州著名的Jackson Ho...
|

|
FDA 药品质量办公室 2020 年度报告概览
2021.02.13
美国 FDA 药品质量办公室(OPQ)于 2 月 11 日发布 2020 年年度报告,这是自 OPQ 成立以来发布的第四份年报(前三年的年报全文翻译点击相应年份阅览:2019 年;2018 年;2017 年)。今年的年报版式上与过去两年类似,但增加了多媒体链接,一些重要事项直接加入了相关视频链接...
|
|
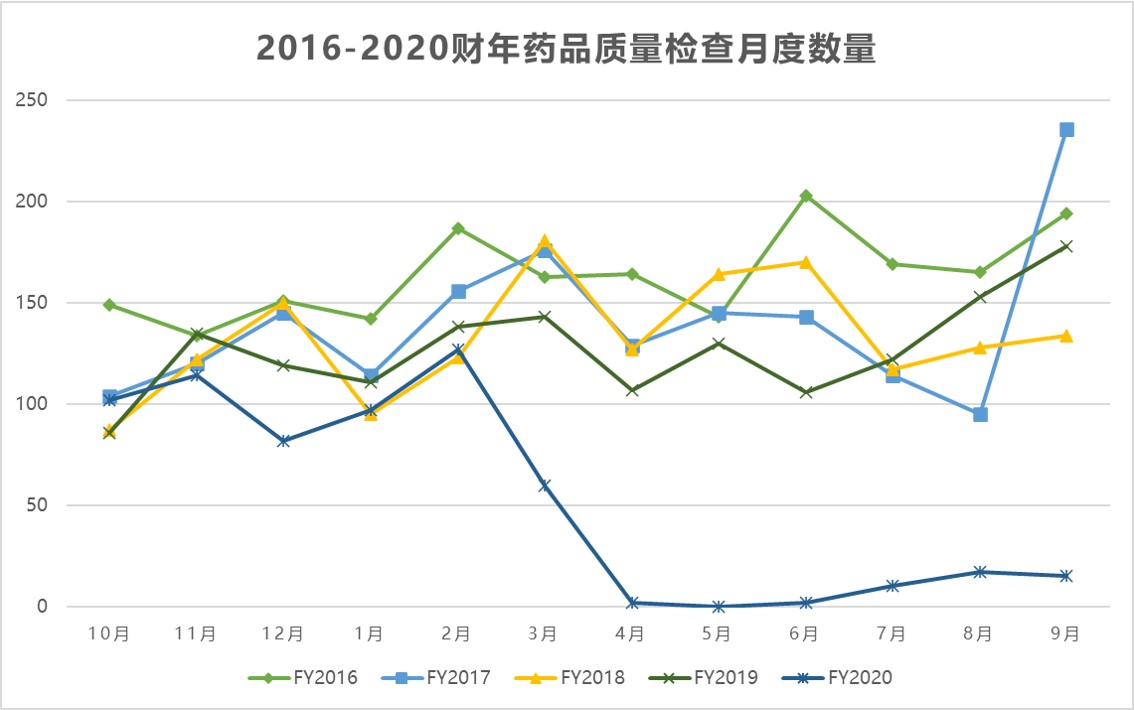
美国 FDA 检查分类情况回顾,做好准备迎接未来的检...
2021.02.12
识林祝大家过年好!牛年第一天我们来回顾一下 FDA 2020 财年的检查分类情况,以及通过这些数据,企业可以提前为未来的检查做哪些准备。
去年,疫情严重影响了美国 FDA 的执法计划,这一影响将在今年持续,并可能波及未来几年。上周识林集中报道了有关 FDA 首封基于远程记录审查的警...
|

|
欧盟 2020 年 PRIME 优先药品计划回顾
2021.02.10
欧洲药品管理局(EMA)的优先药品(PRIME)计划是一项旨在加强针对未获满足的医疗需求的药品的开发支持。2020 年,共有 20 个研究性药品获得 PRIME 认定,是该计划自 2016 年启动以来数量最多的一个年份(虽然数量差距较小)其中一些针对新治疗领域和适应症。
PRIME 于 2016 ...
|

|
EMA 提供 PRIME 优先药品计划工具箱指南,加速开发...
2021.02.10
欧洲药品管理局(EMA)正在试图帮助获得 PRIME(优先药品)计划认定的研究性药物开发人员,以最大程度地增大其快速开发产品并赢得上市许可的机会。
EMA 表示,“到目前为止的经验表明,在 PRIME 计划中为产品准备稳健的质量数据包时,开发者经常会遇到困难。”为解决这一问题,EMA...
|
|
Keytruda 乳腺癌新适应症审评简报,数据不足毒性大试...
2021.02.09
近日,美国 FDA 对默沙东(Merck & Co)用于治疗高危早期三阴性乳腺癌患者的 PD-1 免疫疗法 Keytruda(pembrolizumab)补充申请提出了多方面的批评。
根据 FDA 公布的计划于 2 月 9 日召开的肿瘤药专家会的会前简报资料显示,默沙东正在寻求对 Keytruda适应症补充申请...
|